我国明崇祯年间《徐光启手迹》记载了《造强水法》 :“绿钒(FeSO4•7H2O)五斤,硝五斤,将矾炒去,约折五分之一,将二味同研细,次用铁作锅,…… 锅下起火,取气冷定,开坛则药化为水……。用水入五金皆成水,惟黄金不化水中,加盐则化。……强水用过无力……”。下列有关解释错误的是
| A.“将矾炒去,约折五分之一”后生成FeSO4•4H2O |
| B.该方法所造“强水”为硝酸 |
| C.“惟黄金不化水中,加盐则化”的原因是加入 NaCl溶液后氧化性增强 |
| D.“强水用过无力”的原因是“强水”用过以后,生成了硝酸盐溶液,其氧化性减弱 |
18-19高三·湖北·开学考试 查看更多[11]
重庆市乌江新高考协作体2023-2024学年高三上学期12月期中联考化学试题(已下线)专题卷02 化学与传统文化-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)二轮专题强化练 专题7 化学与传统文化安徽师范大学附属中学2021-2022学年高三上学期11月考试化学试题(已下线)2021年高考化学押题预测卷(山东卷)02(含考试版、答题卡、参考答案、全解全析)湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)河南省郑州市第一中学2021届高三上学期开学测试化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】2020届高三《新题速递·化学》12月第01期(考点01-06)湖北省武汉市部分学校2020届新高三起点质量监测化学试题
更新时间:2019-09-11 14:28:55
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是
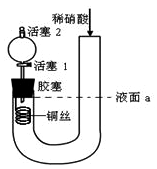

| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】1.52g铜镁合金完全溶解于50mL密度为1.40g•mL﹣1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体 1 120mL(标准状况),向反应后的溶液中加入1.0mol•L﹣1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是
| A.得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol•L﹣1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.该合金中铜与镁的物质的量之比是1:2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】X溶液中含有下表离子中的某5种,且其浓度均为 0. 1mol/L(不考虑水的电离与离子水解)。向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后 阴离子种类没有变化。下列叙述不正确的是
| 阳离子 | 阴离子 |
| Na+ 、Mg2+、Al3+、Ca2+ Fe2+ 、Fe3+ | OH−、CO32−、HCO3− Cl−、NO3−、SO42− |
| A.生成无色气体的离子方程式为:3Fe2+ +NO3−+4H+===3Fe3++NO ↑+2H2O |
| B.X溶液中不可能含有HCO3−或CO32− |
| C.根据电荷守恒,原溶液中一定含Mg2+ |
| D.X溶液中含有3种阳离子、2种阴离子 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】某小组在Fe2+检验实验中观察到异常现象,为探究“红色褪去”的原因,进行如下实验:
分析上述三个实验,下列叙述不正确 的是
| 编号 | 实验I | 实验II | 实验II |
| 实验步骤 | 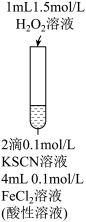 | 将实验I褪色后的溶液分三份分别进行实验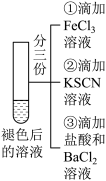 | 为进一步探究“红色褪去”的原因,又进行以下实验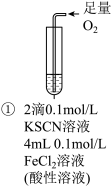 ②取反应后的溶液,滴加盐酸和BaCl2溶液 |
| 现象 | 溶液先变红,片刻后红色褪去,有气体生成(经检验为O2) | ①无明显现象 ②溶液变红 ③产生白色沉淀 | ①溶液变红,一段时间后不褪色。 ②无白色沉淀产生 |
| A.在此实验条件下H2O2氧化Fe2+的速率比氧化SCN-的速率快 |
| B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化 |
| C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与H2O2的氧化性有关 |
| D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列实验操作所对应的现象以及结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用坩埚钳夹住一小块用砂纸打磨过的铝箔,在酒精灯上加热 | 铝箔熔化并滴落 | 金属铝的熔点较低 |
| B | 先向某溶液滴加H2O2,然后再滴加几滴KSCN 溶液 | 溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 在KI 溶液中滴加少量氯水,再加入CCl4,充分振荡 | 液体分层,下层溶液呈紫红色 | 氯的非金属性强于碘 |
| D | 向1mL 0.1mol/L MgCl2 溶液中先滴1~2 滴2 mol/L NaOH溶液,再滴加2 滴0.1mol/L FeCl3溶液,静置 | 先有白色沉淀生成,后白色沉淀变为红褐色 | Ksp[Mg(OH)2]< Ksp[Fe(OH)3] |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】某溶液可能含有 、
、 、
、 、
、 、
、 、
、 、
、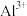 、
、 。某同学为了确认其成分,取部分试液,设计并完成了如下实验,由此可知原溶液中
。某同学为了确认其成分,取部分试液,设计并完成了如下实验,由此可知原溶液中
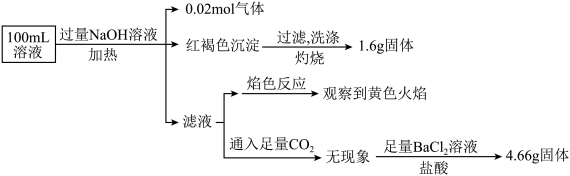
 、
、 、
、 、
、 、
、 、
、 、
、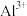 、
、 。某同学为了确认其成分,取部分试液,设计并完成了如下实验,由此可知原溶液中
。某同学为了确认其成分,取部分试液,设计并完成了如下实验,由此可知原溶液中

A.原溶液中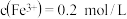 |
B.要确定原溶液中是否含有 ,其操作为:取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有 ,其操作为:取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有 |
C. 、 、 、 、 一定存在, 一定存在, 、 、 一定不存在 一定不存在 |
D.溶液中至少有4种离子存在,其中 一定存在,且 一定存在,且 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
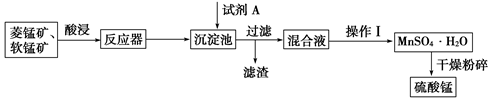
【推荐1】硫酸锰可用于饲料营养强化剂和媒染剂,其生产原材料软锰矿(MnO2)、菱锰矿(MnCO3)中常混有硫酸亚铁和硫酸镁等杂质。其生产工艺如图:
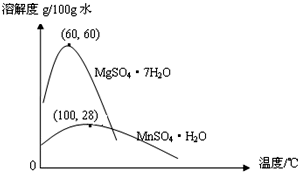
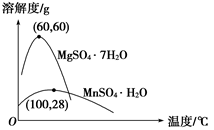
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图。
(2)完全沉淀离子的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。
下列判断正确的是( )
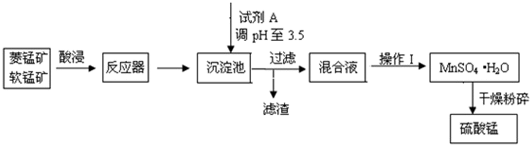
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图。
(2)完全沉淀离子的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。
下列判断正确的是( )
| A.试剂A可以选择H2O2,目的是将Fe2+氧化为Fe3+ |
| B.试剂A可选择氨水,目的是调节溶液的pH |
| C.操作Ⅰ包括蒸发、冷却结晶、趁热过滤、洗涤等步骤,洗涤时可用稀硫酸做洗液 |
| D.在蒸发结晶时,温度应该控制在60℃左右 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某学习小组在实验室通过6NaClO3 + CH3OH + 3H2SO4 = 6ClO2 + 5H2O + 3Na2SO4 + CO2制备ClO2,并将其转化为便于运输和储存的NaClO2固体,实验装置如图所示。(已知ClO2沸点为10℃,浓度较高时易发生爆炸)下列说法正确的是
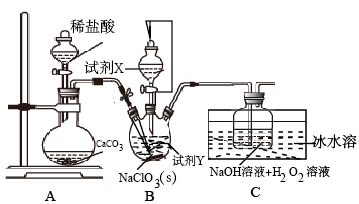

| A.试剂X是甲醇 |
| B.B中开始反应后立即停止通二氧化碳 |
| C.此实验可以不用冰水浴 |
| D.C中发生的反应方程式为:2ClO2+2NaOH+H2O2=2NaClO2+2H2O+O2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】硫酸锰可用于饮料营养强氧化剂和媒染剂。其生产原材料软锰矿(MnO2)、菱锰矿(MnCO3)中常混有硫酸亚铁和硫酸镁等杂质,生产工艺流程如图所示:
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图所示。
(2)各离子完全沉淀的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。下列判断正确的是
已知:(1)硫酸锰晶体和硫酸镁晶体的溶解度曲线如图所示。
(2)各离子完全沉淀的pH:Fe3+为3.5,Fe2+为9.5,Mn2+为10.8,Mg2+为11.6。下列判断正确的是
| A.试剂A应该选择H2O2,目的是将Fe2+氧化为Fe3+ |
| B.试剂A应该选择氨水,目的是调节溶液的pH |
| C.操作Ⅰ包括蒸发浓缩、冷却结晶、趁热过滤、洗涤等步骤,洗涤时可用稀硫酸作洗涤液 |
| D.通过操作Ⅰ得到MnSO4·H2O的过程中,包括蒸发结晶,在蒸发结晶时,温度应该高于60 ℃ |
您最近半年使用:0次



