名校
1 . 氧化还原反应原理在研究物质性质及物质转化等方面具有重要的价值。回答下列问题:
(1)按照不同的分类方法将下列化学反应进行分类。
a. ;b.
;b. ;c.
;c.
d. ;e.
;e.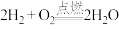 。
。
其中属于氧化还原反应,但不属于四大基本反应类型的是______ (填字母)。
(2)亚硝酸钠( )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:______ 。
(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为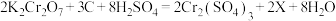

①该反应中,生成物X的化学式为______ 。
②该反应中,氧化剂为______ (填化学式),被氧化的元素为______ (填元素符号)。
③该反应中, 表现出
表现出______ (填字母)
A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol ,转移
,转移______ mol电子。
(1)按照不同的分类方法将下列化学反应进行分类。
a.
 ;b.
;b. ;c.
;c.
d.
 ;e.
;e.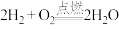 。
。其中属于氧化还原反应,但不属于四大基本反应类型的是
(2)亚硝酸钠(
 )具有致癌作用,许多腌制食品中含
)具有致癌作用,许多腌制食品中含 。酸性
。酸性 溶液与
溶液与 反应的化学方程式为
反应的化学方程式为 ,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:
,将它改写为离子方程式并用双线桥表示电子转移的方向和数目:(3)新储氢材料—碳纳米管可利用电弧法合成,合成过程中会伴随大量的碳纳米颗粒杂质,这种碳纳米颗粒杂质可用氧化气化法提纯,反应方程式为
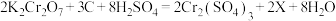

①该反应中,生成物X的化学式为
②该反应中,氧化剂为
③该反应中,
 表现出
表现出A.酸性 B.还原性 C.氧化性
④该反应中,每生成3mol
 ,转移
,转移
您最近一年使用:0次
2 . 回答下列问题
(1) 中氮元素的化合价为
中氮元素的化合价为___________ 价。
(2)已知 能发生反应:
能发生反应: 。用单线桥法表示该反应中电子转移情况
。用单线桥法表示该反应中电子转移情况___________ 。
(1)
 中氮元素的化合价为
中氮元素的化合价为(2)已知
 能发生反应:
能发生反应: 。用单线桥法表示该反应中电子转移情况
。用单线桥法表示该反应中电子转移情况
您最近一年使用:0次
名校
3 . 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素。
1.氯离子结构示意图为___________ ,碘在元素周期表中的位置是___________ 。
2.氯气可用来制取漂白粉,漂白粉的有效成分是___________ 。
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。___________
___________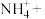 ___________
___________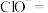 ___________
___________ ___________
___________ ___________
___________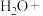 ___________
___________
1.氯离子结构示意图为
2.氯气可用来制取漂白粉,漂白粉的有效成分是
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。
___________
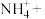 ___________
___________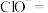 ___________
___________ ___________
___________ ___________
___________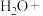 ___________
___________
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语正确的是
A.中子数为18的氯原子: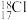 |
B.NaHCO3的电离方程式:NaHCO3=Na++H++ |
C.Al3+的结构示意图: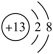 |
D.H2还原CuO反应中电子的转移: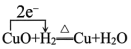 |
您最近一年使用:0次
解题方法
5 . 有氧时在硝化细菌作用下, 可转化为
可转化为 和
和 ,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)
,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)______ 。
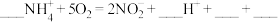 。
。
 可转化为
可转化为 和
和 ,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)
,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)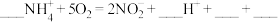 。
。
您最近一年使用:0次
6 . 高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。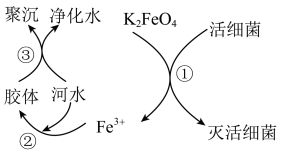
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
7 . CuCl在有机合成中常用作催化剂或还原剂,其一种制备方法为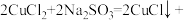
 ,下列说法错误的是
,下列说法错误的是
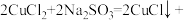
 ,下列说法错误的是
,下列说法错误的是| A.氧化剂和还原剂的物质的量之比为2∶1 |
| B.还原产物为CuCl |
C.电子转移的方向和数目可表示为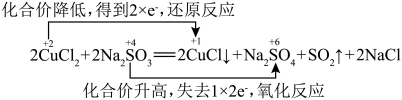 |
D.每转移1 mol ,生成 ,生成 的质量为142 g 的质量为142 g |
您最近一年使用:0次
名校
解题方法
8 . 某汽车安全气囊的产气药剂主要含有 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。
① 的电子式为
的电子式为_______ 。
②Na与冷水常温下发生反应,请写出该反应的化学方程式_______ 。
(2) 含有的化学键类型为
含有的化学键类型为_______ 。
(3)从结构组成的分类, 属于
属于_______ (选填“离子化合物”或“共价化合物”),请写出鉴别离子化合物和共价化合物的方法:_______ 。
(4)某些安全气囊产气药剂中含 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: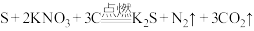
①标出该化学方程式电子转移的方向和数目_______ 。
②其中生成物 的电子式为
的电子式为_______ ; 的结构式为
的结构式为_______ 。
(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是_______ ,该元素单核负离子的结构示意图为_______ 。
 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。①
 的电子式为
的电子式为②Na与冷水常温下发生反应,请写出该反应的化学方程式
(2)
 含有的化学键类型为
含有的化学键类型为(3)从结构组成的分类,
 属于
属于(4)某些安全气囊产气药剂中含
 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: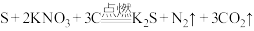
①标出该化学方程式电子转移的方向和数目
②其中生成物
 的电子式为
的电子式为 的结构式为
的结构式为(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是
您最近一年使用:0次
9 . 回答下列问题
将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO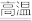 3Fe+4CO2 ②2KMnO4
3Fe+4CO2 ②2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
③Zn+H2SO4=ZnSO4+H2↑ ④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2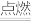 2CO2+3H2O ⑥3Fe+2O2
2CO2+3H2O ⑥3Fe+2O2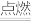 Fe3O4
Fe3O4
⑦CuO+H2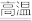 Cu+H2O
Cu+H2O
(1)属于化合反应的是___________ ,属于氧化还原反应的是___________ 。
铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(2)①用双线桥标出电子转移的方向和数目________________ 。
②硫元素被___________ (填“氧化”或“还原”)
③此反应中体现了硫酸的___________ 和___________ 。
(3)设NA为阿伏加德罗常数的数值,完成下列填空:
①1molCH4含 碳原子_____ mol,含氢原子_____ mol。
②标准状况下,0.5mol个CO2分子所占有的体积为__________ L。
③标准状况下,33.6LH2所含的分子数目为__________ 。
④34g H2O2的物质的量为_________ mol; 0.5molH2SO4的质量为________ g。
将符合下列反应类型的化学方程式的序号填入相应的横线中:
①Fe3O4+4CO
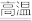 3Fe+4CO2 ②2KMnO4
3Fe+4CO2 ②2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑③Zn+H2SO4=ZnSO4+H2↑ ④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤C2H5OH+3O2
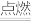 2CO2+3H2O ⑥3Fe+2O2
2CO2+3H2O ⑥3Fe+2O2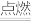 Fe3O4
Fe3O4⑦CuO+H2
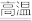 Cu+H2O
Cu+H2O(1)属于化合反应的是
铜和浓硫酸发生反应的化学方程式为Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O(2)①用双线桥标出电子转移的方向和数目
②硫元素被
③此反应中体现了硫酸的
(3)设NA为阿伏加德罗常数的数值,完成下列填空:
①1molCH4含 碳原子
②标准状况下,0.5mol个CO2分子所占有的体积为
③标准状况下,33.6LH2所含的分子数目为
④34g H2O2的物质的量为
您最近一年使用:0次
名校
10 . I:我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时发生的反应为:S+2KNO3+3C=K2S+N2↑+3X↑请回答:
(1)X的化学式是___________ ,按照物质的组成和性质分类,属于___________ (填字母)。
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)___________ 。
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。___________ 。
(4)在上述反应中,氧化剂为___________ ,氧化产物为___________ ,将两者的氧化性相比较,___________ 的氧化性更强。
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目___________ 。
(1)X的化学式是
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。

(4)在上述反应中,氧化剂为
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目
您最近一年使用:0次



