21. 弱电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为
___________________。
②下列方法中,可以使醋酸稀溶液中 CH3COOH 电离程度增大的是
__________________(填字母序号)。
a 滴加少量浓盐酸
b 微热溶液
c 加水稀释
d 加入少量醋酸钠晶体
(2)用 0.1 mol·L-
1 NaOH 溶液分别滴定体积均为 20.00 mL、浓度均为 0.1 mol·L-
1的盐酸和醋酸溶液,得到滴定过程中溶液 pH随加入 NaOH溶液体积而变化的两条滴定曲线。
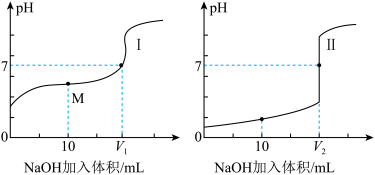
①滴定醋酸的曲线是
_______________(填“I”或“II”)。
②室温时,若 0.1 mol·L-
1的醋酸的电离度为 1%,计算这醋酸溶液的 pH 值
________。
③滴定开始前,三种溶液中由水电离出的 c(H
+)最大的是
________________。
④上述用 0.1 mol·L-
1的 NaOH 溶液滴定 0.1 mol·L-
1的盐酸,下列操作不正确的是
________________。
A.用标准 NaOH 溶液润洗碱式滴定管后,再装入标准碱溶液
B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
⑤上述滴定用酚酞作指示剂,滴定终点的现象
_______________________________________。