13. Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为
_________,基态Fe原子的电子排布式为
__________。
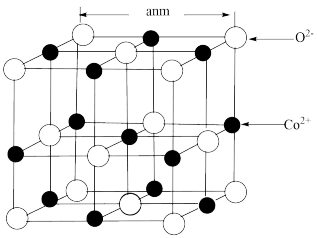
(2)CoO的面心立方晶胞如图所示。设阿伏加 德罗常数的值为
NA,则CoO晶体的密度为
______g﹒cm
-3:三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为
_______。
(3)Fe、Co、Ni能与Cl
2反应,其中Co和为Ni均生产二氯化物,由此推断FeCl
3、CoCl
3和Cl
2的氧化性由强到弱的顺序为
____,Co(OH)
3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:
______。
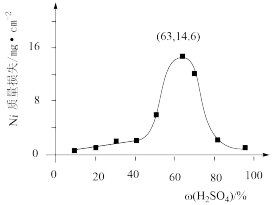
(4)95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示,当
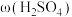
大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
_____。由于Ni与H
2SO
4反应很慢,而与稀硝酸反应很快,工业上选用H
2SO
4和HNO
3的混酸与Ni反应制备NiSO
4。为了提高产物的纯度,在硫酸中添加HNO
3的方式为
______(填“一次过量”或“少量多次”),此法制备NiSO
4的化学方程式为
_______。