新疆2021届高三上学期第一次联考化学试卷
新疆
高三
模拟预测
2021-01-13
635次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
新疆2021届高三上学期第一次联考化学试卷
新疆
高三
模拟预测
2021-01-13
635次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
1. 朱砂( )又称之为丹砂、辰砂,是一种红色的天然矿石,我国史前先民真正开始认识并使用朱砂可以追溯到湖北宜都城背溪文化,古代先贤们也给我们留下了很多关于“朱砂”的诗、词、句。下列有关叙述错误的是
)又称之为丹砂、辰砂,是一种红色的天然矿石,我国史前先民真正开始认识并使用朱砂可以追溯到湖北宜都城背溪文化,古代先贤们也给我们留下了很多关于“朱砂”的诗、词、句。下列有关叙述错误的是
 )又称之为丹砂、辰砂,是一种红色的天然矿石,我国史前先民真正开始认识并使用朱砂可以追溯到湖北宜都城背溪文化,古代先贤们也给我们留下了很多关于“朱砂”的诗、词、句。下列有关叙述错误的是
)又称之为丹砂、辰砂,是一种红色的天然矿石,我国史前先民真正开始认识并使用朱砂可以追溯到湖北宜都城背溪文化,古代先贤们也给我们留下了很多关于“朱砂”的诗、词、句。下列有关叙述错误的是| A.《自咏》(白居易)中记载:朱砂贱如土,不解烧为丹。指出朱砂在古代可用于炼丹 |
B.《本草从新》中记载:独用多用,令人呆闷。“令人呆闷”可能与 的毒性有关 的毒性有关 |
| C.“三尺讲台,序写华殇;朱批点点,娇比海棠”的“朱批”所用的原料是朱砂 |
| D.《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”包含两个置换反应 |
【知识点】 化学科学对人类文明发展的意义解读
您最近一年使用:0次
2021-01-12更新
|
359次组卷
|
3卷引用:新疆2021届高三上学期第一次联考化学试卷
新疆2021届高三上学期第一次联考化学试卷(已下线)微专题03 传统文化与物质的性质、转化-备战2022年高考化学考点微专题广东省揭阳市惠来县第一中学2021-2022学年高二上学期第一次阶段考试化学试题
单选题
|
适中(0.65)
2. NA是阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2L氯仿中含有分子的数目为0.5 NA |
B.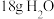 中含有的质子数和中子数均为10NA 中含有的质子数和中子数均为10NA |
| C.30g甲醛中含共用电子对总数为4NA |
| D.5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
3. 下列由实验得出的结论正确的是
| 实验 | 结论 | |
| A | 用小试管收集气体A做爆鸣实验,发现有爆鸣声 | A一定是 |
| B | 某气体充入澄清石灰水中,有白色沉淀 | 气体一定是 |
| C | 对某溶液做焰色试验时,观察到黄色火焰 | 溶液中弈定含有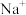 ,一定不含有 ,一定不含有 |
| D | 铁片投入到浓硫酸中,无现象 | 铁因钝化表面生成了氧化物保护膜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 1,4-二氧己环(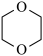 )主要用作溶剂、乳化剂、去垢剂等。下列关于1,4-二氧己环的叙述错误的是
)主要用作溶剂、乳化剂、去垢剂等。下列关于1,4-二氧己环的叙述错误的是
 )主要用作溶剂、乳化剂、去垢剂等。下列关于1,4-二氧己环的叙述错误的是
)主要用作溶剂、乳化剂、去垢剂等。下列关于1,4-二氧己环的叙述错误的是| A.所有原子共平面 | B.与2-甲基丙酸互为同分异构体 |
| C.核磁共振氢谱中只有一个吸收峰 | D.可以由乙二醇脱水生成 |
【知识点】 核磁共振氢谱解读 同分异构体书写 有机分子中原子共面的判断解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 下列对应的离子方程式书写正确的是
A.CaCO3的电离方程式: |
B.饱和Na2CO3溶液处理锅炉水垢: |
C. Mg(HCO3)2与足量的NaOH溶液: |
D.Fe(OH)3溶于氢碘酸溶液: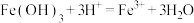 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 某白色固体混合物由两种物质组成,进行如下实验:
①取少量样品加入足量稀盐酸有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
改白色粉末可能为
①取少量样品加入足量稀盐酸有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
改白色粉末可能为
A. 、 、 | B. 、 、 |
C. 、 、 | D.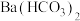 、 、 |
您最近一年使用:0次
7. 物质中少量杂质(括号内为杂质)的检验、除杂方法或试剂都正确的是
选项 | 物质及其杂质 | 检验 | 除杂 |
A |
|
| 饱和 |
B |
| 酸性 | 过量 |
C |
| 澄清石灰水 | 适量 |
D |
| 焰色试验 | 冷却结晶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-12更新
|
357次组卷
|
2卷引用:新疆2021届高三上学期第一次联考化学试卷
单选题
|
适中(0.65)
8. 常温下,保持体积不变,改变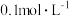 一元酸HA溶液的pH,溶液中HA、
一元酸HA溶液的pH,溶液中HA、 的物质的量分数
的物质的量分数 随pH的变化如图所示。下列叙述错误的是(已知
随pH的变化如图所示。下列叙述错误的是(已知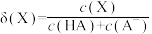 )
)

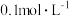 一元酸HA溶液的pH,溶液中HA、
一元酸HA溶液的pH,溶液中HA、 的物质的量分数
的物质的量分数 随pH的变化如图所示。下列叙述错误的是(已知
随pH的变化如图所示。下列叙述错误的是(已知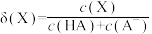 )
)
A.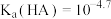 |
| B.a,b两点的pH之和等于9.4 |
C.b点存在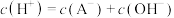 |
D.物质的量之比为 的HA,NaA的混合溶液呈酸性 的HA,NaA的混合溶液呈酸性 |
您最近一年使用:0次
2021-01-12更新
|
310次组卷
|
2卷引用:新疆2021届高三上学期第一次联考化学试卷
单选题
|
适中(0.65)
名校
11. 一种由短周期主族元素组成的化合物Р的结构式如图所示,其中元素W,X、Y,Z的原子序数依次增大,W,X的单质是空气的主要成分,W、Y同主族,P中Z原子满足最外层8电子结构。下列叙述错误的是

A.原子半径: | B.最高价氧化物水化物的酸性: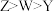 |
| C.W的液态简单氢化物可用作制冷剂 | D.P中,X、Y均显正价 |
您最近一年使用:0次
2021-01-12更新
|
371次组卷
|
3卷引用:新疆2021届高三上学期第一次联考化学试卷
单选题
|
适中(0.65)
12. 化学知识为环境保护提供了有力的专业保障,一种利用电化学原理设计的可监测空气质量的装置如图所示。下列叙述正确的是
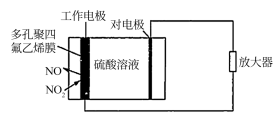

| A.“对电极”上发生的是还原反应 |
| B.工作过程中,电池液的pH不变 |
C.“工作电极”上发生的电极反应为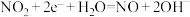 |
D.放大器接收电信号的强弱与空气中 浓度的大小有关 浓度的大小有关 |
【知识点】 原电池原理 原电池电极反应式书写解读
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
13. 一种铁催化剂催化反应的机理如图所示。下列叙述错误的是
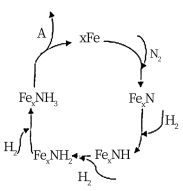
| A.反应过程中Fe元素的化合价没有变化 | B.Fe可以降低反应的能耗,活化能 |
C.物质A是 | D.该过程原子利用率达到了100% |
【知识点】 催化剂对化学反应速率的影响解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
14. 已知:25℃时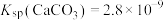 ,常温时,
,常温时, 在水中的溶解平衡曲线如图所示,下列叙述错误的是
在水中的溶解平衡曲线如图所示,下列叙述错误的是
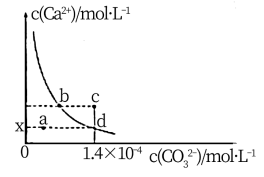
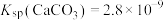 ,常温时,
,常温时, 在水中的溶解平衡曲线如图所示,下列叙述错误的是
在水中的溶解平衡曲线如图所示,下列叙述错误的是
A.加入少量的 固体可使溶液由a点变到d点 固体可使溶液由a点变到d点 |
| B.加入蒸馏水可使澄清溶液由b点变到d点 |
| C.c点液体经静置会变到曲线上b、d之间的某点 |
| D.曲线上的各点对应溶液的溶质可能不相同 |
您最近一年使用:0次
二、计算题 添加题型下试题
计算题
|
适中(0.65)
15. 过氧乙酸(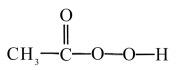 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是__________ ,所以过氧乙酸需要___________ 保存。
(2)过氧乙酸具有强氧化性,这与它的( )
)________ (填序号)键有关,向硫酸酸化的过氧乙酸溶液中加入少量KI溶液,溶液变黄,发生反应的离子方程式是_________ ,如有 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是___________ mol。
(3)过氧乙酸可由 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是_________ ,其中浓硫酸用量(浓硫酸占反应液的体积百分数)对过氧乙酸的含量的影响如图:___________ %(填整数)。
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
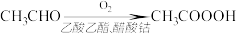
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为________ kg。
 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是
(2)过氧乙酸具有强氧化性,这与它的(
 )
) 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是(3)过氧乙酸可由
 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是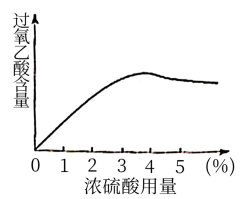
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
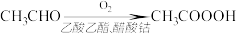
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为
【知识点】 氧化还原反应在生活、生产中的应用解读
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
解题方法
16. 利用磷石膏脱钙渣制备轻质碳酸钙流程如下:
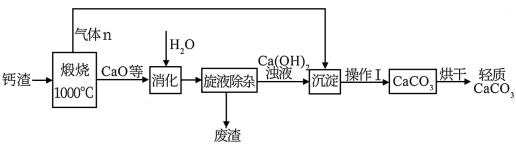
已知:磷石膏脱硫钙渣的成分
25℃时,几种物质的溶解情况
回答下列问题:
(1)煅烧前钙渣要进行粉碎处理,目的是_______ ,煅烧时发生的主要反应的化学方程式是__________ 。
(2)CaO消化后的产物是_________ (填化学式),消化时,水量过少,会造成产率下降,原因是________ 。
(3)旋液除杂时,难溶物下降, 形成悬浊液上升,实现了难溶物和悬浊液的分离,废渣的主要成分有
形成悬浊液上升,实现了难溶物和悬浊液的分离,废渣的主要成分有_________ 。
(4) 浊液中含有少量的
浊液中含有少量的________ (填化学式),它的存在________ (填“影响”或“不影响”)产品的纯度。
(5)操作Ⅰ的名称是___________ ,流程中,气体a如果没有全部被 浊液吸收,造成的后果有
浊液吸收,造成的后果有__________ 。

已知:磷石膏脱硫钙渣的成分
| 成分 |  |  |  |  | 其他 |
| 含量(%) | 87.35 | 1.60 | 1.77 | 9.20 | 0.08 |
| 物质 |  |  |  |
| 溶解度或溶解情况 | 0.165g | 不溶 | 0.2g |
(1)煅烧前钙渣要进行粉碎处理,目的是
(2)CaO消化后的产物是
(3)旋液除杂时,难溶物下降,
 形成悬浊液上升,实现了难溶物和悬浊液的分离,废渣的主要成分有
形成悬浊液上升,实现了难溶物和悬浊液的分离,废渣的主要成分有(4)
 浊液中含有少量的
浊液中含有少量的(5)操作Ⅰ的名称是
 浊液吸收,造成的后果有
浊液吸收,造成的后果有【知识点】 物质分离、提纯综合应用解读 物质制备的探究解读
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
17. 苯乙酮有特殊的芳香气味,沸点202℃,微溶于水,易溶于苯等有机溶剂。一种实验室利用无水 (易溶于水、苯,
(易溶于水、苯, 等)催化合成的方法如下:
等)催化合成的方法如下:
反应原理: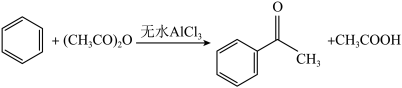
实验步骤:
Ⅰ、按图组装仪器
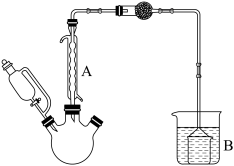
Ⅱ、依次在三颈烧瓶中加入搅拌子,10g无水 ,15mL无水苯,在搅拌下从恒压分液漏斗处滴入3mL(0.032mol)醋酸酐和5mL无水苯混合液,加热半小时至无HCl气体逸出为止。
,15mL无水苯,在搅拌下从恒压分液漏斗处滴入3mL(0.032mol)醋酸酐和5mL无水苯混合液,加热半小时至无HCl气体逸出为止。
Ⅲ、将三颈烧瓶浸入冷水浴中,加入25mL浓盐酸,25mL冰水,固体完全溶解后;分出苯层,水层每次用8mL苯萃取两次,合并苯溶液,依次用5%NaOH溶液、水各10mL洗涤上述苯溶液,再用无水 处理分液出的苯层。
处理分液出的苯层。
Ⅳ、蒸馏,收集馏分,得2.6g产品。回答下列问题:
(1)装置A的名称是________ ,使用恒压滴液漏斗的好处是__________ 。
(2) 干燥管的作用是
干燥管的作用是_________ ,B装置使用漏斗的目的是________ 。
(3)Ⅱ中,苯分两次加入,第一次加入的苯的作用是________ ,Ⅲ中,使用苯的作用是__________ ,Ⅲ中,使用次数最多的装置是__________ 。
A. B.
B.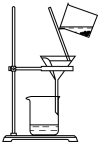 C.
C.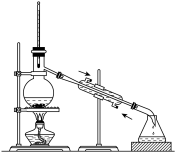 D.
D.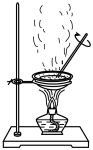
(4)使用5%NaOH的目的是除去苯层中的_____ ,使用无水 的目的是除去苯层中的
的目的是除去苯层中的____ 。
(5)蒸馏时,温度计指示刚到达202℃时,不能立即收集,原因是________ ,本实验中,苯乙酮的产率为_________ 。
 (易溶于水、苯,
(易溶于水、苯, 等)催化合成的方法如下:
等)催化合成的方法如下:反应原理:

实验步骤:
Ⅰ、按图组装仪器

Ⅱ、依次在三颈烧瓶中加入搅拌子,10g无水
 ,15mL无水苯,在搅拌下从恒压分液漏斗处滴入3mL(0.032mol)醋酸酐和5mL无水苯混合液,加热半小时至无HCl气体逸出为止。
,15mL无水苯,在搅拌下从恒压分液漏斗处滴入3mL(0.032mol)醋酸酐和5mL无水苯混合液,加热半小时至无HCl气体逸出为止。Ⅲ、将三颈烧瓶浸入冷水浴中,加入25mL浓盐酸,25mL冰水,固体完全溶解后;分出苯层,水层每次用8mL苯萃取两次,合并苯溶液,依次用5%NaOH溶液、水各10mL洗涤上述苯溶液,再用无水
 处理分液出的苯层。
处理分液出的苯层。Ⅳ、蒸馏,收集馏分,得2.6g产品。回答下列问题:
(1)装置A的名称是
(2)
 干燥管的作用是
干燥管的作用是(3)Ⅱ中,苯分两次加入,第一次加入的苯的作用是
A.
 B.
B. C.
C. D.
D.
(4)使用5%NaOH的目的是除去苯层中的
 的目的是除去苯层中的
的目的是除去苯层中的(5)蒸馏时,温度计指示刚到达202℃时,不能立即收集,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
18. 天然气中含有一定量的 气体;天然气脱硫及
气体;天然气脱硫及 的综合利用意义重大。
的综合利用意义重大。
(1) 在一定条件下可以发生如下反应:
在一定条件下可以发生如下反应:
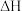 ,
,
相关物质的燃烧热数据如下表所示:
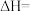
___________ 。
(2)化石燃料燃烧产生的 可以利用
可以利用 化会化转化为
化会化转化为 ,从而实现变废为宝,反应方程式为;
,从而实现变废为宝,反应方程式为;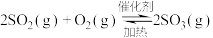

某温度时,在密闭容器中充入物质之比 的
的 和
和 ,保持温度不变,测得反应初始和平衡时的压强分别为
,保持温度不变,测得反应初始和平衡时的压强分别为 和0.7
和0.7 ,则平衡时,
,则平衡时, 的转化率为
的转化率为____________ , 的体积分数为
的体积分数为_________ ,
____________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)热分解是有效利用 的一种有开发前景的方法,反应原理为:
的一种有开发前景的方法,反应原理为: 。利用作图法可以计算某时刻的瞬时速率(在
。利用作图法可以计算某时刻的瞬时速率(在 变化曲线上画出该时刻对应点的切线,切线的斜率就是该时刻的瞬时速率),反应初期,
变化曲线上画出该时刻对应点的切线,切线的斜率就是该时刻的瞬时速率),反应初期, 热分解反应的
热分解反应的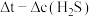 变化曲线如图所示,则A点的瞬时反应速率
变化曲线如图所示,则A点的瞬时反应速率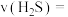
__________ ,随着反应的进行,瞬时反应速率的变化趋势是__________ 。
(4)电化学分解法也可以用来处理天然气中的 气体,从而获得硫和氢气。原理如下图所示:
气体,从而获得硫和氢气。原理如下图所示:
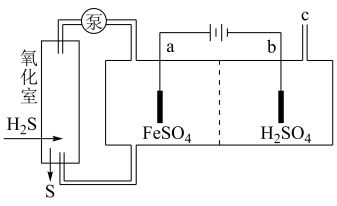
①a极上的反应式是_________ ;
②交换膜应选用________ (填“阳离子”、“阴离子”或“质子”)交换膜。
③氧化室发生反应的离子方程式是______________ 。
 气体;天然气脱硫及
气体;天然气脱硫及 的综合利用意义重大。
的综合利用意义重大。(1)
 在一定条件下可以发生如下反应:
在一定条件下可以发生如下反应:
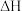 ,
,相关物质的燃烧热数据如下表所示:
| 物质 |  |  |
燃烧热 |  |  |
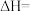
(2)化石燃料燃烧产生的
 可以利用
可以利用 化会化转化为
化会化转化为 ,从而实现变废为宝,反应方程式为;
,从而实现变废为宝,反应方程式为;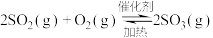

某温度时,在密闭容器中充入物质之比
 的
的 和
和 ,保持温度不变,测得反应初始和平衡时的压强分别为
,保持温度不变,测得反应初始和平衡时的压强分别为 和0.7
和0.7 ,则平衡时,
,则平衡时, 的转化率为
的转化率为 的体积分数为
的体积分数为
(3)热分解是有效利用
 的一种有开发前景的方法,反应原理为:
的一种有开发前景的方法,反应原理为: 。利用作图法可以计算某时刻的瞬时速率(在
。利用作图法可以计算某时刻的瞬时速率(在 变化曲线上画出该时刻对应点的切线,切线的斜率就是该时刻的瞬时速率),反应初期,
变化曲线上画出该时刻对应点的切线,切线的斜率就是该时刻的瞬时速率),反应初期, 热分解反应的
热分解反应的 变化曲线如图所示,则A点的瞬时反应速率
变化曲线如图所示,则A点的瞬时反应速率

(4)电化学分解法也可以用来处理天然气中的
 气体,从而获得硫和氢气。原理如下图所示:
气体,从而获得硫和氢气。原理如下图所示:
①a极上的反应式是
②交换膜应选用
③氧化室发生反应的离子方程式是
您最近一年使用:0次
四、填空题 添加题型下试题
19. 现有四种溶液m,n,p、q,分别含阴阳离子 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
(1)p是________ ,q是_________ (均填化学式)。
(2)写出在m中逐滴滴入p,沉淀减少时发生反应的离子方程式__________ 。
(3)实验室检验q中阳离子需要的试剂或试纸是___________ 。
(4)经分析, 存在于
存在于_________ (填m、n、p、q)溶液中,实验室常用重量法检验该溶液中 离子的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的
离子的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的 溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。
溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。
①所用量筒的规格为___________ 。
A.10mL B.50mL C.100mL D.500mL
②过滤时,沉淀物颗粒的大小会影响过滤速度,从利于过滤的角度分析,沉淀反应需要在接近沸腾的温度下进行的原因可能是__________ 。
③检验沉淀洗涤干净的方法是___________ 。
④计算,硫酸根的浓度为___________ mol/L(用含a的式子表示)。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。(1)p是
(2)写出在m中逐滴滴入p,沉淀减少时发生反应的离子方程式
(3)实验室检验q中阳离子需要的试剂或试纸是
(4)经分析,
 存在于
存在于 离子的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的
离子的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的 溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。
溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。①所用量筒的规格为
A.10mL B.50mL C.100mL D.500mL
②过滤时,沉淀物颗粒的大小会影响过滤速度,从利于过滤的角度分析,沉淀反应需要在接近沸腾的温度下进行的原因可能是
③检验沉淀洗涤干净的方法是
④计算,硫酸根的浓度为
您最近一年使用:0次
2021-01-12更新
|
826次组卷
|
5卷引用:新疆2021届高三上学期第一次联考化学试卷
新疆2021届高三上学期第一次联考化学试卷(已下线)第28讲 物质的分离、提纯和检验(精练)-2022年高考化学一轮复习讲练测(已下线)第05讲 离子共存 离子的检验和推断(精练)-2022年高考化学一轮复习讲练测西藏拉萨中学2022届高三第七次月考理综化学试题(已下线)第05讲 离子共存 离子的检验和推断(练)-2023年高考化学一轮复习讲练测(全国通用)
试卷分析
导出
整体难度:适中
考查范围:化学与STSE、认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
试卷题型(共 19题)
题型
数量
单选题
14
计算题
1
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 根据n=m/M进行相关计算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 3 | 0.85 | 酸性氧化物的通性 浓硫酸的强氧化性 焰色试验 离子的检验 | |
| 4 | 0.65 | 核磁共振氢谱 同分异构体书写 有机分子中原子共面的判断 | |
| 5 | 0.65 | 离子方程式的正误判断 Fe3+与其他物质氧化性强弱关系 沉淀转化 | |
| 6 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 无机物的检验 探究物质组成或测量物质的含量 | |
| 7 | 0.85 | 碳酸钠与碳酸氢钠性质的比较 铁盐、亚铁盐相互除杂 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 | |
| 8 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐的水解常数 盐类水解在解题方面的应用 弱电解质的电离平衡常数 | |
| 9 | 0.65 | 氯水的性质 硝酸的物理性质 二氧化硫的漂白性 | |
| 10 | 0.65 | 二氧化硅的化学性质 铁盐的检验 化学实验基础操作 | |
| 11 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 | |
| 12 | 0.65 | 原电池原理 原电池电极反应式书写 | |
| 13 | 0.94 | 催化剂对化学反应速率的影响 | |
| 14 | 0.65 | 沉淀溶解平衡的应用 同离子效应对难溶电解质溶解平衡的影响 | |
| 二、计算题 | |||
| 15 | 0.65 | 氧化还原反应在生活、生产中的应用 | |
| 三、解答题 | |||
| 16 | 0.65 | 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 17 | 0.65 | 有机物分离提纯操作的综合考查 常见有机物的制备 探究物质组成或测量物质的含量 | 实验探究题 |
| 18 | 0.65 | 盖斯定律的应用 化学反应速率计算 化学平衡常数的有关计算 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 四、填空题 | |||
| 19 | 0.65 | 离子反应的实际应用 无机综合推断 离子的检验 | |

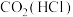
 溶液
溶液 溶液
溶液 溶液
溶液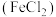
 溶液
溶液
 溶液
溶液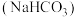
 溶液
溶液 晶体
晶体
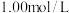 的
的 和湿润的
和湿润的 都有漂白性,二者混合后漂白性更强
都有漂白性,二者混合后漂白性更强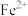 可用新制氯水和KSCN溶液检验
可用新制氯水和KSCN溶液检验

