13. 低能耗高效率的合成氨技术开发是实现氨燃料化利用的基础。探索新型合成氨技术是该领域研究热点之一。
回答下列问题:
(1)哈伯合成氨在较高温度下以氢气做氢源,氢气可由天然气制备。
CH
4(g)+H
2O(g)

CO(g) + 3H
2(g)
下表列出了几种化学键的键能:
| 化学键 | H-H | C-H | H-O | C O O |
| 键能kJ/mol | 436 | 413 | 467 | 1072 |
①298K时,上述反应的ΔH =
_______②为提高CH
4的平衡转化率,可采用的措施是
_______A.使用合适的催化剂
B.采用较高的温度
C.采用较高的压强 D.延长反应时间
③在1L刚性密闭容器中充入0.2molCH
4和1.0mol H
2O进行反应,加热时容器内温度升高。当温度升高至900K,若容器内n(CO)=0.1mol,此时反应
_______(填“正向进行”“逆向进行”“处于平衡状态”),若保持900K,达到平衡时再往容器内充入0.1molHe,v
正_______(填“增大”“减小”“不变”)(已知:900K时反应的平衡常数为1.2)
(2)催化剂的选择是合成氨的核心技术之一,使用催化剂1或催化剂2合成氨,产氨速率与温度的关系如图。

①根据由图判断,活化能Ea
1_______Ea
2(填“>”“=”“<”,下同)
②使用催化剂1或催化剂2时,合成氨的ΔH
1_______ΔH
2(3)电催化氮气还原合成氨是一种常温常压条件下利用水作为氢源的低碳环保路线,如图是电催化合成氨装置示意图。
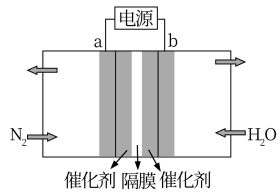
①a电极应该连接电源
_______极。
②电催化合成氨的化学方程式为
_______。