17. 第23号元素钒在地壳中的含量大约为0.009%,在过渡元素中仅次于Fe、Ti、Mn、Zn,排第五位。
(1)基态钒原子价电子排布图为
____。
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是
___。
(3)VCl
2溶液与乙二胺(H
2N—CH
2—CH
2—NH
2)可形成配离子[V(En)
2]
2+(En是乙二胺的简写)。乙二胺分子中氮原子的杂化轨道类型为
_____,乙二胺和三甲胺[N(CH
3)
3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是
_____。
(4)V
2O
5溶解在NaOH溶液中,可得到钒酸钠(Na
3VO
4),该盐阴离子的立体构型为
_____;也可以得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为
_____。


(5)钒能形成多种配合物,钒的两种配合物X、Y的化学式均为V(NH
3)
3ClSO
4,取X、Y的溶液进行如下实验(已知配体难电离出来)。
| X | X | Y | Y |
试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
____,Y的配体是
_____。
(6)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。CO作配体时,配位原子是C而不是O,其原因是
____。过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)
5]、[Mn(CO)
5]
-等都满足这个规则。已知化合物
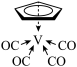
满足18电子规则,其配体“

”中的大π键可表示为
_____。
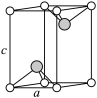
(7)VCl
2(熔点1027℃)和VBr
2(熔点827℃)均为六方晶胞,结构如图所示。设晶体中阴、阳离子半径分别为r
-和r
+,该晶体的空间利用率为
_____(用含a、c、r
+和r
-的式子表示)。