19. 研究甲醇的合成方法和用途具有重要的价值。
Ⅰ.利用合成气(CO和H
2)合成甲醇,发生如下反应:CO(g) + 2H
2(g)
⇌CH
3OH(g) ΔH
(1)由元素最稳定的单质生成1mol纯化合物时的反应热称为该化合物的标准摩尔生成焓(ΔH
f)。几种物质的标准摩尔生成焓如下表,则ΔH=
______kJ·mol
−1。
| 物质 | H2(g) | CO(g) | CH3OH(g) |
| ΔHf/kJ·mol-1 | 0 | -110.53 | -201.17 |
(2)800℃时,该反应平衡常数K=0.15.若某时刻c(CO)=0.1mol·L
−1、c(H
2)=0.2mol·L
−1、c(CH
3OH)=0.4mol·L
−1,此时v
正______v
逆(填“>”“<”、或“=”)。
(3)T℃时,在密闭的刚性容器中,按物质的量之比1∶1充入CO和H
2,若平衡时容器内总压为pPa,H
2 的转化率为50%。则T℃时,上述反应的平衡常数Kp=
______Pa
−2(用含p的代数式表示,Kp为用分压表示的平衡常数)。
Ⅱ.甲醇也可以通过微生物电催化反应合成,装置如图所示。
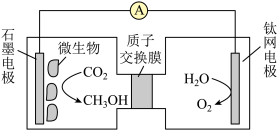
(4)石墨电极上的电极反应式为
______,当体系的温度升高到一定程度,电极反应的速率反而迅速下降,主要原因是
______。
Ⅲ.甲醇催化脱水制二甲醚日益受到关注,反应方程式为:2CH
3OH(g)
⇌CH
3OCH
3(g)+H
2O(g) ΔH<0,某催化反应的机理如下:
历程i:CH
3OH(g)→CH
3OH
◎历程ⅱ:CH
3OH
◎+CH
3OH
◎→CH
3OCH
3◎+H
2O
◎历程ⅲ:……
历程iv:H
2O
◎→H
2O(g)
上述历程中,“
◎”代表分子吸附在催化剂表面上。
(5)为提高CH
3OH的平衡转化率,可采用的措施是
______。
A.容积不变,充入一定量He
B.及时分离出H
2O(g)
C.进一步改进催化剂
D.降低反应温度
(6)历程ⅲ:
______。