17. 一种从废电池正极材料(含铝箔、LiCoO
2、Fe
2O
3及少量不溶于酸碱的导电剂中回收各种金属的工艺流程如图:
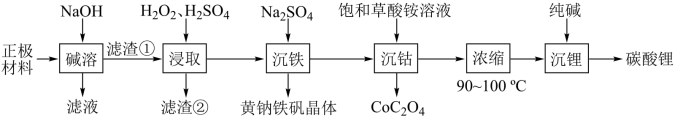
已知:①黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
②钴酸锂难溶于水,碳酸锂的溶解度随温度升高而降低。
③
Ksp(CoC
2O
4)=6.3×10
-8,
Ksp[Co(OH)
2]=6.3×10
-4。
回答下列问题:
(1)为了提高“碱溶”效率,可以采取的措施是
___(写出一条即可)。
(2)“浸取”时有无色气体产生,发生反应的离子方程式为
___。
(3)“沉钴”时采用饱和草酸铵溶液将钴元素转化为CoC
2O
4,与草酸钠溶液相比效果更好,原因是
___。
(4)“沉锂”后得到碳酸锂固体的实验操作为
___。
(5)“沉铁”时所得黄钠铁矾的化学式可表示为Na
xFe
y(SO
4)
m(OH)
n。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
I.称取4.850g样品,加盐酸完全溶解后,配成100.00mL溶液。
II.量取25.00mL溶液,加入足量的KI,用0.2500mol·L
-1Na
2S
2O
3溶液进行滴定至终点(I
2+2Na
2S
2O
3=2NaI+Na
2S
4O
6),消耗30.00mLNa
2S
2O
3溶液。
III.另取25.00mL溶液,加入足量BaCl
2溶液,充分反应后过滤、洗涤、干燥,得到沉淀1.165g。
用Na
2S
2O
3溶液进行滴定时,使用的指示剂为
___;黄钠铁矾的化学式为
___。
(6)高能锂离子电池的总反应为2Li+FeS=Fe+Li
2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF
6·SO(CH
3)
2为电解质)。
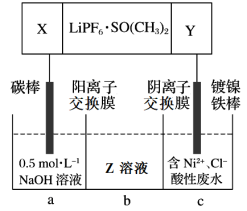
①电极X的反应材料是
___(填化学式);中间隔室b可以得到的主要物质Z是
___ (填化式)。
②电解总反应的离子方程式为
___。
已知F=96500C/mol,Q=It=n(e
-)·F。若电池工作tmin,维持电流强度为IA,理论回收Ni
___g(写出计算表达式即可)。