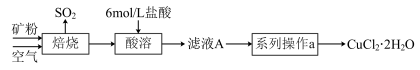
16. 某矿样中含有大量的CuS及少量其他不含铜不溶于酸的杂质。实验室中以该矿样为原料制备CuCl
2·2H
2O晶体,流程如下:
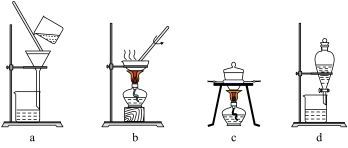
(1)①若在实验室中完成系列操作a。则下列实验操作中,不需要的是
____________(填字母)。
②CuCl
2溶液中存在平衡:Cu(H
2O)
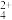
(蓝色)+4Cl
-
CuCl

(黄色)+4H
2O。欲用实验证明滤液A(绿色)中存在上述平衡,除滤液A外,下列试剂中还需要的是
_____(填字母)。
a.FeCl
3固体b.CuCl
2固体c.蒸馏水
(2)某化学小组欲在实验室中研究CuS焙烧的反应过程,查阅资料得知在空气中焙烧CuS时,固体质量变化曲线及SO
2生成曲线如图。
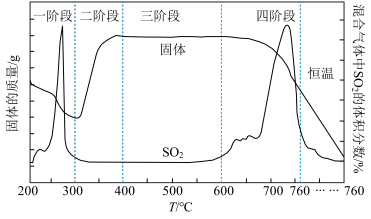
①CuS矿样在焙烧过程中,有Cu
2S、CuO·CuSO
4、CuSO
4、CuO生成,转化顺序为CuS

Cu
2S

CuO·CuSO
4
CuSO
4
CuO第①步转化主要在200~300℃内进行,该步转化的化学方程式
__________________。
②300~400℃内,固体质量明显增加的原因是
_________________.
③实验证明第四阶段所得混合气体所需试剂为
________、
________。
④若原CuS矿样的质量为10.0g,实验过程中,保持在760℃左右持续加热,待矿样充分反应后,所得固体的质量为8.4g,则原矿样中CuS的质量分数为
_____。