11. 科学工作者合成了含镁、镍、碳三种元素的超导材料,具有良好的应用前景。回答下列问题:
(1)镍元素在周期表中的位置
_______(2) CO易于铁触媒作用导致其失去催化活性: Fe+5CO=Fe(CO)
5,Fe(CO)
5又名羰基铁,常温下为黄色油状液体,则Fe(CO)
5的晶体类型是
_______,与CO互为等电子体的有
_______、
_______。(分子、离子各写1种)
(3)第一电离能介于Al、P之间的第三周期元素有
_______种,S
2Cl
2分子中S原子的杂化类型为
_______。
(4)过渡金属与O形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子的电子总数相同,称为有效原子序数规则。根据此规则推断,镍与CO形成的羰基配合物Ni(CO)
x中,x=
_______(5)离子水化能是气态离子溶于大量水中成为无限稀释溶液时释放的能量。离子在溶液中的稳定性可以从离子半径的大小、电荷、水化能等因素来解释。Cu
2+和Cu
+的水化能分别是-2121kJ/mol和-582kJ/mol,在水溶液里Cu
2+比Cu
+稳定的原因是
_______。
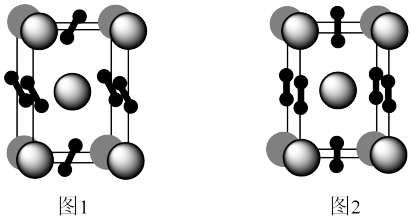
(6)如图表示的是某物质的两种结构的晶胞,(大球表示的是Ni原子,小球表示O原子),图1中的O
2单元空间取向有
_______种。若Ni之间底面上的最近距离为apm,竖直方向上为bpm,图2表示的晶体密度为
_______g/cm
3。(N
A表示阿伏加德罗常数)