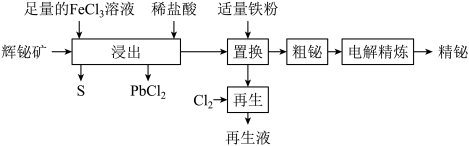
铋(Bi)及其化合物广泛应用于电子、医药等领域。以辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等) 为原料,采用湿法治金制备精铋工艺流程如下:
下列说法错误的是

下列说法错误的是
| A.“浸出”产生S 的主要离子反应为 6Fe3++Bi2S3=6Fe2++2Bi3++3S |
| B.“浸出”时使用稀盐酸主要目的是还原杂质 PbO2 |
| C.“电解精炼”时,粗铋应与电源的正极相连 |
| D.再生液可以加入“浸出”操作中循环利用 |
19-20高三·广东深圳·阶段练习 查看更多[3]
更新时间:2020/11/04 14:50:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
| A.NO | B.NO2 | C.N2O | D.NH4NO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
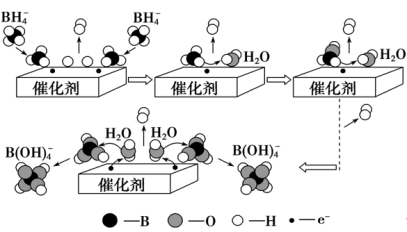
【推荐2】硼氢化钠( )是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
)是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
 )是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
)是有机反应中常用强还原剂,其在催化剂作用下与水反应获得氢气的微观过程如图所示。下列说法错误的是
| A.转化过程中,氢元素的化合价有−1价、0价和+1价 |
B. → → 过程中,既有化学键的断裂,又有化学键的形成 过程中,既有化学键的断裂,又有化学键的形成 |
C.总反应的实质为 中−1价氢与 中−1价氢与 中的+1价氢发生氧化还原反应生成氢气 中的+1价氢发生氧化还原反应生成氢气 |
| D.整个过程中出现了5种含硼微粒 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1mol  中 中 键的个数为14 键的个数为14 |
B.铜电解精炼时,当电路中通过 个电子时,阳极质量减少32g 个电子时,阳极质量减少32g |
C.标准状况下,22.4L苯乙烯( )含有的碳碳双键数目为 )含有的碳碳双键数目为 |
D.1mol超分子二苯并-18-冠醚-6( )中, )中, 杂化的原子总数为8 杂化的原子总数为8 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】电解原理在化学工业中有着广泛的应用。图甲表示电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列说法不正确的是
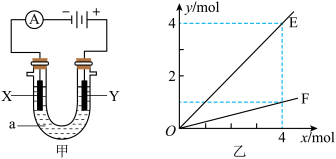

| A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解质溶液a可以是硫酸铜或氯化铜溶液 |
| B.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入1 mol的Cu(OH)2刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol |
| C.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 |
| D.若X、Y为铂电极,a溶液为500 mL KCl和KNO3混合液,经一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
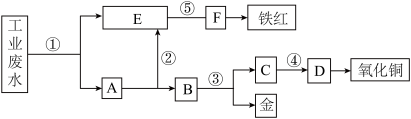
【推荐1】某工业废水显酸性,含有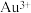 、
、 和
和 等离子,工业上为了变废为宝,常用酸、碱和废铁屑,将废水处理回收金、铁红和氧化铜。
等离子,工业上为了变废为宝,常用酸、碱和废铁屑,将废水处理回收金、铁红和氧化铜。
下列说法正确的是

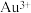 、
、 和
和 等离子,工业上为了变废为宝,常用酸、碱和废铁屑,将废水处理回收金、铁红和氧化铜。
等离子,工业上为了变废为宝,常用酸、碱和废铁屑,将废水处理回收金、铁红和氧化铜。 
下列说法正确的是


| A.A是Cu和Au的混合物 |
B. 是稀硝酸,分离出铁和铜 是稀硝酸,分离出铁和铜 |
C. 的离子方程式是 的离子方程式是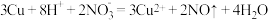 |
| D.F是氢氧化铁红褐色沉淀 |
您最近一年使用:0次
【推荐2】正高碘酸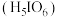 是白色结晶性粉末,能溶于水,主要用作氧化剂和分析试剂。由
是白色结晶性粉末,能溶于水,主要用作氧化剂和分析试剂。由 制取
制取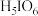 的实验流程如图所示:
的实验流程如图所示:
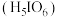 是白色结晶性粉末,能溶于水,主要用作氧化剂和分析试剂。由
是白色结晶性粉末,能溶于水,主要用作氧化剂和分析试剂。由 制取
制取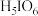 的实验流程如图所示:
的实验流程如图所示: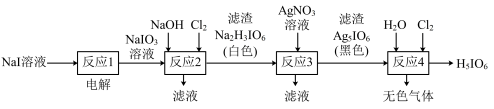
A.“反应1”是为了将 转化为 转化为 |
B.“反应2”中发生的反应是 |
C.“反应3”的滤液中含有大量的 等 等 |
| D.“反应4”得到的无色气体可能是氧气 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】锌冶炼过程中会产生大量的铅浮渣,其主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。利用铅浮渣生产硫酸铅的流程如下。下列说法不正确的是
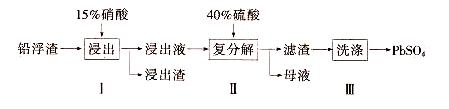

A.步骤Ⅰ中反应的离子方程式是:Pb+4H++2NO =Pb2++2NO↑+2H2O =Pb2++2NO↑+2H2O |
| B.复分解反应的方程式是:Pb(NO3)2+H2SO4= PbSO4↓+2HNO3 |
| C.为保证产品纯度,需控制硝酸的量以为防止Ag被溶解 |
| D.步骤Ⅱ得到的粗产品PbSO4 含有少量CaSO4杂质,还需用Pb(NO3)2溶液多次洗涤 |
您最近一年使用:0次



