综合利用海水可以制备金属镁,其流程如图所示。
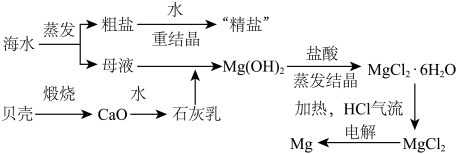
(1)煅烧贝壳过程中发生反应的化学方程式为________ ;Mg(OH)2与盐酸反应的离子方程式为_________ 。
(2)电解熔融MgCl2的化学方程式是__________ 。
(3)实验室里将粗盐制成“精盐”的过程中,在溶解、过滤、蒸发三个操作中都要用到玻璃棒,分别说明在这三个操作中玻璃棒的作用。
溶解:________ ;过滤:_________ ;蒸发:_________ 。
(4)若在空气中加热MgCl2·6H2O,生成的有MgO和HCl,写出相应反应的化学方程式:_________ 。

(1)煅烧贝壳过程中发生反应的化学方程式为
(2)电解熔融MgCl2的化学方程式是
(3)实验室里将粗盐制成“精盐”的过程中,在溶解、过滤、蒸发三个操作中都要用到玻璃棒,分别说明在这三个操作中玻璃棒的作用。
溶解:
(4)若在空气中加热MgCl2·6H2O,生成的有MgO和HCl,写出相应反应的化学方程式:
更新时间:2020/10/08 21:40:28
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】海水盐分中镁的占有量仅次于氯和钠,位居第三。镁具有重量轻、强度高等特点。海水提镁的主要流程如图:
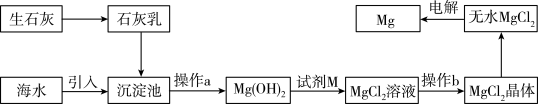
请回答下列问题:
(1)试剂M是____ ,操作b______ 。
(2)加入石灰乳的作用是___ ,写出沉淀池中发生反应的离子方程式:________ 。
(3)请写出无水MgCl2制得Mg的化学方程式_____ ,从节约成本和废物循环利用的角度考虑,反应产生的氯气可以用于制________ ,循环利用。
(4)有同学提出可直接由Mg(OH)2得到MgO,再电解熔融MgO制金属镁,你认为方法可行吗?___ (填“可行”或“不可行”),理由是_________ 。

请回答下列问题:
(1)试剂M是
(2)加入石灰乳的作用是
(3)请写出无水MgCl2制得Mg的化学方程式
(4)有同学提出可直接由Mg(OH)2得到MgO,再电解熔融MgO制金属镁,你认为方法可行吗?
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】海水是一种丰富的资源,工业上可从海水中提取多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。
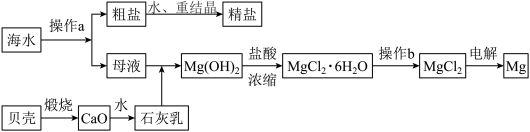
回答下列问题:
(1)海水淡化的方法主要有_____ (填任意一种)。
(2)从离子反应的角度思考,往海水中加入石灰乳的作用是_____ 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____ (填具体操作)。
②操作b是在若在空气中加热,则会生成Mg(OH)2,写出有关反应的化学方程式:_____ 。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为_____ ,从考虑成本和废物循环利用的角度,副产物氯气可以用于_____ 。

回答下列问题:
(1)海水淡化的方法主要有
(2)从离子反应的角度思考,往海水中加入石灰乳的作用是
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
②操作b是在若在空气中加热,则会生成Mg(OH)2,写出有关反应的化学方程式:
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:

(1)为了使MgSO4转化为Mg(OH)2,从经济角度上考虑,试剂①可以选用___________ [填“Ca(OH)2”或“NaOH”],要使MgSO4完全转化为沉淀,加入试剂①的量应___________ (填“少量”或“过量”)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是___________ (填“过滤”或“蒸发”)。
(3)试剂②可以选用___________ 。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为___________ 。

(1)为了使MgSO4转化为Mg(OH)2,从经济角度上考虑,试剂①可以选用
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是
(3)试剂②可以选用
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
您最近一年使用:0次



