将铁粉、铜粉、氧化铁、氧化铜溶于一定量的盐酸溶液中,充分反应,试判断下列情况溶液中存在的金属化合物。
(1)若铁粉有剩余,则溶液中一定有___________ (填溶质的化学式,下同)。
(2)若铜粉有剩余,则溶液中一定有___________ ,可能有___________ 。
(3)若溶液中有氯化铜,则溶液中一定还有___________ 。
(1)若铁粉有剩余,则溶液中一定有
(2)若铜粉有剩余,则溶液中一定有
(3)若溶液中有氯化铜,则溶液中一定还有
更新时间:2020/12/22 10:35:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】工业尾气中的氯气有多种处理方法。
(1)处理尾气中少量氯气的方法如图所示。
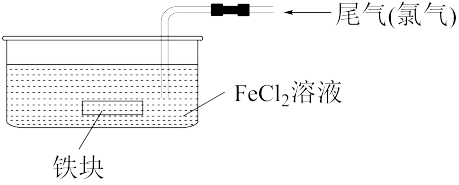
①处理过程中,发生反应的离子方程式为_______ 。
②为维持处理过程的持续进行,需要定期加入的物质是_______ 。
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为_______ mol。
(1)处理尾气中少量氯气的方法如图所示。

①处理过程中,发生反应的离子方程式为
②为维持处理过程的持续进行,需要定期加入的物质是
(2)大量氯气可用NaOH溶液处理,标准状况下,处理11.2L Cl2转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从古至今,铁及其化合物在人类的生产生活中都起了巨大的作用。
(1)中国四大发明之一的指南针由天然磁石制成的,其主要成分是___________(填字母)。
(2)将烧至红热的铁丝伸入盛有氯气的集气瓶中,可观察到有棕黄色的烟生成,该反应中被还原的物质是___________ (填化学式)。
(3)实验室用绿矾(FeSO4·7H2O)配制FeSO4溶液时,为防止FeSO4被空气氧化为Fe2(SO4)3,常向其中加入铁粉,写出加入铁粉的离子方程式___________ 。
(4)利用部分变质的FeSO4溶液制备Fe2O3:部分变质的FeSO4溶液 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
①写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式___________ 。
②“操作Ⅲ”的名称是___________ 。
(1)中国四大发明之一的指南针由天然磁石制成的,其主要成分是___________(填字母)。
| A.Fe | B.FeO | C.Fe3O4 | D.Fe2O3 |
(3)实验室用绿矾(FeSO4·7H2O)配制FeSO4溶液时,为防止FeSO4被空气氧化为Fe2(SO4)3,常向其中加入铁粉,写出加入铁粉的离子方程式
(4)利用部分变质的FeSO4溶液制备Fe2O3:部分变质的FeSO4溶液
 溶液Ⅰ
溶液Ⅰ 沉淀Ⅱ
沉淀Ⅱ Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。
Fe2O3;H2O2的作用是把FeSO4氧化为Fe2(SO4)3。①写出由“溶液Ⅰ”到“沉淀Ⅱ”反应的离子方程式
②“操作Ⅲ”的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】本题分为选做题(a)、(b)两道平行题,分值一样,可根据高一课程学习情况选择其中一道题完成作答,若二道题均作答,则按(a)题给分。
(a)有H、N、O、Na、Cl五种短周期主族元素。
(1)写出氯离子的原子结构示意图________ ,写出水分子的电子式________ 。
(2)NH4NO3是_______ 化合物(填“离子”或“共价”)。
(3)氯气是有毒气体,写出用饱和氢氧化钠溶液吸收氯气的离子方程式:_____________ 。
(4)金属元素铁是中学化学常见元素,将铁单质浸入氯化铁溶液中,该反应的离子方程式为__________ 。
(5)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出电极反应式。

正极反应式:___________________ ,负极反应式:___________________ 。
(a)有H、N、O、Na、Cl五种短周期主族元素。
(1)写出氯离子的原子结构示意图
(2)NH4NO3是
(3)氯气是有毒气体,写出用饱和氢氧化钠溶液吸收氯气的离子方程式:
(4)金属元素铁是中学化学常见元素,将铁单质浸入氯化铁溶液中,该反应的离子方程式为
(5)请依据(4)中的反应,设计一个原电池。要求:画出实验装置图,注明电解质溶液名称、正负极及正负极材料,并标出电子移动方向,写出电极反应式。

正极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将铁粉,铜粉,FeCl3溶液和CuCl2溶液混合于某溶液中充分反应,判断下列情况下,溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则溶液中不可能有的离子是_______ ,铜单质______ (填“一定”或“可能”)存在.
(2)若氯化铁和氯化铜都有剩余.则容器中不可能有的单质是_______ , Fe2+_______ ,(填“一定”或“可能”)存在。
(3)若充分反应后,容器中没有固体,则反应的化学方程式有________________ 。
(1)若铁粉有剩余,则溶液中不可能有的离子是
(2)若氯化铁和氯化铜都有剩余.则容器中不可能有的单质是
(3)若充分反应后,容器中没有固体,则反应的化学方程式有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】我们生活中处处都与化学有密切关系。
(1)洪灾过后,饮用水可用漂白粉消毒。工业上将氯气通入石灰乳 [Ca(OH)2]中制取漂白粉,反应的化学方程式为____________ 。
(2)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式__________________ ;如何检验FeCl3腐蚀铜后的溶液是否含Fe3+__________ 。
(3)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________ 。
(1)洪灾过后,饮用水可用漂白粉消毒。工业上将氯气通入石灰乳 [Ca(OH)2]中制取漂白粉,反应的化学方程式为
(2)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式
(3)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁、铜混合粉末18.0 g加入到100 mL 5.0 mol·L-1FeCl3溶液中,充分反应后,剩余固体质量为2.8g。求:
(1)剩余固体是___________ ;
(2)原固体混合物中铜的质量是___________ g;
(3)反应后溶液中n(Fe2+)+n(Cu2+)=___________ mol。
(1)剩余固体是
(2)原固体混合物中铜的质量是
(3)反应后溶液中n(Fe2+)+n(Cu2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与人类生活密切相关。请按要求回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 +3Cl2 +10KOH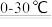 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____ ,当反应中有0.5mol K2FeO4生成时,消耗Cl2在标况下的体积为_________ ,转移电子的数目为_____ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式__________ 。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________ 。
(4)工业上制漂白粉的化学方程式为_______________________________ ,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______ 。
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_____________________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 +3Cl2 +10KOH
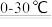 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(4)工业上制漂白粉的化学方程式为
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到消毒效果更好的___________ (填物质名称),将该反应的离子方程式补充完整:___________ ClO-+CO2+H2O=_____+_____。
(2)将铁粉投入到盛有Cu2+、Ag+、Fe3+的溶液中,反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不含的金属离子是___________ ,若烧杯中没有铁粉剩余,则溶液中一定含有的金属离子是___________ ,若溶液中不含有Cu2+时,则一定不含有的金属离子是___________ 。
(2)将铁粉投入到盛有Cu2+、Ag+、Fe3+的溶液中,反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不含的金属离子是
您最近一年使用:0次



