已知CaCrO4微溶于水,某传统测定CaCrO4溶度积的实验如下:
①配制250 mL待标定的K2CrO4溶液。
②标定测得K2CrO4溶液浓度为0.6025 mol/L。
③按下表数据将0.2000 mol/LCaCl2溶液、K2CrO4溶液及蒸馏水混匀,静置(溶液体积变化忽略不计)。
④取上层清液于锥形瓶中,加入H2SO4和H3PO4溶液酸化,溶液由黄色转变为橙色,加入指示剂,用0.2000 mol/L(NH4)2Fe(SO4)2溶液滴定,数据记入下表。
⑤滴定测出上层清液中的c( ),进而计算出上层清液中的c(Ca2+),即得Ksp(CaCrO4)。
),进而计算出上层清液中的c(Ca2+),即得Ksp(CaCrO4)。
回答下列问题:
(1)步骤①中无需使用下列哪些仪器_______ (填标号)。
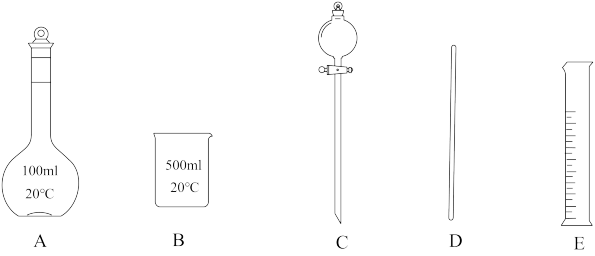
(2)基态Cr原子的电子排布式为_______ 。
(3)步骤④中所得橙色溶液中铬元素的主要存在形式为_______ (填化学式);滴定时还原产物为Cr3+,写出反应的离子方程式_______ 。
(4) 根据第2组滴定数据,计算得上层清液中c( )=
)=_______ mol/L。
(5)滴定时,有一组数据出现了明显异常,所测c( )偏大,原因可能有
)偏大,原因可能有_______ (填标号)。
A.滴定终点读数时仰视刻度线 B.达终点时滴定管尖嘴有标准液悬挂
C.盛装待测液的锥形瓶未润洗 D.摇动锥形瓶时有液体溅出
(6)利用上表数据经计算绘制出如下图点,请根据图点绘出溶度积曲线_________ 。
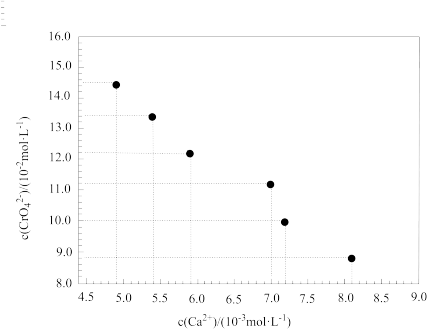
(7)请结合图线推测Ksp(CaCrO4)≈_______ (保留两位有效数字)。
①配制250 mL待标定的K2CrO4溶液。
②标定测得K2CrO4溶液浓度为0.6025 mol/L。
③按下表数据将0.2000 mol/LCaCl2溶液、K2CrO4溶液及蒸馏水混匀,静置(溶液体积变化忽略不计)。
④取上层清液于锥形瓶中,加入H2SO4和H3PO4溶液酸化,溶液由黄色转变为橙色,加入指示剂,用0.2000 mol/L(NH4)2Fe(SO4)2溶液滴定,数据记入下表。
组别 体积(mL) 物质 | 1 | 2 | 3 | 4 | 5 | 6 |
CaCl2 | 25.00 | 25.00 | 25.00 | 25.00 | 25.00 | 25.00 |
K2CrO4 | 15.00 | 16.00 | 17.00 | 18.00 | 19.00 | 20.00 |
蒸馏水 | 10.00 | 9.00 | 8.00 | 7.00 | 6.00 | 5.00 |
取上层清液 | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
耗(NH4)2Fe(SO4)2 | 13.33 | 15.00 | 16.78 | 18.42 | 20.15 | 21.89 |
 ),进而计算出上层清液中的c(Ca2+),即得Ksp(CaCrO4)。
),进而计算出上层清液中的c(Ca2+),即得Ksp(CaCrO4)。回答下列问题:
(1)步骤①中无需使用下列哪些仪器

(2)基态Cr原子的电子排布式为
(3)步骤④中所得橙色溶液中铬元素的主要存在形式为
(4) 根据第2组滴定数据,计算得上层清液中c(
 )=
)=(5)滴定时,有一组数据出现了明显异常,所测c(
 )偏大,原因可能有
)偏大,原因可能有A.滴定终点读数时仰视刻度线 B.达终点时滴定管尖嘴有标准液悬挂
C.盛装待测液的锥形瓶未润洗 D.摇动锥形瓶时有液体溅出
(6)利用上表数据经计算绘制出如下图点,请根据图点绘出溶度积曲线

(7)请结合图线推测Ksp(CaCrO4)≈
更新时间:2021-01-25 13:16:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,157℃时开始分解:
(1)探究草酸的酸性
25℃H2C2O4K1= 5.4 x 10-2,K2= 5. 4 x 10-5;H2CO3K1=4.5x10-7K2= 4.7X10-11
下列化学方程式可能正确的是________
A. H2C2O4+CO32-=HCO3-+HC2O4-B. HC2O4-+CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32-D. H2C2O4+CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物
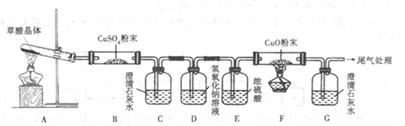
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:_______ ,证明有CO气体生成的现象是:_____________________
②写出H2C2O4分解的化学方程式_____________________
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液,再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀。填写下表:
(4)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.00mL于锥形瓶中再向瓶中加入足量稀H2SO4,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
①高锰酸钾溶液应装在_______ 滴定管中。(填“酸式”或“碱式”)
②滴定至终点时的实验现象是:______________ 。
③Na2C2O4的纯度是:______________
(1)探究草酸的酸性
25℃H2C2O4K1= 5.4 x 10-2,K2= 5. 4 x 10-5;H2CO3K1=4.5x10-7K2= 4.7X10-11
下列化学方程式可能正确的是
A. H2C2O4+CO32-=HCO3-+HC2O4-B. HC2O4-+CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32-D. H2C2O4+CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物

①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:
②写出H2C2O4分解的化学方程式
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加入4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液,再向乙试管中加入一粒黄豆大的MnSO4固体,摇匀。填写下表:
| 反应现象 | |
| 实验结论 | |
| 试管中发送反应的离子方程式 |
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.00mL于锥形瓶中再向瓶中加入足量稀H2SO4,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
①高锰酸钾溶液应装在
②滴定至终点时的实验现象是:
③Na2C2O4的纯度是:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】科学界目前流行的关于生命起源假设的理论认为生命起源于约40亿年前古洋底的热液环境,那里普遍存在铁硫簇合物,可用FexSy表示。为研究某铁硫簇合物成分,化学兴趣小组设计了如图所示的实验装置测定样品中铁、硫的含量。具体步骤为:
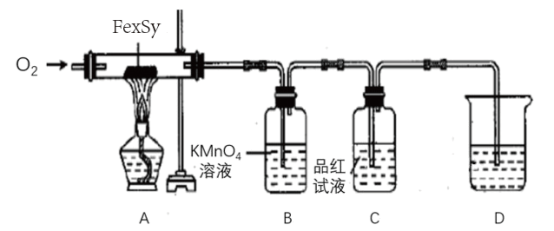
①按上图连接装置,进行气密性检查。
②在A中放入1.0g含杂质的样品(杂质不溶于水、盐酸,且不参与A中的反应),B中加入0.1mol/L酸性高锰酸钾溶液30mL,C中加入品红试液。
③通入氧气并加热,A中固体逐渐转变为红棕色。
④待固体完全转化后,取B中的溶液3mL于锥形瓶中,用0.1mol/L碘化钾溶液滴定。滴定共进行3次,实验数据记录于下表。
⑤取A中的残留固体于烧杯中,加入稀盐酸,充分搅拌后过滤。
⑥往滤液中加入足量氢氧化钠溶液,出现沉淀。过滤后取滤渣灼烧,得0.32g固体。
已知:Mn2+离子在极稀溶液中近乎无色。
回答下列问题:
(1)装置C中品红试液的作用是___________ 。有同学认为,撤去装置C,对此实验没有影响。你的观点是___________ (选填“赞同”或“不赞同”),理由是___________ 。
(2)用碘化钾溶液滴定酸性高锰酸钾时,生成碘单质和锰离子,写出反应的离子方程式___________ 。无色的草酸(H2C2O4)溶液也可代替碘化钾进行滴定,反应方程式为:2KMnO₄ + 5H₂C₂O₄+ 3H₂SO₄ →K₂SO₄ + 2MnSO₄ + 10CO₂ + 8H₂O,判断到达滴定终点时的现象应当是___________ 。
(3)为防止尾气污染,装置D中应加入___________ 溶液。
(4)根据上述实验所得数据,可确定该铁硫簇结构的化学式为___________ 。
(5)下列操作,可能导致x:y的值偏大的是___________ (填字母代号)
a.配置碘化钾标准液时,定容操作俯视刻度线。
b.步骤④所用锥形瓶未干燥,残留有蒸馏水
c.滴定时,碘化钾溶液不小心滴到锥形瓶外一滴
d.步骤⑥灼烧滤渣不够充分

①按上图连接装置,进行气密性检查。
②在A中放入1.0g含杂质的样品(杂质不溶于水、盐酸,且不参与A中的反应),B中加入0.1mol/L酸性高锰酸钾溶液30mL,C中加入品红试液。
③通入氧气并加热,A中固体逐渐转变为红棕色。
④待固体完全转化后,取B中的溶液3mL于锥形瓶中,用0.1mol/L碘化钾溶液滴定。滴定共进行3次,实验数据记录于下表。
| 滴定次数 | 待测液体积 /mL | 消耗碘化钾溶液体积 / mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 3.00 | 1.00 | 7.50 |
| 2 | 3.00 | 7.50 | 12.53 |
| 3 | 3.00 | 12.53 | 17.52 |
⑥往滤液中加入足量氢氧化钠溶液,出现沉淀。过滤后取滤渣灼烧,得0.32g固体。
已知:Mn2+离子在极稀溶液中近乎无色。
回答下列问题:
(1)装置C中品红试液的作用是
(2)用碘化钾溶液滴定酸性高锰酸钾时,生成碘单质和锰离子,写出反应的离子方程式
(3)为防止尾气污染,装置D中应加入
(4)根据上述实验所得数据,可确定该铁硫簇结构的化学式为
(5)下列操作,可能导致x:y的值偏大的是
a.配置碘化钾标准液时,定容操作俯视刻度线。
b.步骤④所用锥形瓶未干燥,残留有蒸馏水
c.滴定时,碘化钾溶液不小心滴到锥形瓶外一滴
d.步骤⑥灼烧滤渣不够充分
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】水合肼(N2H4·H2O)为无色透明液体,沸点为120℃,具有强还原性,能与水、醇混溶,不溶于乙醚和氯仿,在空气中可吸收CO2而产生烟雾。广泛应用于合成农药、水处理剂、发泡剂、引发剂和固化剂等,开发利用前景广阔。工业上用尿素[CO(NH2)2]、NaOH和NaClO溶液反应制备水合肼的实验流程如图:据此某化学兴趣小组设计了下列实验制备N2H4·H2O。回答下列问题:
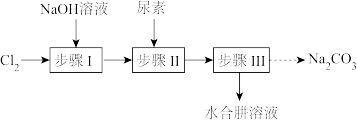
Ⅰ.制备NaClO溶液。实验制备装置如图所示:
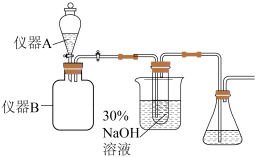
(1)仪器B中盛放试剂为Cl2,则仪器A中盛放的液体为___________ 。
(2)制备NaClO时,NaOH溶液用冰水浴控制温度在30℃以下,目的是___________ 。
(3)配制质量分数为30%的NaOH溶液时,下列仪器中除托盘天平外,还需要使用的是___________ 。(填仪器名称)
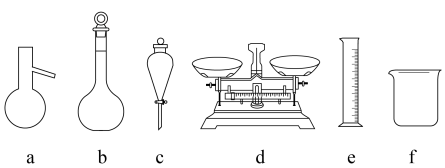
Ⅱ.制备水合肼
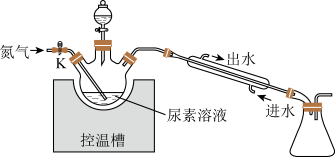
(4)分液漏斗中盛装的溶液是___________ (填字母)。
A.CO(NH2)2溶液 B.NaOH和NaClO溶液
三颈烧瓶中生成水合肼的化学反应方程式:___________ 。
(5)有同学认为该实验收集装置有缺陷,请你写出改进措施___________ 。
(6)水合肼的纯度测定:取ag样品配成溶液,加入一定量的碳酸氢钠固体,用0.1mol/LI2标准溶液滴定(已知N2H4·H2O+2I2=N2↑+4HI+H2O),进行三次平行实验,平均消耗I2标准溶液VmL。该样品的纯度为___________ %(用含a、V的代数式表示),若不加入适量NaHCO3固体,则测量结果会___________ (填“偏大”“偏小”“无影响”)

Ⅰ.制备NaClO溶液。实验制备装置如图所示:

(1)仪器B中盛放试剂为Cl2,则仪器A中盛放的液体为
(2)制备NaClO时,NaOH溶液用冰水浴控制温度在30℃以下,目的是
(3)配制质量分数为30%的NaOH溶液时,下列仪器中除托盘天平外,还需要使用的是

Ⅱ.制备水合肼

(4)分液漏斗中盛装的溶液是
A.CO(NH2)2溶液 B.NaOH和NaClO溶液
三颈烧瓶中生成水合肼的化学反应方程式:
(5)有同学认为该实验收集装置有缺陷,请你写出改进措施
(6)水合肼的纯度测定:取ag样品配成溶液,加入一定量的碳酸氢钠固体,用0.1mol/LI2标准溶液滴定(已知N2H4·H2O+2I2=N2↑+4HI+H2O),进行三次平行实验,平均消耗I2标准溶液VmL。该样品的纯度为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】精对苯二甲酸(PTA)是生产聚酯纤维的重要化工原料。生产过程产生的氧化残渣主要含有苯甲酸、对苯二甲酸、钴锰催化剂等。采用以下工艺流程可实现PTA残渣中有效成分苯甲酸和Co2+、Mn2+的回收与纯化,达到废物再利用的目的。
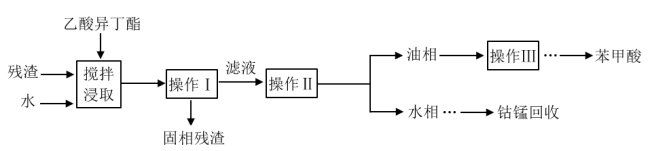
(1)操作I的方法是______ ;实验室进行操作Ⅱ主要用的玻璃仪器有_________ 。
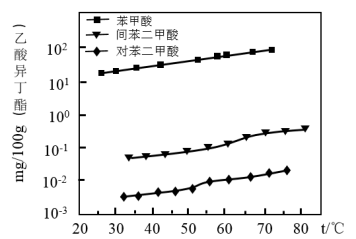
(2)判定乙酸异丁酯可用于浸取并有效回收苯甲酸的理由是_________ 。
(3)从上表所列实验数据可知苯甲酸在乙酸异丁酯中的溶解过程是_________ (填“放热”或“吸热”)过程。
(4)操作Ⅲ为蒸馏,蒸出的溶剂可返回_________ 工序循环使用。
(5)钴锰回收时常采用Na,S沉淀法将钴沉淀为CoS,若油水分离后的溶液经蒸发浓缩后,Co2+和Mn2+的浓度均为0.1mol∙L-1,计算说明当Co2+完全沉淀时产生的固体中不含MnS,支持这个结论的数学关系式是_________ 。[已知:Ksp(CoS)=2×10-25,Ksp(MnS)=2×10-13,完全沉淀指溶液中离子浓度小于10-5mol∙L-1]
(6)得到的CoS通过硫酸化焙烧转变为水溶性的CoSO4,其化学方程式为_________ 。


| 序号 | 浸取温度/℃ | 进料质量比溶剂:水:干残渣 | 苯甲酸浸取率/% |
| 1 | 30 | 4∶1∶1 | 87.48 |
| 2 | 40 | 4∶1∶1 | 90.33 |
| 3 | 50 | 4∶1∶1 | 90.81 |
(1)操作I的方法是
(2)判定乙酸异丁酯可用于浸取并有效回收苯甲酸的理由是
(3)从上表所列实验数据可知苯甲酸在乙酸异丁酯中的溶解过程是
(4)操作Ⅲ为蒸馏,蒸出的溶剂可返回
(5)钴锰回收时常采用Na,S沉淀法将钴沉淀为CoS,若油水分离后的溶液经蒸发浓缩后,Co2+和Mn2+的浓度均为0.1mol∙L-1,计算说明当Co2+完全沉淀时产生的固体中不含MnS,支持这个结论的数学关系式是
(6)得到的CoS通过硫酸化焙烧转变为水溶性的CoSO4,其化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】软锰矿是一种常见的锰矿物,其主要成分是MnO2,还含有Al2O3, Fe2O3, SiO2杂质。高锰酸钾具有强氧化性,在实验室中和工业上常用作氧化剂。以软锰矿为原料先制得锰酸钾,再使其在酸性条件下歧化而制得高锰酸钾的工艺流程如图所示。
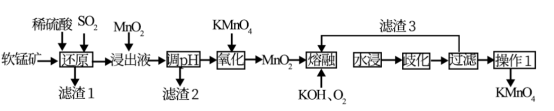
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“还原”中加稀硫酸的两个作用分别是__________________ 、___________ 。
(2)“滤渣2”的成分是____________ 。 利用上表格数据,计算Mn(OH)2的Ksp=______ (列出计算式)。
(3)“熔融”时生成锰酸钾的化学方程式为__________________ 。
(4) “歧化”时氧化剂与还原剂的物质的量之比为____________________ 。
(5) 操作1为蒸发浓缩,冷却结晶,减压过滤,“减压过滤”(装置如图所示)的目的是_____ 。

(6)由锰酸钾制备高锰酸钾除了有歧化法,还有电解法:以锰酸钾为电解液,镍板为阳极,铁板为阴极。
①写出生成高锰酸钾的电极反应式:___________ 。
②由电解法制备高锰酸钾时可循环利用的物质是________ (填化学式)。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Mn2+ |
| 开始沉淀时(c=0.01mol/L)的pH | 3.7 | 2.2 | 7.5 | 8.6 |
| 完全沉淀时(c=1.0×10-5mol/L)的pH | 4.7 | 3.2 | 9.0 | 10.1 |
(1)“还原”中加稀硫酸的两个作用分别是
(2)“滤渣2”的成分是
(3)“熔融”时生成锰酸钾的化学方程式为
(4) “歧化”时氧化剂与还原剂的物质的量之比为
(5) 操作1为蒸发浓缩,冷却结晶,减压过滤,“减压过滤”(装置如图所示)的目的是

(6)由锰酸钾制备高锰酸钾除了有歧化法,还有电解法:以锰酸钾为电解液,镍板为阳极,铁板为阴极。
①写出生成高锰酸钾的电极反应式:
②由电解法制备高锰酸钾时可循环利用的物质是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】用含铬不锈钢废渣(含 、
、 、
、 、
、 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:
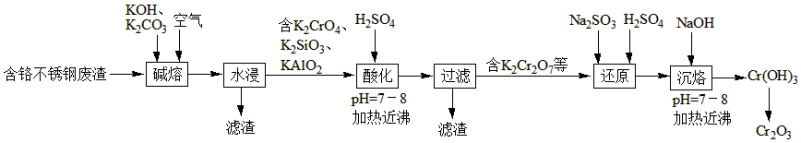
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是___________ 、___________ 。
(2) 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(3)“水浸”时,碱熔渣中的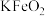 强烈水解生成的难溶物为
强烈水解生成的难溶物为___________ (填化学式,下同);为检验“水浸”后的滤液中是否含有 ,可选用的化学试剂是
,可选用的化学试剂是___________ 。
(4)常温下,“酸化”时pH不宜过低的原因是___________ ;若此时溶液的 ,则
,则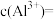
___________ mol/L。{已知:常温下,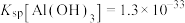 }
}
(5)“还原”时发生反应的离子方程式为___________ 。
(6)“沉铬”时加热近沸的目的是___________ ;由 制取铬绿的方法是
制取铬绿的方法是___________ 。
 、
、 、
、 、
、 等)制取
等)制取 (铬绿)的工艺流程如图所示:
(铬绿)的工艺流程如图所示:
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是
(2)
 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为(3)“水浸”时,碱熔渣中的
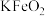 强烈水解生成的难溶物为
强烈水解生成的难溶物为 ,可选用的化学试剂是
,可选用的化学试剂是(4)常温下,“酸化”时pH不宜过低的原因是
 ,则
,则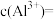
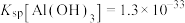 }
}(5)“还原”时发生反应的离子方程式为
(6)“沉铬”时加热近沸的目的是
 制取铬绿的方法是
制取铬绿的方法是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】水中的溶解氧是水生生物生存不可缺少的条件,某课外小组采用碘量法测定学校周边河水中的溶解氧,实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I−还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2 +I2=2I−+
+I2=2I−+ )。
)。
回答下列问题:
(1)氧的固定”中发生反应的化学方程式为_________________________________ 。
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、胶头滴管、试剂瓶和_________________________ ,配制溶液定容时俯视会导致Na2S2O3溶液的浓度__________ ,(填“偏高”或“偏低”)蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除________________ 及二氧化碳。
(3)取100.00 mL水样经固氧、酸化后,用0.5 mol·L−1Na2S2O3溶液滴定,以_________ 作指示剂,如何判断该反应到达终点_________________________________________________ ;若反应中消耗Na2S2O3溶液的体积为10 mL,则水样中溶解氧的含量为_________ mg·L−1。
(4)上述滴定完成时,若滴定前平视,滴定后仰视会导致测量结果___________ 。(填“偏高”或“偏低”)
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I−还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2
 +I2=2I−+
+I2=2I−+ )。
)。回答下列问题:
(1)氧的固定”中发生反应的化学方程式为
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、胶头滴管、试剂瓶和
(3)取100.00 mL水样经固氧、酸化后,用0.5 mol·L−1Na2S2O3溶液滴定,以
(4)上述滴定完成时,若滴定前平视,滴定后仰视会导致测量结果
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
查阅资料:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;
②2B+6HCl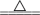 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;
③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:
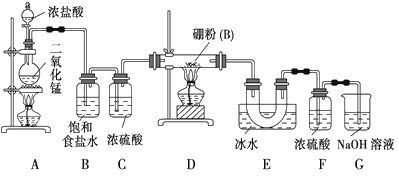
请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方式:___________________ 。
(2)E装置的作用是_______________ 。如果拆去B装置,可能的后果是__________________________ 。
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:_________________ ;
(4)为了顺利完成实验,正确的操作是________ (填序号).
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(5)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓_____________ (填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
II.实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0用0.1000 mol·L-1 NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是_____________________________
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(6)使用酸碱中和滴定的方法,用0.01 moL/L盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作能够使测定结果偏高的是___________________
A用量筒量取浓盐酸配制0.01 mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸
B配制稀盐酸定容时,俯视容量瓶刻度线
C滴定结束时,读数后发现滴定管下端尖嘴处悬挂有一滴液滴
D滴定过程中用少量蒸馏水将锥形瓶内壁附着的盐酸冲下
查阅资料:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;
②2B+6HCl
 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:

请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方式:
(2)E装置的作用是
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:
(4)为了顺利完成实验,正确的操作是
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(5)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓
II.实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0用0.1000 mol·L-1 NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(6)使用酸碱中和滴定的方法,用0.01 moL/L盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作能够使测定结果偏高的是
A用量筒量取浓盐酸配制0.01 mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸
B配制稀盐酸定容时,俯视容量瓶刻度线
C滴定结束时,读数后发现滴定管下端尖嘴处悬挂有一滴液滴
D滴定过程中用少量蒸馏水将锥形瓶内壁附着的盐酸冲下
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】结晶硫酸亚铁部分失水时,分析结果如仍按FeSO4·7H2O的质量分数计算,其值会超过100%。国家标准规定,FeSO4·7H2O的含量:一级品99.50%~100.5%;二级品99.00%~100.5%;三级品98.00%~101.0%。
为测定样品中FeSO4·7H2O的质量分数,可采用在酸性条件下与高锰酸钾溶液进行滴定。
5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O;
2MnO4-+5C2O42-+16H+→2Mn2++10CO2↑+8H2O
测定过程:粗配一定浓度的高锰酸钾溶液1L,然后称取0.200 g 固体Na2C2O4(式量为134.0)放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70℃~80℃。
(1)若要用滴定法测定所配的高锰酸钾溶液浓度,滴定终点的现象是_______________ 。
(2)将溶液加热的目的是____ ;反应刚开始时反应速率较小,其后因非温度因素影响而增大,根据影响化学反应速率的条件分析,其原因可能是______________________ 。
(3)若滴定时发现滴定管尖嘴部分有气泡,滴定结束气泡消失,则测得高锰酸钾浓度_____ (填“偏大”“偏小”“无影响”)。
(4)滴定用去高锰酸钾溶液29.50mL,则c(KMnO4)=_____ mol/L(保留四位有效数字)。
(5)称取四份FeSO4·7H2O试样,质量均为0.506g,,用上述高锰酸钾溶液滴定达到终点,记录滴定数据
该试样中FeSO4·7H2O的含量(质量分数)为_________ (小数点后保留两位),符合国家______ 级标准。
(6)如实际准确值为99.80%,实验绝对误差=____ %,如操作中并无试剂、读数与终点判断的失误,则引起误差的可能原因是:__________ 。
为测定样品中FeSO4·7H2O的质量分数,可采用在酸性条件下与高锰酸钾溶液进行滴定。
5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O;
2MnO4-+5C2O42-+16H+→2Mn2++10CO2↑+8H2O
测定过程:粗配一定浓度的高锰酸钾溶液1L,然后称取0.200 g 固体Na2C2O4(式量为134.0)放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70℃~80℃。
(1)若要用滴定法测定所配的高锰酸钾溶液浓度,滴定终点的现象是
(2)将溶液加热的目的是
(3)若滴定时发现滴定管尖嘴部分有气泡,滴定结束气泡消失,则测得高锰酸钾浓度
(4)滴定用去高锰酸钾溶液29.50mL,则c(KMnO4)=
(5)称取四份FeSO4·7H2O试样,质量均为0.506g,,用上述高锰酸钾溶液滴定达到终点,记录滴定数据
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(高锰酸钾)/mL(初读数) | 0.10 | 0.20 | 0.00 | 0.20 |
| V(高锰酸钾)/mL(终读数) | 17.76 | 17.88 | 18.16 | 17.90 |
(6)如实际准确值为99.80%,实验绝对误差=
您最近半年使用:0次



