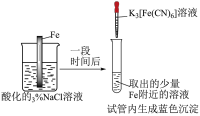
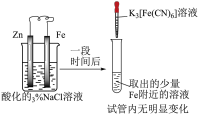
氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol。实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4kJ/mol。实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气。下列有关合成氨反应的说法正确的是
 2NH3(g) ΔH=-92.4kJ/mol。实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4kJ/mol。实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气。下列有关合成氨反应的说法正确的是 | A.反应的ΔS>0 |
| B.反应的ΔH=E(N-N)+3E(H-H)-6E(N-H) (E表示键能) |
| C.反应中每消耗1mol H2转移电子的数目约等于2×6.02×1023 |
| D.反应在高温、高压和催化剂条件下进行可提高H2的平衡转化率 |
2021·江苏·模拟预测 查看更多[3]
(已下线)押江苏卷第8题 化学反应速率与化学平衡、热化学 -备战2022年高考化学临考题号押题(江苏卷)(已下线)2.4 化学反应的调控-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)江苏省2021年普通高中学业水平选择考适应性测试化学试题
更新时间:2021-01-25 14:14:40
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知:N2(g)+3H2(g)⇌2NH3(l) ∆H1=akJ/mol反应历程的能量变化如曲线I,下列说法正确的是
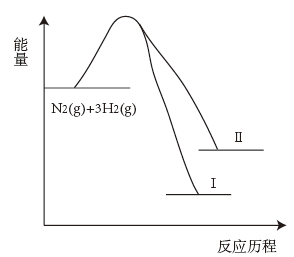

| A.1molN2(g)和3molH2(g)的总能量低于2molNH3(l)的总能量 |
| B.1molN2(g)和3molH2(g)中的化学键断裂时需要吸收|a|kJ能量 |
| C.正反应的活化能:曲线I>曲线II |
| D.曲线II对应的热化学方程式可能为N2(g)+3H2(g)⇌2NH3(g) ∆H2=bkJ/mol,且a<b |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应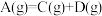 的能量变化如图所示,下列说法中正确的是
的能量变化如图所示,下列说法中正确的是
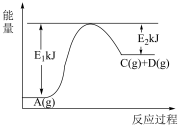
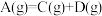 的能量变化如图所示,下列说法中正确的是
的能量变化如图所示,下列说法中正确的是
| A.C物质的能量一定高于A物质的能量 |
| B.反应物断键吸收的总能量小于产物形成新键放出的总能量 |
C. 晶体与 晶体与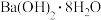 晶体反应中的能量变化符合左图关系 晶体反应中的能量变化符合左图关系 |
D.若使用催化剂,会使 、 、 减小,反应热 减小,反应热 减小 减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】尿酸(Uric acid)的化学式为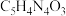 ,可用
,可用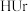 表示。痛风病与关节滑液中尿酸钠(
表示。痛风病与关节滑液中尿酸钠( )的沉积有关,
)的沉积有关, 增多,病情加重,其在体内产生的过程可表示为
增多,病情加重,其在体内产生的过程可表示为 。下列说法不正确的是
。下列说法不正确的是
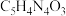 ,可用
,可用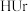 表示。痛风病与关节滑液中尿酸钠(
表示。痛风病与关节滑液中尿酸钠( )的沉积有关,
)的沉积有关, 增多,病情加重,其在体内产生的过程可表示为
增多,病情加重,其在体内产生的过程可表示为 。下列说法不正确的是
。下列说法不正确的是| A.寒冷季节更易诱发关节疼痛 | B.大量饮水会增大痛风病发作的可能性 |
| C.饮食中摄入过多食盐,会加重痛风病病情 | D.痛风病患者应少吃能代谢产生尿酸的食物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
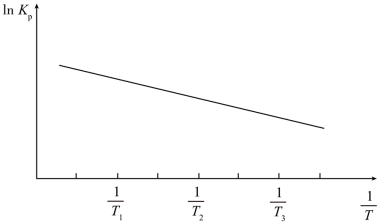
【推荐2】工业上用重晶石与焦炭在高温下反应: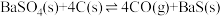 ,其
,其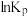 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
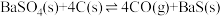 ,其
,其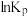 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.该反应的 |
| B.该反应在低温下能自发进行 |
| C.其他条件相同时,T1比T3时反应先达到平衡状态 |
| D.若温度在T2时达到平衡后,减压,再次到达平衡状态,CO的浓度增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列对化学平衡移动的分析中,不正确的是
①有气体参加的反应平衡时,若减小反应器容积时,平衡则向气体体积增大的方向移动
②有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡不会发生移动
③已达平衡的反应C(s)+H2O(g)⇌CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
④已达平衡的反应N2(g)+3H2(g)⇌2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,H2的转化率一定升高
①有气体参加的反应平衡时,若减小反应器容积时,平衡则向气体体积增大的方向移动
②有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡不会发生移动
③已达平衡的反应C(s)+H2O(g)⇌CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
④已达平衡的反应N2(g)+3H2(g)⇌2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,H2的转化率一定升高
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒温下,反应aX(g) bY(g)+cZ(s)达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断中正确的是
bY(g)+cZ(s)达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断中正确的是
 bY(g)+cZ(s)达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断中正确的是
bY(g)+cZ(s)达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断中正确的是| A.平衡向逆反应移动 | B.X的转化率减小 | C.a>b | D.a<b |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】液态的 可作制冷剂,
可作制冷剂, 还可用于制造铵态(
还可用于制造铵态( )氮肥和硝态(
)氮肥和硝态( )氮肥。20世纪初,德国化学家哈伯首次用锇作催化剂在
)氮肥。20世纪初,德国化学家哈伯首次用锇作催化剂在 Pa、550°C的条件下以
Pa、550°C的条件下以 和
和 为原料合成了
为原料合成了 :
:
 。2021年11月,我国报道了新的合成氨催化剂设计策略,该技术可实现温和条件下的氨催化合成。对于反应
。2021年11月,我国报道了新的合成氨催化剂设计策略,该技术可实现温和条件下的氨催化合成。对于反应 ,下列说法正确的是
,下列说法正确的是
 可作制冷剂,
可作制冷剂, 还可用于制造铵态(
还可用于制造铵态( )氮肥和硝态(
)氮肥和硝态( )氮肥。20世纪初,德国化学家哈伯首次用锇作催化剂在
)氮肥。20世纪初,德国化学家哈伯首次用锇作催化剂在 Pa、550°C的条件下以
Pa、550°C的条件下以 和
和 为原料合成了
为原料合成了 :
:
 。2021年11月,我国报道了新的合成氨催化剂设计策略,该技术可实现温和条件下的氨催化合成。对于反应
。2021年11月,我国报道了新的合成氨催化剂设计策略,该技术可实现温和条件下的氨催化合成。对于反应 ,下列说法正确的是
,下列说法正确的是| A.高温条件,有利于反应的自发进行 |
| B.升高温度,反应的化学平衡常数K增大 |
| C.增大压强,活化分子百分数增多,反应速率加快 |
D.若反应放出92.4kJ热量,则过程中有3mol 被氧化 被氧化 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
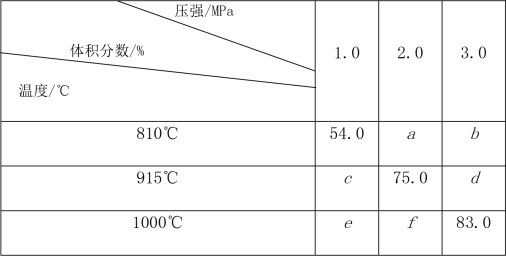
①b>f ②915℃,2.0MPa时E的转化率为60% ③该反应的ΔS<0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
①b>f ②915℃,2.0MPa时E的转化率为60% ③该反应的ΔS<0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实: ,下列叙述错误的是
,下列叙述错误的是
 ,下列叙述错误的是
,下列叙述错误的是A.使用 催化剂可大大提高生产效率 催化剂可大大提高生产效率 |
| B.该反应正向为熵增过程 |
C.充入大量 气体可提高 气体可提高 的转化率 的转化率 |
D.从混合气体中分离出 和 和 可提高 可提高 和 和 的利用率 的利用率 |
您最近半年使用:0次


 N2O4(g)
N2O4(g) H2(g)+I2
H2(g)+I2