题型:未知-未知
难度:0.4
引用次数:1159
题号:12194277
在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H= -164.7 kJ/mol
CH4(g)+2H2O(g) △H= -164.7 kJ/mol
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H= 41.2 kJ/mol
CO(g)+H2O(g) △H= 41.2 kJ/mol
反应III:2CO(g)+2H2(g) CO2(g)+CH4(g) △H= -247.1 kJ/mol
CO2(g)+CH4(g) △H= -247.1 kJ/mol
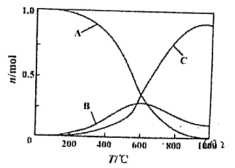
向恒压,密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2 的物质的量随温度的变化如图所示。下列说法正确的是
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H= -164.7 kJ/mol
CH4(g)+2H2O(g) △H= -164.7 kJ/mol反应II:CO2(g)+H2(g)
 CO(g)+H2O(g) △H= 41.2 kJ/mol
CO(g)+H2O(g) △H= 41.2 kJ/mol反应III:2CO(g)+2H2(g)
 CO2(g)+CH4(g) △H= -247.1 kJ/mol
CO2(g)+CH4(g) △H= -247.1 kJ/mol向恒压,密闭容器中通入1 mol CO2和4 mol H2,平衡时CH4、CO、CO2 的物质的量随温度的变化如图所示。下列说法正确的是

A.反应I的平衡常数可表示为K= |
| B.图中曲线B表示CO的物质的量随温度的变化 |
| C.CH4(g)+H2O(g) =CO(g)+3H2(g)的△H= -205.9 kJ/mol |
| D.提高CO2转化为CH4的转化率,需要研发在低温区高效的催化剂 |
更新时间:2021-01-25 14:14:40
|



