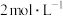K2Cr2O7溶液中存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。分别在26.3℃,50.0℃恒温条件下,往100mL0.100 mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下pH传感器连续测量溶液的pH,得到如下实验图象,下列说法正确的是
+2H+。分别在26.3℃,50.0℃恒温条件下,往100mL0.100 mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下pH传感器连续测量溶液的pH,得到如下实验图象,下列说法正确的是

 +H2O
+H2O 2CrO
2CrO +2H+。分别在26.3℃,50.0℃恒温条件下,往100mL0.100 mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下pH传感器连续测量溶液的pH,得到如下实验图象,下列说法正确的是
+2H+。分别在26.3℃,50.0℃恒温条件下,往100mL0.100 mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下pH传感器连续测量溶液的pH,得到如下实验图象,下列说法正确的是
| A.曲线①是50.0℃的pH-t曲线 |
| B.曲线②对应的平衡常数的数量级是10-14 |
C.t1后,c(Cr2O )+ c(CrO )+ c(CrO )=c(K+) )=c(K+) |
D.26.3℃,与0.100mol·L-1的K2Cr2O7溶液相比,达到新平衡时c2(CrO )/c(Cr2O )/c(Cr2O )增大 )增大 |
2021·福建·模拟预测 查看更多[8]
河北省石家庄市第二中学教育集团2021-2022学年高一下学期期末考试化学试题(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)课时37 化学平衡常数-2022年高考化学一轮复习小题多维练(全国通用)(已下线)难点8 水溶液中的四大平衡常数-2021年高考化学【热点·重点·难点】专练(新高考)江西景德镇市浮梁一中2020-2021学年高二下学期4月月考争优部化学试题(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密09 化学反应速率与平衡(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练福建省2021年普通高中学业水平选择考适应性测试化学试题
更新时间:2021-01-27 15:36:14
|
相似题推荐
【推荐1】合成淀粉的重要反应包括二氧化碳制备甲醇的反应,该反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是

 CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
CH3OH(g)+H2O(g)。该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态),下列说法错误的是
| A.曲线甲中过渡态中TS3最稳定 |
| B.催化剂可使反应历程中决速步骤的活化能降低0.2eV |
| C.化学平衡后,降低温度达新的平衡后甲醇的百分含量会增大 |
| D.图中使用催化剂的曲线是曲线乙 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
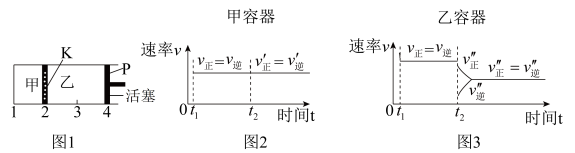
【推荐2】一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
| A.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减小 |
| B.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| C.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| D.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
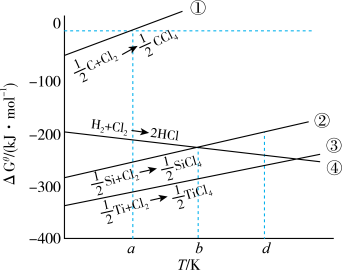
【推荐1】图表示生成几种氯化物反应的自由能变化 随温度变化情况。若在图示温度范围内焓变
随温度变化情况。若在图示温度范围内焓变 和熵变
和熵变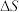 不变,且
不变,且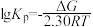 ,其中R为常数,T为温度。下列说法错误的是
,其中R为常数,T为温度。下列说法错误的是
 随温度变化情况。若在图示温度范围内焓变
随温度变化情况。若在图示温度范围内焓变 和熵变
和熵变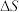 不变,且
不变,且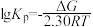 ,其中R为常数,T为温度。下列说法错误的是
,其中R为常数,T为温度。下列说法错误的是
A.反应①在温度a时的平衡常数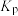 为1 为1 | B.反应②的平衡常数随温度升高而减小 |
| C.图示温度范围内,③是自发进行的 | D.任何温度下均可用 还原 还原 制备 制备 |
您最近半年使用:0次
【推荐2】在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应:2CO(g)+SO2(g) S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
下列说法正确的是
 S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。容器 | 起始时物质的量/mol | 平衡时CO2(g)的物质的量/mol | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 0 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.8 |
丙 | 2 | 1 | 0 | 0 | b |
| A.其他条件不变,容器乙达到平衡后,再充入体系中四种气体各1mol,平衡逆向移动 |
| B.b=1.6 |
| C.平衡常数:K甲>K乙 |
| D.其他条件不变,向容器甲再充入1mol CO,平衡常数(K)不变 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
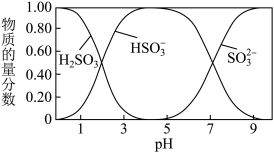
【推荐1】25℃时,起始浓度为0.1mol.L-1的亚硫酸溶液中,H2SO3、HSO 、SO
、SO 三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
 、SO
、SO 三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
| A.读取图中数据计算可得到常温下亚硫酸溶液的Ka2≈10-7 |
B.向该体系中加入一定量的NaOH固体,HSO 的物质的量分数一定增大 的物质的量分数一定增大 |
C.在pH=1.0溶液中:c(H2SO3)>c(HSO )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
D.在该体系中的任意一点都存在:c2(H+)=c(H+)·c(HSO )+2c(H+)∙c(SO )+2c(H+)∙c(SO )+Kw )+Kw |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
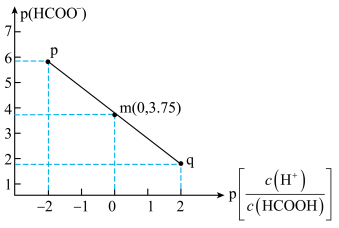
【推荐2】25℃下,将KOH溶液滴加到甲酸溶液中,测得混合溶液中的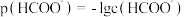 与
与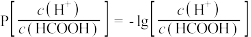 的变化关系如图所示。下列叙述错误的是
的变化关系如图所示。下列叙述错误的是
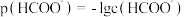 与
与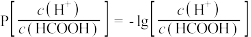 的变化关系如图所示。下列叙述错误的是
的变化关系如图所示。下列叙述错误的是
| A.25℃时 Ka(HCOOH)=10-3.75 |
B.滴加KOH溶液过程中, 始终不变 始终不变 |
| C.溶液中K+浓度:c(q)<c(p) |
D.m点所示溶液中 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】同温同压下,研究Cl2分别在不同浓度的盐酸和NaCl溶液中的溶解度(用溶解Cl2的物质的量浓度表示)变化如图所示。已知氯气在溶解时存在以下

①Cl2(aq)+H2O HClO+H++Cl- K1=4.2×10-4
HClO+H++Cl- K1=4.2×10-4
②Cl2(aq)+Cl- Cl3(aq) K2=0.19
Cl3(aq) K2=0.19
③HClO H++C1O- Ka=3.2×10-8
H++C1O- Ka=3.2×10-8
下列说法错误的是

①Cl2(aq)+H2O
 HClO+H++Cl- K1=4.2×10-4
HClO+H++Cl- K1=4.2×10-4②Cl2(aq)+Cl-
 Cl3(aq) K2=0.19
Cl3(aq) K2=0.19③HClO
 H++C1O- Ka=3.2×10-8
H++C1O- Ka=3.2×10-8下列说法错误的是
A.随着NaCl浓度的增大,Cl2溶解度减小,溶液中 减小 减小 |
| B.随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解 |
| C.a点时,c(H+)>c(Cl-)>c(Cl3-)>c(ClO-) |
| D.b点时,c(Na+)<c(Cl-)+c(Cl3-)+c(ClO-) |
您最近半年使用:0次

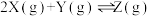
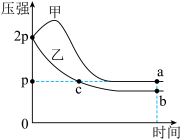


 的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应: ,已知该反应平衡常数与温度的关系如表:
,已知该反应平衡常数与温度的关系如表: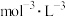 )
)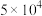
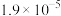
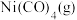
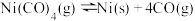 的平衡常数为
的平衡常数为
 、
、 浓度均为
浓度均为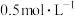 ,则此时
,则此时
 ,则
,则