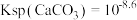三种难溶金属硫化物的溶度积常数(25℃):
下列有关说法中正确的是
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 1.59×10-19 | 1.3×10-36 | 4.65×10-14 |
| A.25℃时,CuS的溶解度大于MnS的溶解度 |
| B.25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-18mol/L |
| C.因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生 |
| D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
更新时间:2021-01-18 15:31:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述中不正确的是
| A.对于阴阳离子个数比相同的难溶电解质,溶度积大的溶解度也大 |
| B.向含有Ca(OH)2固体的溶液中加入适量的水使Ca(OH)2溶解,又达到平衡时,Ca(OH)2的溶度积不变 |
| C.将难溶电解质放入纯水中,达到沉淀溶解平衡时,难溶电解质电离出的离子的浓度之积就是该难溶电解质的溶度积 |
| D.AgCl水溶液的导电性很弱,但AgCl是强电解质 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
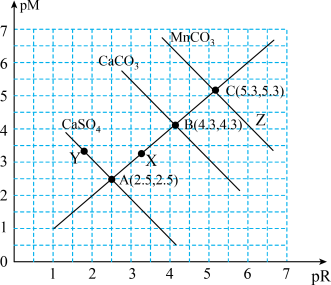
【推荐2】如图是 在温度分别为置T时的沉淀溶解平衡曲线[温度为
在温度分别为置T时的沉淀溶解平衡曲线[温度为 时
时 的
的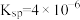 ,
,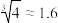 ]。下列说法正确的是
]。下列说法正确的是
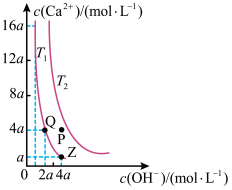
 在温度分别为置T时的沉淀溶解平衡曲线[温度为
在温度分别为置T时的沉淀溶解平衡曲线[温度为 时
时 的
的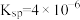 ,
,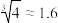 ]。下列说法正确的是
]。下列说法正确的是
A. |
B.温度为 时,P点分散系中分散质粒子直径均小于1nm 时,P点分散系中分散质粒子直径均小于1nm |
C.Q点对应的溶液中 约为 约为 |
| D.加水稀释时溶液碱性减弱,Z点对应的溶液可转化为Q点对应的溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式正确的是
A.向含氯化铁的氯化镁溶液中加入氧化镁: |
B.稀硫酸逐滴加入 溶液中,出现浑浊: 溶液中,出现浑浊: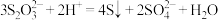 |
C.向血红色 溶液中加入过量铁粉至溶液褪色: 溶液中加入过量铁粉至溶液褪色: |
D.电解 水溶液: 水溶液: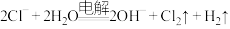 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】某研究小组为探究沉淀能否由一个溶解度较小的物质转化为溶解度较大的物质,设计了如下实验流程(每个实验步骤均充分反应)。
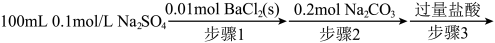
已知:该温度下,Ksp(BaSO4)=1×10-10, Ksp(BaCO3)=5×10-9,H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11]。忽略体积变化,下列说法正确的是
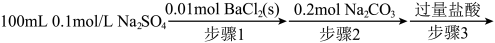
已知:该温度下,Ksp(BaSO4)=1×10-10, Ksp(BaCO3)=5×10-9,H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11]。忽略体积变化,下列说法正确的是
A.BaCO3悬浊液取上层清液,含碳微粒最主要以 形式存在 形式存在 |
B.反应BaSO4+  BaCO3 + BaCO3 + 正向进行,需满足 c( 正向进行,需满足 c( )/( )/( )>0.02 )>0.02 |
| C.经过步骤2,约有40%的BaSO4转化为BaCO3 |
D.取步骤2中上层清液,溶液中c(Na+) =2[c( )+c( )+c( )+(H2CO3) ] )+(H2CO3) ] |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,下列叙述中正确的是
| A.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B.将0.001 mol·L-1 AgNO3溶液滴入KCl和KI的混合溶液中,一定产生AgI沉淀 |
| C.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 |
| D.向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)>c(Cl-) |
您最近半年使用:0次
【推荐2】下列实验方案能够达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究生成物浓度改变FeCl3+3KSCN Fe(SCN)3+3KCl化学平衡的影响 Fe(SCN)3+3KCl化学平衡的影响 | 在平衡体系中加入KCl晶体,观察并比较实验现象 |
| B | 探究草酸浓度对反应速率的影响 | 向两支试管中分别加入2mL0.01mol/L的酸性KMnO4溶液,再同时分别向两支试管加入2mL0.1mol/L的H2C2O4溶液和2mL0.05mol/L的H2C2O4溶液,观察KMnO4溶液褪色所需时间 |
| C | 比较H2CO3和HClO酸性强弱 | 相同温度下,用pH试纸测定等浓度的NaHCO3和NaClO溶液的pH |
| D | 比较AgCl和AgI的Ksp大小 | 向盛有1mL0.1mol·L-1AgNO3溶液的试管中滴加2滴0.1mol·L-1NaCl溶液,有白色沉淀生成,向其中继续滴加几滴0.1mol/LKI溶液,有黄色沉淀产生 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

 H3O++CO32-
H3O++CO32- )=-lgc(CO
)=-lgc(CO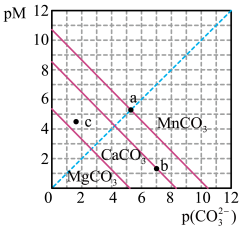
 和阴离子浓度的负对数
和阴离子浓度的负对数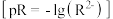 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是