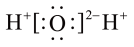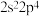现有四种元素基态原子的电子排布式如下:① ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是
 ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是| A.第一电离能:④>③>①>② | B.原子半径:④>③>②>① |
| C.电负性:④>③>①>② | D.最高正化合价:④>③=②>① |
20-21高二·全国·课后作业 查看更多[15]
(人教版2019)选择性必修2 阶段性综合评估测试卷(二)鲁科版2019选择性必修2阶段性综合评估测试卷(二)河北省石家庄市第二中学2022年高二寒假考试化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题重庆市朝阳中学2021-2022学年高二下学期期中考试化学试题湖北省武汉市钢城第四中学2021-2022学年高二下学期期中考试化学试题吉林省洮南市第一中学2022-2023学年高二下学期学习质量检测化学试卷新疆维吾尔自治区塔城地区2022-2023学年高二下学期5月期中化学试题广东省揭阳市三所中学联考2022-2023学年高二下学期4月期中考试化学试题陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题江西省丰城拖船中学2022-2023学年高二下学期6月期末考试化学试题吉林省长春市新解放学校2022-2023学年高二下学期7月期末考试化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二下学期第一次月考化学试题四川省南充市白塔中学2023-2024学年高二下学期第一次(3月)月考化学试题新疆阿克苏市实验中学2023-2024学年高二下学期第一次月考化学试题
更新时间:2021/02/01 21:16:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中,正确的是
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层 |
| C.微粒的最外层只能是8个电子才稳定 |
| D.在多电子的原子里,能量高的电子通常在离核远的区域内活动 |
您最近一年使用:0次
【推荐2】现有2种元素的基态原子的电子排布式如下:①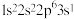 ;②
;② 。下列比较中不正确的是
。下列比较中不正确的是
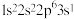 ;②
;② 。下列比较中不正确的是
。下列比较中不正确的是| A.非金属性:②>① | B.简单离子半径:①<② |
| C.原子半径:①>② | D.元素的最高正化合价:①<② |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关第一电离能的叙述正确的是
| A.一般来说,同周期元素中ⅦA族元素的第一电离能最大 |
| B.C、N、O三种元素第一电离能从大到小的顺序是O>N>C |
| C.第ⅠA、ⅡA族元素的原子,其原子半径越大,第一电离能越大 |
| D.Al的第一电离能比Mg小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】由C、H和与C处于同周期的X、Y四种元素组成的穴醚的键线式如图,该结构中除H外其余原子均满足8电子稳定结构,其空腔直径大约为260~320 pm,可以适配直径与之相近的碱金属离子从而实现离子识别。下列说法正确的是
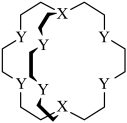
| 离子 | 直径/pm |
 | 204 |
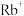 | 304 |
| A.第一电离能:X>Y |
| B.简单氢化物的沸点:X>Y |
| C.键角:C-Y-C>C-X-C |
D.该穴醚可与 通过配位键形成超分子,对 通过配位键形成超分子,对 进行识别 进行识别 |
您最近一年使用:0次
【推荐1】现有四种元素基态原子的电子排布式如下。则下列有关比较中不正确的是
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
①1s22s22p5②1s22s22p3③1s22s22p63s23p4④1s22s22p63s23p3
| A.电负性:①>②>③>④ |
| B.第一电离能:①>②>③>④ |
| C.原子半径:④>③>②>① |
| D.②、③的简单氢化物,中心原子均为sp3杂化,且均为极性分子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:元素的电负性和元素的化合价一样,也是元素的一种基本性质;两成键元素间电负性差值大于1.7时,通常形成离子键,两成键元素间电负性差值小于1.7时,通常形成共价键。下表给出了14种元素的电负性,则下列说法错误的是
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
| A.随着原子序数递增,元素的电负性呈周期性变化 |
| B.元素电负性越大,其非金属性越强 |
| C.根据电负性数据可知Mg3N2中含有离子键 |
| D.BeCl2含金属元素铍,故属于离子化合物 |
您最近一年使用:0次

 制备无水
制备无水 。下列说法正确的是
。下列说法正确的是 为非极性分子
为非极性分子 的电子式为
的电子式为