以某冶金工业产生的废渣(含Cr2O3、SiO2及少量的Al2O3)为原料,根据下列流程可制备K2Cr2O7。
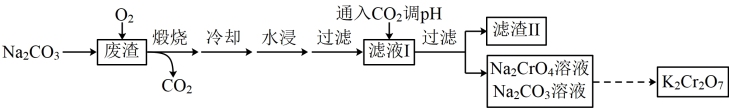
下列说法正确的是

下列说法正确的是
| A.煅烧时没有发生氧化还原反应 |
| B.滤渣Ⅱ中主要成分是Al(OH)3 |
| C.可循环使用的物质是CO2和Na2CO3 |
| D.由Na2CrO4转化为K2Cr2O7的过程中需加入KOH |
2021·湖南·模拟预测 查看更多[13]
巩固训练7江苏省苏州市重点中学2022-2023学年高三上学期10月月考化学试题江苏省南京师范大学附属中学2021-2022学年高三下学期开学考试化学试题 (已下线)专题14 无机综合运用(选择题)-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题06 金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)考向06 钠及其重要化合物-备战2022年高考化学一轮复习考点微专题(已下线)难点1 化工流程微设计-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)押山东卷第09题 化工生产流程选择题-备战2021年高考化学临考题号押题(山东卷)(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)山东省济南市平阴县第一中学2021届高三下学期3月月考化学试题(已下线)热点5 常见元素及其化合物的性质与相互转化-2021年高考化学专练【热点·重点·难点】(新高考)山东省聊城市第一中学2021届高三下学期开学模拟考试化学试题湖南省2021年普通高中学业水平选择考适应性测试化学试题
更新时间:2021-03-04 18:04:29
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】用铝土矿生产 过程中,容易形成一种叫做“赤泥”的固体废弃物,现设计从赤泥中(含
过程中,容易形成一种叫做“赤泥”的固体废弃物,现设计从赤泥中(含 、
、 、
、 )提取镓(Ga)的工艺如图所示,下列说法错误的是
)提取镓(Ga)的工艺如图所示,下列说法错误的是
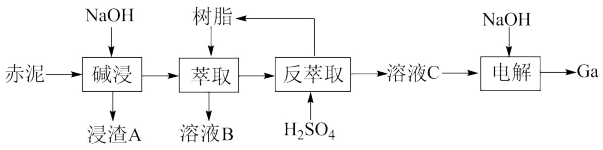
已知: 与
与 性质相似,能与NaOH反应生成可溶性盐
性质相似,能与NaOH反应生成可溶性盐 。
。
 过程中,容易形成一种叫做“赤泥”的固体废弃物,现设计从赤泥中(含
过程中,容易形成一种叫做“赤泥”的固体废弃物,现设计从赤泥中(含 、
、 、
、 )提取镓(Ga)的工艺如图所示,下列说法错误的是
)提取镓(Ga)的工艺如图所示,下列说法错误的是
已知:
 与
与 性质相似,能与NaOH反应生成可溶性盐
性质相似,能与NaOH反应生成可溶性盐 。
。A.浸渣A的主要成分是 |
B.溶液B中含有的阳离子主要有 、 、 |
| C.通过萃取、反萃取的操作可实现Ga元素的富集 |
D.电解过程中阴极的电极反应方程式为 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
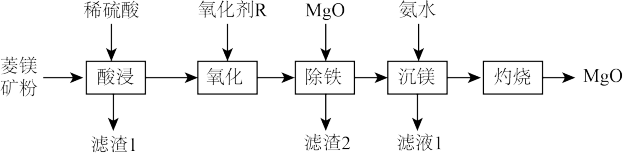
【推荐2】以菱镁矿(主要成分为 ,含少量
,含少量 、
、 等)为原料制备耐火材料MgO的流程如图所示。下列说法错误的是
等)为原料制备耐火材料MgO的流程如图所示。下列说法错误的是
 ,含少量
,含少量 、
、 等)为原料制备耐火材料MgO的流程如图所示。下列说法错误的是
等)为原料制备耐火材料MgO的流程如图所示。下列说法错误的是
| A.滤渣2可以用于制备铁红 | B.在实验室中“灼烧”可在蒸发皿中进行 |
| C.氧化剂R可以是双氧水或氧气 | D.滤液1中的主要成分含有 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)制备铝的某种化合物的工艺流程如下,下列有关说法不正确的是( )
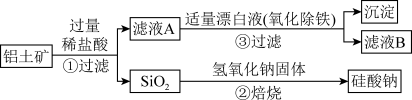

| A.向滤液A中加入KSCN溶液,溶液一定会变红 |
B. 的离子反应方程式为 的离子反应方程式为 |
C. 漂白液的目的是氧化除铁,该过程中涉及的氧化还原反应为 漂白液的目的是氧化除铁,该过程中涉及的氧化还原反应为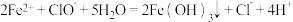 |
D. 中漂白液要适量,若过量则可能产生有毒的气体氯气 中漂白液要适量,若过量则可能产生有毒的气体氯气 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】对废催化剂进行回收可有效利用金属资源,某含银废催化剂主要含Ag、 (
( 为载体,不溶于硝酸)及少量MgO、
为载体,不溶于硝酸)及少量MgO、 、
、 、
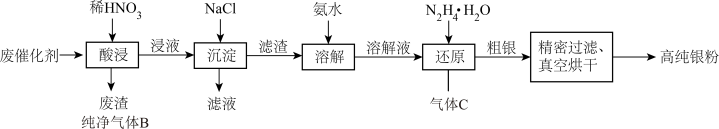
、 等,一种回收制备高纯银粉工艺的部分流程如图:下列说法正确的是
等,一种回收制备高纯银粉工艺的部分流程如图:下列说法正确的是
 (
( 为载体,不溶于硝酸)及少量MgO、
为载体,不溶于硝酸)及少量MgO、 、
、 、
、 等,一种回收制备高纯银粉工艺的部分流程如图:下列说法正确的是
等,一种回收制备高纯银粉工艺的部分流程如图:下列说法正确的是
A.废渣只含 |
| B.气体B可以通入NaOH溶液除去 |
| C.溶解过程的氨水可以换成氢氧化钠溶液 |
| D.“还原”过程中生成无毒气体,B与C的物质的量的理论比值为4∶3 |
您最近半年使用:0次
单选题
|
较难
(0.4)
真题
【推荐2】一种以锰尘(主要成分为 ,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯
,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯 的清洁生产新工艺流程如下:
的清洁生产新工艺流程如下:
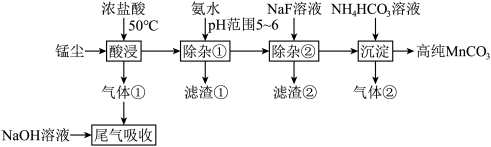
已知:室温下相关物质的 如下表。
如下表。
下列说法错误的是
 ,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯
,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯 的清洁生产新工艺流程如下:
的清洁生产新工艺流程如下:
已知:室温下相关物质的
 如下表。
如下表。 |  |  |  |  |  |  |  |
 |  |  | 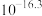 |  |  | 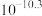 | 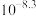 |
| A.酸浸工序中产生的气体①为氯气 |
B.滤渣①主要成分为 和 和 |
C.除杂②工序中逐渐加入 溶液时,若 溶液时,若 浓度接近,则 浓度接近,则 先析出 先析出 |
D.沉淀工序中发生反应的离子方程式为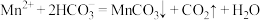 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】银铜合金广泛应用于航空工业。从银铜合金的切割废料中回收银和制备CuAlO2的流程
如下。
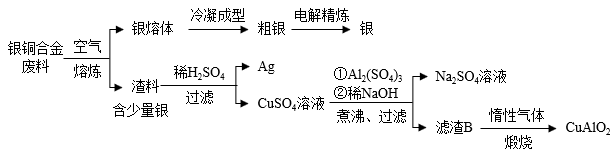
已知:Al(OH) 3和Cu(OH) 2开始分解的温度分别为450℃和 80℃。 下列说法错误的是
如下。

已知:Al(OH) 3和Cu(OH) 2开始分解的温度分别为450℃和 80℃。 下列说法错误的是
| A.电解精炼时,粗银做阳极,纯银做阴极 |
| B.为提高原料利用率,流程中应加过量的稀NaOH |
C.滤渣B煅烧时发生的反应为 4CuO+4Al(OH)3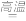 4CuA1O2+ O2↑+6H2O 4CuA1O2+ O2↑+6H2O |
| D.若用 1.0 kg 银铜合金(铜的质量分数为64%) 最多可生成 10.0mol CuA1O2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列关于下列元素及其化合物的说法正确的是
| A.将等物质的量的①Na②Na2O③Na2O2④NaOH⑤Na2CO3露置于空气中,最后质量变化由小到大的顺序⑤<④<③<①<② |
| B.Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到 |
| C.将澄清石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者无明显现象 |
| D.在反应4FeCl2+4 Na2O2+6H2O=4 Fe(OH)3+O2↑+8NaCl中,做氧化剂的过氧化钠和做还原剂的过氧化钠物质的量之比为1:3 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用NaClO氧化尿素[CO(NH2)2]制备N2H4·H2O(水合肼)的实验流程如图所示:
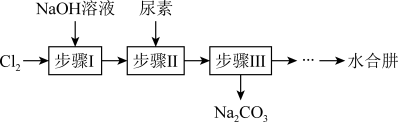
已知:①氯气与烧碱溶液的反应是放热反应;②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。下列说法错误的是

已知:①氯气与烧碱溶液的反应是放热反应;②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。下列说法错误的是
| A.步骤I中为避免温度过高,可采用冰水浴 |
| B.步骤I制备NaClO溶液时,若溶液中NaClO与副产物NaClO3的物质的量之比为5:1,则参与反应的氧化剂与还原剂的物质的量之比为5:3 |
| C.步骤II中可将NaClO碱性溶液逐滴滴入尿素水溶液中 |
D.生成水合肼反应的离子方程式为ClO-+CO(NH2)2+2H+=Cl-+N2H4·H2O+ |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】K2Cr2O7是重要氧化剂。工业制备重铬酸钾的原理是:将铬铁矿与纯碱按一定比例混合在高温下煅烧:①4Fe(CrO2)2+7O2+8Na2CO3 2Fe2O3+8Na2CrO4+8CO2;②2Na2CrO4+H2SO4=Na2Cr2O7+H2O+Na2SO4;③Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl。下列有关说法正确的是
2Fe2O3+8Na2CrO4+8CO2;②2Na2CrO4+H2SO4=Na2Cr2O7+H2O+Na2SO4;③Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl。下列有关说法正确的是
 2Fe2O3+8Na2CrO4+8CO2;②2Na2CrO4+H2SO4=Na2Cr2O7+H2O+Na2SO4;③Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl。下列有关说法正确的是
2Fe2O3+8Na2CrO4+8CO2;②2Na2CrO4+H2SO4=Na2Cr2O7+H2O+Na2SO4;③Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl。下列有关说法正确的是| A.反应①中Na2CO3作还原剂 |
| B.反应①中每生成80gFe2O3转移7mol电子 |
| C.反应②中,可以用浓盐酸替代硫酸 |
| D.反应③符合溶解度较小物质转化成溶解度较大的物质 |
您最近半年使用:0次
【推荐1】一种以铝土矿(含Al2O3、Ga2O3)为原料制备金属稼(Ga)的工艺流程如图。
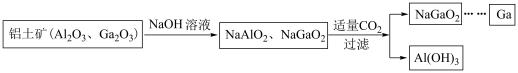
下列说法正确的是
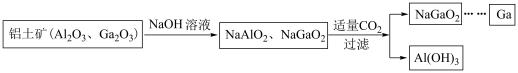
下列说法正确的是
| A.Ga2O3是碱性氧化物 |
| B.由流程可知,酸性:Al(OH)3>Ga(OH)3 |
| C.基态镓原子的简化电子排布式为:[Ar]4s24p1 |
D.通入适量CO2时反应的离子方程式: |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】锌冶炼过程中会产生大量的铅浮渣,其主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。利用铅浮渣生产硫酸铅的流程如下。下列说法不正确的是
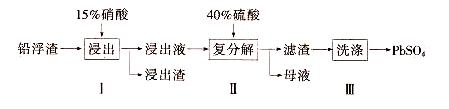

A.步骤Ⅰ中反应的离子方程式是:Pb+4H++2NO =Pb2++2NO↑+2H2O =Pb2++2NO↑+2H2O |
| B.复分解反应的方程式是:Pb(NO3)2+H2SO4= PbSO4↓+2HNO3 |
| C.为保证产品纯度,需控制硝酸的量以为防止Ag被溶解 |
| D.步骤Ⅱ得到的粗产品PbSO4 含有少量CaSO4杂质,还需用Pb(NO3)2溶液多次洗涤 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
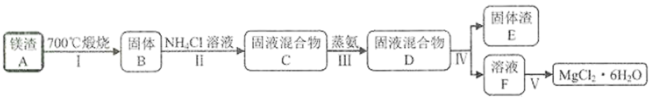
【推荐3】某兴趣小组在定量分析了镁渣[含有 、
、 、
、 、
、 、
、 和
和 ]中Mg含量的基础上,按如流程制备六水合氯化镁(
]中Mg含量的基础上,按如流程制备六水合氯化镁( )。
)。
相关信息如下:
①700℃只发生 和
和 的分解反应。
的分解反应。
② 溶液仅与体系中的MgO反应,且反应程度不大。
溶液仅与体系中的MgO反应,且反应程度不大。
③“蒸氨”是将氨从固液混合物中蒸出来,且须控制合适的蒸出量。
下列说法错误的是
 、
、 、
、 、
、 、
、 和
和 ]中Mg含量的基础上,按如流程制备六水合氯化镁(
]中Mg含量的基础上,按如流程制备六水合氯化镁( )。
)。相关信息如下:
①700℃只发生
 和
和 的分解反应。
的分解反应。②
 溶液仅与体系中的MgO反应,且反应程度不大。
溶液仅与体系中的MgO反应,且反应程度不大。③“蒸氨”是将氨从固液混合物中蒸出来,且须控制合适的蒸出量。
下列说法错误的是

A.步骤Ⅱ,反应的方程式是: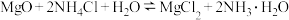 |
| B.步骤Ⅲ,可以将固液混合物C先过滤,再蒸氨 |
| C.步骤Ⅲ,蒸氨促进平衡正向移动,提高MgO的溶解量 |
| D.溶液F经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。取少量产品溶于水后发现溶液呈碱性,可能是结晶时过度蒸发导致氯化镁水解,部分生成碱式氯化镁 |
您最近半年使用:0次



