实验室用乳酸与异戊醇反应制备乳酸异戊酯,有关数据和装置示意图如下: +
+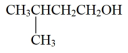
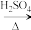
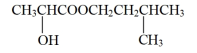 +H2O
+H2O
实验步骤:
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:
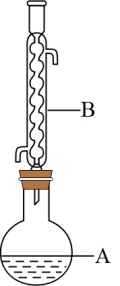
(1)图中A仪器的名称是___________ ,B仪器的作用是___________ 。
(2)在该实验中,A的容积最适合的是___________ (填入正确选项前的字母)。
A.50mL B.100mL C.150mL
(3)用饱和碳酸钠溶液洗涤的主要目的是___________ ,分离提纯过程中加入无水硫酸镁的目的是___________ 。
(4)在蒸馏纯化过程中,下列说法错误的是___________ 。
A.加热一段时间后发现忘记加瓷片,应该冷却后补加
B.温度计应该插入液面以下
C.冷却水的方向是上进下出,保证冷却水快速流动
D.蒸馏时用到的主要玻璃仪器有:酒精灯、蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶
(5)本实验中加入过量异戊醇的目的是___________ ,本实验的产率是___________ 。
 +
+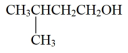
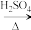
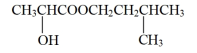 +H2O
+H2O| 相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解度 | |
| 乳酸 | 90 | 1.209 | 122 | 溶 |
| 异戊醇 | 88 | 0.81 | 131 | 微溶 |
| 乳酸异戊酯 | 160 | 0.987 | 202 | 不溶 |
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:

(1)图中A仪器的名称是
(2)在该实验中,A的容积最适合的是
A.50mL B.100mL C.150mL
(3)用饱和碳酸钠溶液洗涤的主要目的是
(4)在蒸馏纯化过程中,下列说法错误的是
A.加热一段时间后发现忘记加瓷片,应该冷却后补加
B.温度计应该插入液面以下
C.冷却水的方向是上进下出,保证冷却水快速流动
D.蒸馏时用到的主要玻璃仪器有:酒精灯、蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶
(5)本实验中加入过量异戊醇的目的是
更新时间:2021/03/14 18:19:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】有“退热冰”之称的乙酰苯胺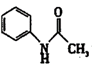 具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等。乙酰苯胺可通过苯胺(
具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等。乙酰苯胺可通过苯胺(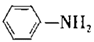 )和乙酸反应(该反应是放热反应)制得。
)和乙酸反应(该反应是放热反应)制得。
已知:
1.苯胺在空气中易被氧化。
2.可能用到的有关性质如下:
Ⅰ.制备乙酰苯胺的实验步骤如下:
步骤1:在制备装置加入9.2mL苯胺、17.4mL冰醋酸、0.1g锌粉及少量水。
步骤2:小火加热回流1h。
步骤3:待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250mL冷水的烧杯中,乙酰苯胺晶体析出。冷却,减压过滤(抽滤),用滤液洗涤晶体2~3次。
请回答下列问题:
(1)写出制备乙酰苯胺的化学方程式___ 。
(2)将三种试剂混合时,最后加入的试剂是___ ,这样做的原因是:___ 。
(3)步骤2:小火加热回流1h,装置如图所示。请回答下列问题:
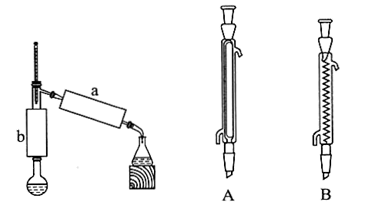
①b处使用的仪器为___ (填“A”或“B”),该仪器的名称是___ 。
②得到的粗乙酰苯胺固体,为使其更加纯净,还需要进行的分离方法是___ 。
Ⅱ.实验小组通过控制反应温度,测得不同温度下产品的平衡产率如图所示:

(4)从图中可知,反应体系温度在100℃-105℃时,乙酰苯胺的产率上升的原因可能是:___ 。
(5)①该实验最终得纯品10.8g,则乙酰苯胺的产率是___ 。(精确到小数点后1位)
②导致实际值低于理论值的原因可能是___ (填字母标号)。
A.没有等充分冷却就开始过滤
B.抽滤后没有把滤液合并在一起
C.乙酰苯胺中的乙酸未除干净
 具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等。乙酰苯胺可通过苯胺(
具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺在工业上可用作橡胶硫化促进剂、纤维酯涂料的稳定剂、过氧化氢的稳定剂等。乙酰苯胺可通过苯胺(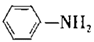 )和乙酸反应(该反应是放热反应)制得。
)和乙酸反应(该反应是放热反应)制得。已知:
1.苯胺在空气中易被氧化。
2.可能用到的有关性质如下:
| 名称 | 相对分子质量 | 性状 | 密度/g∙cm3 | 熔点/℃ | 沸点/℃ | 溶解度 | |
| g/100g水 | g/100g乙醇 | ||||||
| 苯胺 | 93 | 棕黄色油状液体 | 1.02 | -6.3 | 184 | 微溶 | ∞ |
| 冰醋酸 | 60 | 无色透明液体 | 1.05 | 16.6 | 117.9 | ∞ | ∞ |
| 乙酰苯胺 | 135 | 无色片状晶体 | 1.21 | 155~156 | 280~290 | 温度高,溶解度大 | 较水中大 |
步骤1:在制备装置加入9.2mL苯胺、17.4mL冰醋酸、0.1g锌粉及少量水。
步骤2:小火加热回流1h。
步骤3:待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250mL冷水的烧杯中,乙酰苯胺晶体析出。冷却,减压过滤(抽滤),用滤液洗涤晶体2~3次。
请回答下列问题:
(1)写出制备乙酰苯胺的化学方程式
(2)将三种试剂混合时,最后加入的试剂是
(3)步骤2:小火加热回流1h,装置如图所示。请回答下列问题:

①b处使用的仪器为
②得到的粗乙酰苯胺固体,为使其更加纯净,还需要进行的分离方法是
Ⅱ.实验小组通过控制反应温度,测得不同温度下产品的平衡产率如图所示:

(4)从图中可知,反应体系温度在100℃-105℃时,乙酰苯胺的产率上升的原因可能是:
(5)①该实验最终得纯品10.8g,则乙酰苯胺的产率是
②导致实际值低于理论值的原因可能是
A.没有等充分冷却就开始过滤
B.抽滤后没有把滤液合并在一起
C.乙酰苯胺中的乙酸未除干净
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
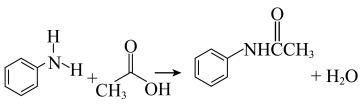
【推荐2】酰胺常被用作溶剂和化工原料,也用于合成农药、医药等。实验室可以通过下列反应制备乙酰苯胺:
有如下实验步骤:
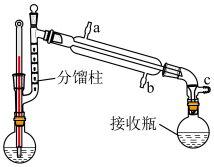
Ⅰ、用25mL圆底烧瓶组装成如图所示的分馏装置。在烧瓶中加入约4.5mL(50mmol)新制的苯胺(苯胺易被氧化变质)、7.5mL的冰乙酸和0.05g锌粉,摇匀。
Ⅱ、加热,保持反应液微沸约20min,逐渐升高温度,使反应温度维持在100~105℃,反应大约1h.然后将温度升高至110℃,当温度出现较大波动时,停止加热。
Ⅲ、趁热将反应液倒入盛有100mL冷水的烧杯中,有白色沉淀析出。稍加搅拌冷却,抽滤,洗涤固体,抽干,在红外灯下烘干。得到含有少量苯胺的粗产品,提纯后得产品4.59g。
回答下列问题:
(1)接液管的c出口的作用是___________ 。
(2)步骤①中,加入锌粉的主要目的是___________ 。
(3)写出乙酰苯胺与NaOH反应的化学方程式___________ 。
(4)步骤②最后阶段,将温度升高至110℃的主要目的是为了蒸馏出更多的___________ (填分子式)。分馏柱可以使部分蒸发出的物质回流到反应瓶中,该实验使用分馏柱的目的是___________
(5)粗产品提纯的最佳方法是___________ 。
(6)已知酰胺中N原子的未共用电子对与羰基的Π电子形成共轭体系,使N原子上的电子云密度降低。相同条件下,下列物质的碱性由强到弱的顺序为___________ 。
① ②甲胺 ③乙酰苯胺
②甲胺 ③乙酰苯胺
(7)产品的产率为___________ %(用苯胺计算,精确至0.1%)。
| 物质 | 性状 | 沸点/℃ | 溶解性 |
| 冰乙酸 | 无色液体 | 118 | 与水、乙醇、苯等互溶 |
| 苯胺 | 浅黄色液体 | 184 | 微溶于水、溶于乙醇、乙酸、苯等 |
| 乙酰苯胺 | 白色固体 | 304 | 微溶于水、溶于热水、乙醇、乙酸、苯等 |
Ⅰ、用25mL圆底烧瓶组装成如图所示的分馏装置。在烧瓶中加入约4.5mL(50mmol)新制的苯胺(苯胺易被氧化变质)、7.5mL的冰乙酸和0.05g锌粉,摇匀。
Ⅱ、加热,保持反应液微沸约20min,逐渐升高温度,使反应温度维持在100~105℃,反应大约1h.然后将温度升高至110℃,当温度出现较大波动时,停止加热。
Ⅲ、趁热将反应液倒入盛有100mL冷水的烧杯中,有白色沉淀析出。稍加搅拌冷却,抽滤,洗涤固体,抽干,在红外灯下烘干。得到含有少量苯胺的粗产品,提纯后得产品4.59g。
回答下列问题:
(1)接液管的c出口的作用是
(2)步骤①中,加入锌粉的主要目的是
(3)写出乙酰苯胺与NaOH反应的化学方程式
(4)步骤②最后阶段,将温度升高至110℃的主要目的是为了蒸馏出更多的
(5)粗产品提纯的最佳方法是
(6)已知酰胺中N原子的未共用电子对与羰基的Π电子形成共轭体系,使N原子上的电子云密度降低。相同条件下,下列物质的碱性由强到弱的顺序为
①
 ②甲胺 ③乙酰苯胺
②甲胺 ③乙酰苯胺(7)产品的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】我国科学家屠呦呦因青蒿素获得诺贝尔奖,某实验小组拟提取青蒿素并进行测定。
【资料】青蒿素为无色针状晶体,熔点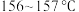 ,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
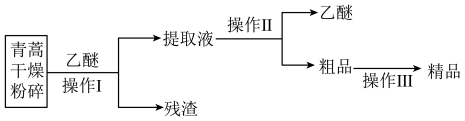
Ⅰ.实验室用乙醚提取青蒿素的工艺流程如下图:___________ ,在操作Ⅰ前要对青蒿进行粉碎,其目的是___________ 。
(2)操作Ⅱ的名称是___________ 。
(3)操作Ⅲ进行的是重结晶,其操作步骤为:________ 。
加热溶解→___________→___________→过滤、洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,为确定其化学式,又进行了如下实验:
①连接装置,检查装置的气密性。
②称量E、F中仪器及药品的质量
③取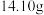 青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧
青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质重
(4)装置E、F中装入的药品分别为___________ 、___________ 。
(5)若使用上述方法会产生较大的实验误差,你的改进方法是___________ 。
(6)实验装置改进后,测得:实验前后装置E、F的质量差值分别为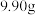 、
、 通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式___________ 。
【资料】青蒿素为无色针状晶体,熔点
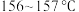 ,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。Ⅰ.实验室用乙醚提取青蒿素的工艺流程如下图:
(2)操作Ⅱ的名称是
(3)操作Ⅲ进行的是重结晶,其操作步骤为:
加热溶解→___________→___________→过滤、洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,为确定其化学式,又进行了如下实验:
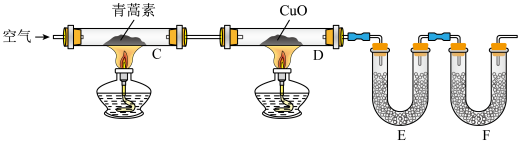
①连接装置,检查装置的气密性。
②称量E、F中仪器及药品的质量
③取
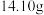 青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧
青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质重
(4)装置E、F中装入的药品分别为
(5)若使用上述方法会产生较大的实验误差,你的改进方法是
(6)实验装置改进后,测得:实验前后装置E、F的质量差值分别为
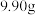 、
、 通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室可用如图装置制取乙酸乙酯。

①在试管a中加好相关试剂后,还需要加入2—3块的碎瓷片,其作用是___________ 。
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的___________ (填“上”或“下”)层,试管b中的导管口应在液面上方而不伸入到液面以下,其原因是___________ 。
③用示踪原子法可确定某些化学反应的机理,写出用CH3CH218OH和CH3COOH反应制取乙酸乙酯的化学方程式___________ 。

①在试管a中加好相关试剂后,还需要加入2—3块的碎瓷片,其作用是
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的
③用示踪原子法可确定某些化学反应的机理,写出用CH3CH218OH和CH3COOH反应制取乙酸乙酯的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】利用淀粉可实现下列转化,请回答下列问题:
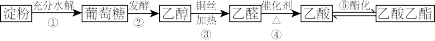
(1)某化学课外活动小组为探究反应③并验证产物,设计甲、乙两套装置图中的夹持仪器均未画出,“△”表示酒精灯热源,每套装置又可划分为Ⅰ、Ⅱ、Ⅲ三部分。仪器中盛放的试剂a为无水乙醇(沸点:78℃);b为铜丝;c为无水硫酸铜;d为新制氢氧化铜悬浊液(已知乙醛与新制氢氧化铜悬浊液加热有明显现象)。
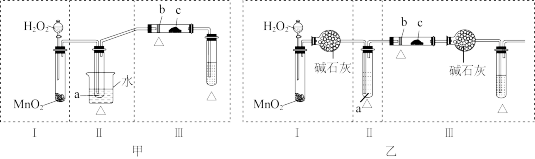
①对比两种方案,简述甲方案的优点:_______ 。
②集中两种方案的优点,组成一套完善合理的方案。按照气流从左至右的顺序为_______ (填写方式如:甲Ⅰ、乙Ⅱ等)。
(2)改进方案后进行该实验。实验过程中通入氧气的速率与反应体系的温度关系曲线如图所示,鼓气速率过快,反应体系温度反而下降的原因是_______ ,为解决该问题可采取的操作是_______ 。

(3)如果用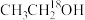 实现反应⑤,写出反应的化学方程式:
实现反应⑤,写出反应的化学方程式:_______ 。
实验室欲从乙酸乙酯、乙酸、乙醇的混合物得到乙酸乙酯,分离流程如下:
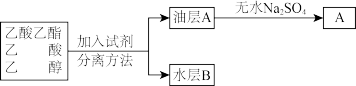
(4)则加入的试剂是_______ ,无水 的作用是
的作用是_______ 。
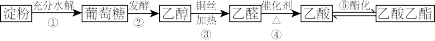
(1)某化学课外活动小组为探究反应③并验证产物,设计甲、乙两套装置图中的夹持仪器均未画出,“△”表示酒精灯热源,每套装置又可划分为Ⅰ、Ⅱ、Ⅲ三部分。仪器中盛放的试剂a为无水乙醇(沸点:78℃);b为铜丝;c为无水硫酸铜;d为新制氢氧化铜悬浊液(已知乙醛与新制氢氧化铜悬浊液加热有明显现象)。

①对比两种方案,简述甲方案的优点:
②集中两种方案的优点,组成一套完善合理的方案。按照气流从左至右的顺序为
(2)改进方案后进行该实验。实验过程中通入氧气的速率与反应体系的温度关系曲线如图所示,鼓气速率过快,反应体系温度反而下降的原因是

(3)如果用
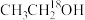 实现反应⑤,写出反应的化学方程式:
实现反应⑤,写出反应的化学方程式:实验室欲从乙酸乙酯、乙酸、乙醇的混合物得到乙酸乙酯,分离流程如下:

(4)则加入的试剂是
 的作用是
的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题。
(1)在烧瓶中除了加入乙醇,浓硫酸和乙酸外,还应放入___________ ,目的是___________________ 。
(2)反应中加入过量的乙醇,目的是_______________ 。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是_____________________________ 。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是分离操作步骤流程:
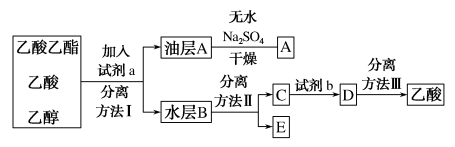
则试剂a是___________ ,分离方法Ⅰ是___________ ,试剂b是___________ ,分离方法Ⅲ是_____________________ 。
(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都是先加 溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
甲得到了显酸性的酯的混合物,乙得到了大量水溶性的物质,丙同学分析了上述实验目标产物后认为上述实验没有成功。试解答下列问题:
①甲实验失败的原因是______________________ ;
②乙实验失败的原因是______________________ 。
(6)若原料为 和
和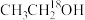 ,则乙酸乙酯中
,则乙酸乙酯中___________  (填含或不含)。
(填含或不含)。
请回答下列问题。
(1)在烧瓶中除了加入乙醇,浓硫酸和乙酸外,还应放入
(2)反应中加入过量的乙醇,目的是
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是分离操作步骤流程:

则试剂a是
(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都是先加
 溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:
溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人实验结果如下:甲得到了显酸性的酯的混合物,乙得到了大量水溶性的物质,丙同学分析了上述实验目标产物后认为上述实验没有成功。试解答下列问题:
①甲实验失败的原因是
②乙实验失败的原因是
(6)若原料为
 和
和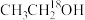 ,则乙酸乙酯中
,则乙酸乙酯中 (填含或不含)。
(填含或不含)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
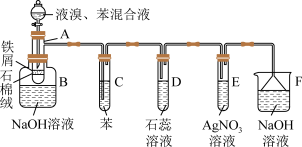
【推荐1】下图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉。
(1)向反应容器A中逐滴加入溴和苯,发生反应。写出A中所发生反应的化学方程式:___________________________________________________________ 。
(2)试管观察D中看到的现象为____________________________________ 。
(3)在上述整套装置中,具有防倒吸作用的仪器有____________ (填字母)。
(1)向反应容器A中逐滴加入溴和苯,发生反应。写出A中所发生反应的化学方程式:
(2)试管观察D中看到的现象为
(3)在上述整套装置中,具有防倒吸作用的仪器有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】黄酮类化合物具有广泛的药理作用,如抗氧化、降血压、抗肿瘤等,其中2-羟基查尔酮的合成反应如下:
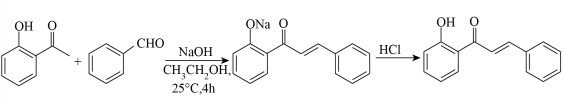
实验装置如图:
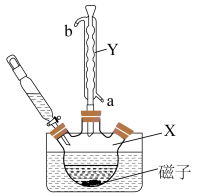
合成实验步骤为:
步骤I:在仪器X中用移液管依次加入1.02mL苯甲醛(10mmol),1.20mL2-羟基苯乙酮(10mmol),量筒量取30.0mL乙醇加入,搅拌。
步骤Ⅱ:量取10.0mL10%的氢氧化钠(25mmol)溶液加到滴液漏斗中,缓慢滴加到仪器X中,保持25℃反应4h。
步骤Ⅲ:反应结束后,把X中混合物倒入盛有冰盐水的烧杯中,搅拌下加入10%的盐酸溶液,调节pH为5-6。
步骤Ⅳ:静置,待固体完全析出后,抽滤,用冰水洗涤。
步骤V:接着用无水乙醇洗涤,重复三次,烘干,称量,得产物2-羟基查尔酮为黄色固体,称得质量约为2.05g。
(1)装置图中仪器X的名称是___________ ;装置Y中冷却水从___________ (填“a”或“b”)口通入。
(2)把X中混合物倒入盛有冰盐水的烧杯中的目的是___________
(3)写出步骤Ⅲ中主要化学反应方程式___________ 。
(4)设计实验证明步骤Ⅳ中所得固体已洗涤干净___________ 。
(5)步骤V中用无水乙醇洗涤产品的目的是___________ 。
(6)已知2-羟基查尔酮的相对分子质量为224,本实验中产品的产率为___________ 。(保留三位有效数字)

实验装置如图:

合成实验步骤为:
步骤I:在仪器X中用移液管依次加入1.02mL苯甲醛(10mmol),1.20mL2-羟基苯乙酮(10mmol),量筒量取30.0mL乙醇加入,搅拌。
步骤Ⅱ:量取10.0mL10%的氢氧化钠(25mmol)溶液加到滴液漏斗中,缓慢滴加到仪器X中,保持25℃反应4h。
步骤Ⅲ:反应结束后,把X中混合物倒入盛有冰盐水的烧杯中,搅拌下加入10%的盐酸溶液,调节pH为5-6。
步骤Ⅳ:静置,待固体完全析出后,抽滤,用冰水洗涤。
步骤V:接着用无水乙醇洗涤,重复三次,烘干,称量,得产物2-羟基查尔酮为黄色固体,称得质量约为2.05g。
(1)装置图中仪器X的名称是
(2)把X中混合物倒入盛有冰盐水的烧杯中的目的是
(3)写出步骤Ⅲ中主要化学反应方程式
(4)设计实验证明步骤Ⅳ中所得固体已洗涤干净
(5)步骤V中用无水乙醇洗涤产品的目的是
(6)已知2-羟基查尔酮的相对分子质量为224,本实验中产品的产率为
您最近一年使用:0次
【推荐3】Ⅰ.以乙烯为原料合成化合物C的流程如图所示:

已知: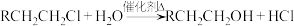
回答下列问题:
(1)写出C的结构简式:_____ 。
(2)乙醇分子中的官能团名称是_____ ,写出一种可鉴别乙醇和乙酸的化学试剂:_____ 。
(3)在①、②、③、④的反应中,属于取代反应的是_____ 。
(4)写出由乙醇与氧气反应生成B的化学方程式_____ 。
(5)物质E是乙醇的同系物,其分子式为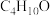 ,E同类的同分异构体共有
,E同类的同分异构体共有_____ 种(包括E)。
Ⅱ.实验室制取丙酸甲酯的主要步骤如下:
①如图,在甲试管中依次加入 甲醇、
甲醇、 浓硫酸、
浓硫酸、 丙酸。
丙酸。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热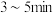 。
。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,用力振荡,然后静置待分层。
④分离出丙酸甲酯层,洗涤、干燥。
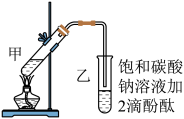
(6)写出丙酸与甲醇在浓硫酸加热条件下反应的化学方程式_____ 。
(7)上述实验中饱和碳酸钠的作用是_____(填字母)。
(8)欲将乙试管中的物质分离开以得到丙酸甲酯,必须使用的主要玻璃仪器有_____ 。

已知:
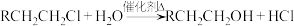
回答下列问题:
(1)写出C的结构简式:
(2)乙醇分子中的官能团名称是
(3)在①、②、③、④的反应中,属于取代反应的是
(4)写出由乙醇与氧气反应生成B的化学方程式
(5)物质E是乙醇的同系物,其分子式为
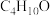 ,E同类的同分异构体共有
,E同类的同分异构体共有Ⅱ.实验室制取丙酸甲酯的主要步骤如下:
①如图,在甲试管中依次加入
 甲醇、
甲醇、 浓硫酸、
浓硫酸、 丙酸。
丙酸。②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热
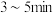 。
。③待试管乙收集到一定量产物后停止加热,撤出试管乙,用力振荡,然后静置待分层。
④分离出丙酸甲酯层,洗涤、干燥。

(6)写出丙酸与甲醇在浓硫酸加热条件下反应的化学方程式
(7)上述实验中饱和碳酸钠的作用是_____(填字母)。
| A.中和甲醇和丙酸 |
| B.与挥发出来的丙酸反应并溶解挥发出的部分甲醇 |
| C.丙酸甲酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出 |
| D.加速酯的生成,提高其产率 |
您最近一年使用:0次



