t ℃时,在一密闭容器中充入2molA和3 mol B,发生如下化学反应:aA(g)+B(g)⇌C(g)+D(g)。已知,平衡时,ca(A)·c(B)= c(C)·c(D),然后在温度不变的情况下,扩大容器容积至原来10 倍,结果A的百分含量始终未有改变,则下列说法错误的是
| A.a=1 |
| B.B的转化率为24% |
| C.平衡常数K=1 |
| D.温度不变的情况下,扩大容器容积,平衡不移动 |
更新时间:2021/07/12 23:07:30
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方法、操作均正确,且能达到实验目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 测定中和反应反应热 | 用简易量热器测量浓硫酸与NaOH溶液反应前后的温度 |
| B | 判断反应后 是否沉淀完全 是否沉淀完全 | 将 溶液与NaCl溶液混合,反应后静置,向上层清液中再加入1滴NaCl溶液 溶液与NaCl溶液混合,反应后静置,向上层清液中再加入1滴NaCl溶液 |
| C | 探究压强对化学反应平衡移动的影响 | 容器中反应 达平衡时,将容器压缩为原体积的 达平衡时,将容器压缩为原体积的 ,观察颜色变化 ,观察颜色变化 |
| D | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的盐酸,分别加入等体积、等浓度的NaOH溶液,对比现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用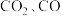 与
与 反应合成甲醇,是目前推动“碳达峰、碳中和”的新路径:①
反应合成甲醇,是目前推动“碳达峰、碳中和”的新路径:① ,②
,② 。在
。在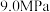 下,分别按一定投料比在密闭容器反应相同时间,测得甲醇的生成速率和温度的关系如图。下列说法正确的是
下,分别按一定投料比在密闭容器反应相同时间,测得甲醇的生成速率和温度的关系如图。下列说法正确的是
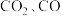 与
与 反应合成甲醇,是目前推动“碳达峰、碳中和”的新路径:①
反应合成甲醇,是目前推动“碳达峰、碳中和”的新路径:① ,②
,② 。在
。在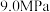 下,分别按一定投料比在密闭容器反应相同时间,测得甲醇的生成速率和温度的关系如图。下列说法正确的是
下,分别按一定投料比在密闭容器反应相同时间,测得甲醇的生成速率和温度的关系如图。下列说法正确的是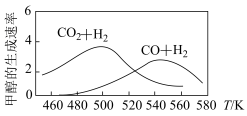
| A.其他条件不变,温度升高,甲醇的生成速率加快 |
| B.其他条件不变,压缩容器体积,甲醇的产率先增大后减小 |
| C.选用更高效的催化剂,可增加甲醇的生成速率和平衡转化率 |
D.反应②低于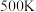 时很难发生可能是因为催化剂未达最适温度 时很难发生可能是因为催化剂未达最适温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】将1molCO和2molH2充入一容积为1L密闭容器中,分别在250℃、T℃发生反应: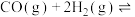

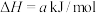 ,根据图示判断,下列正确的是
,根据图示判断,下列正确的是

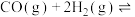

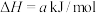 ,根据图示判断,下列正确的是
,根据图示判断,下列正确的是
A. , , |
B.250℃时,0~10min内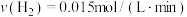 |
| C.CO的平衡转化率在250℃时比T℃时大 |
D.250℃时,起始时改为向容器中充入2molCO和4molH2,恒温达平衡后, 的物质的量大于0.30mol 的物质的量大于0.30mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,反应: 的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
 的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是| A.升高温度,K增大 |
B.2molSO2和1molO2反应放出热量 |
C.其他条件不变,增大 的量,∆H和K均增大 的量,∆H和K均增大 |
D.相同温度时反应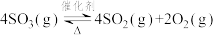 的反应热和化学平衡常数为-2∆H和 的反应热和化学平衡常数为-2∆H和 |
您最近一年使用:0次
【推荐2】某些化学知识用数轴表示能体现出形象直观、简明易记的特点。下列用数轴表示不 合理的是
A.铁和稀硝酸反应: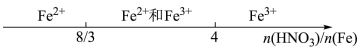 |
B.分散系的分类: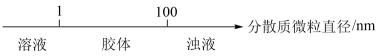 |
C.平衡常数与转化率关系: |
D.氨水与SO2反应后溶液中的铵盐: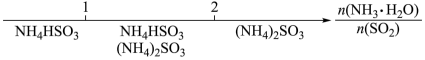 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是

| A.该反应为放热反应 |
| B.催化剂能改变该反应的焓变 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能等于正反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在密闭容器中,保持一定温度进行如下反应:N2(g)+3H2(g)⇌2NH3(g)。其一些实验结果如下表:
则下列关系式中,不正确的是
| 状态 条件 | 起始时各物质的物质的量/mol | 平衡时NH3的物质的量分数 | |||
| 实验编号 | N2 | H2 | NH3 | ||
| 恒压 | ① | 1 | 3 | 0 | a |
| 恒容 | ② | 1 | 3 | 0 | b |
| ③ | 0 | 0 | x | b | |
| ④ | y | 2.25 | z | b | |
| A.x=4 | B.y=0.75 | C.z=0.5 | D.a>b |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】向容积为1.0L的密闭容器中加入X、Y两种物质各0.10 mol,一定温度下下述反应xX+yY  Z中X、Y、Z的物质的量随反应时间的变化曲线如图所示。下列说法中,正确的是
Z中X、Y、Z的物质的量随反应时间的变化曲线如图所示。下列说法中,正确的是

 Z中X、Y、Z的物质的量随反应时间的变化曲线如图所示。下列说法中,正确的是
Z中X、Y、Z的物质的量随反应时间的变化曲线如图所示。下列说法中,正确的是
| A.反应方程式中系数x、y的值分别为3、1 |
| B.该反应达平衡后,增大体系压强或加入催化剂,都可以提高Z的产率 |
| C.若Z为气体,反应开始至2.0 min内,反应平均速率v (Z)为0.01 mol·L-1·min-1 |
| D.反应2.0min后,正、逆反应速率都等于零,故X、Y、Z的物质的量不再随反应时间的变化而改变 |
您最近一年使用:0次

 沉淀。25℃,平衡体系中含
沉淀。25℃,平衡体系中含 微粒的分布系数
微粒的分布系数 [如
[如 ]随
]随 的变化曲线如图所示,
的变化曲线如图所示,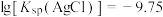 ,下列叙述正确的是
,下列叙述正确的是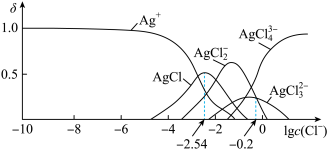
 的溶解度随
的溶解度随 增大而减小
增大而减小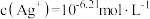
 的平衡常数
的平衡常数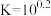
 时,溶液中
时,溶液中


