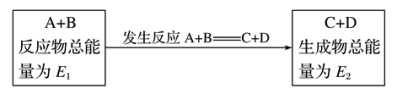
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=________ kJ·mol-1。
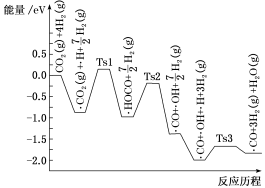
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会_____ (填“放出热量”或“吸收热量”);反应历程中最小能垒(活化能)步骤的化学方程式为____ 。
(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1 167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)⇌CH4(g)+CO(g)的ΔH=________ 。
反应Ⅰ:2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1
反应Ⅱ:NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49 kJ·mol-1
总反应:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ΔH3=-86.98 kJ·mol-1
则反应Ⅰ的ΔH1=
(2)氢气可将CO2还原为甲烷,反应为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)。ShyamKattel等结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面用“·”标注,Ts表示过渡态。物质吸附在催化剂表面,形成过渡态的过程会

(3)已知CO(g)、CH4(g)、CH3CHO(l)的燃烧热分别为283.0 kJ·mol-1、890.31 kJ·mol-1、1 167.9 kJ·mol-1,则乙醛的分解反应CH3CHO(l)⇌CH4(g)+CO(g)的ΔH=
2021高三·全国·专题练习 查看更多[2]
更新时间:2021/08/18 13:15:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】物质都是由微观粒子构成的,这些粒子的结合重组,是构成物质及其物质变化和能量变化的根本原因。
(1)6Li、14C、14N、7Li、23Na、16O这些微粒中,共有_______ 种核素,互为同位素的是_______ 。
(2)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是_______ (填序号),仅离子键被破坏的是_______ (填序号)。
(3)若将反应2Fe3++Cu=2Fe2++Cu2+设计成原电池装置,则负极材料为_______ ,离子导体为_______ ,正极电极反应式是_______ ;若反应过程中有0.2mol电子通过,则电解质溶液的质量变化为_______ 。
(4)从能量的变化角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
则生成1molH2O(g)可以放出热量_______ kJ。
(1)6Li、14C、14N、7Li、23Na、16O这些微粒中,共有
(2)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是
(3)若将反应2Fe3++Cu=2Fe2++Cu2+设计成原电池装置,则负极材料为
(4)从能量的变化角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
| 化学键 | H—H | O=O | H—O |
| 能量(kJ) | 436 | 496 | 463 |
您最近一年使用:0次
【推荐2】1.已知存在下列热化学方程式:
①氢气燃烧H2(g)+ O2(g)= H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)= H2O(g) ΔH1=-241.8 kJ·mol-1
②太阳光分解水制氢气2H2O(l)=2H2(g)+O2(g) ΔH2=571.6 kJ·mol-1
③液态水转化为水蒸气H2O(l)= H2O(g) ΔH3=___ kJ·mol-1
(1)从能量转化角度分析,反应①为_______ 反应。(填“吸热”或“放热”)
(2)反应②中主要能量转化形式为_______ 能转化为_______ 能。
(3)若在反应②中使用催化剂,ΔH2_______ 。(填“增大”“减小”或“不变”)
(4)写出反应③的热化学方程式_______ 。
(5)根据下表内容及你所学知识列举氢气被称为“绿色能源”的原因_______ 。
热值是指某种燃料完全燃烧放出的热量与其质量之比,其单位是kJ/ g (气体)。
①氢气燃烧H2(g)+
 O2(g)= H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)= H2O(g) ΔH1=-241.8 kJ·mol-1②太阳光分解水制氢气2H2O(l)=2H2(g)+O2(g) ΔH2=571.6 kJ·mol-1
③液态水转化为水蒸气H2O(l)= H2O(g) ΔH3=
(1)从能量转化角度分析,反应①为
(2)反应②中主要能量转化形式为
(3)若在反应②中使用催化剂,ΔH2
(4)写出反应③的热化学方程式
(5)根据下表内容及你所学知识列举氢气被称为“绿色能源”的原因
| 燃料名称 | 热值(kJ/g) |
| 氢气 | 142.9 |
| 一氧化碳 | 10.11 |
| 甲烷 | 55.64 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在“碳达峰”、“碳中和”的国家战略下,工业生产废气和汽车尾气中的 和
和 的减排及有效处理,显得尤为重要。
的减排及有效处理,显得尤为重要。
(1)在汽车上安装三元催化转化器可实现反应:
 。
。
已知: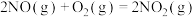
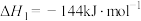 ;
;

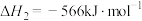

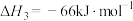 。
。
则
_____ ,该反应在_____ (填“高温”“低温”或“任何温度”)下能自发进行。
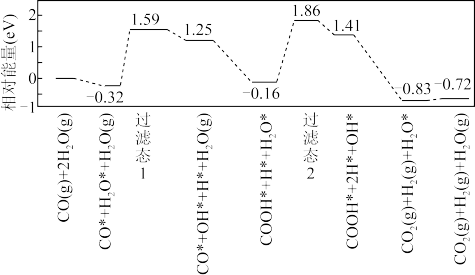
(2)用金作催化剂,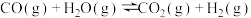 的反应历程如下图所示,其中吸附在金催化剂表面上的微粒用“*”标注。该历程中最大能垒
的反应历程如下图所示,其中吸附在金催化剂表面上的微粒用“*”标注。该历程中最大能垒
_____  ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:_____ 。
(3)将相同量的 和
和 分别充入盛有催化剂(1)和(2)的体积相同的密闭容器,进行反应:
分别充入盛有催化剂(1)和(2)的体积相同的密闭容器,进行反应: ,经过相同时间内测量两容器中
,经过相同时间内测量两容器中 的含量,从而确定
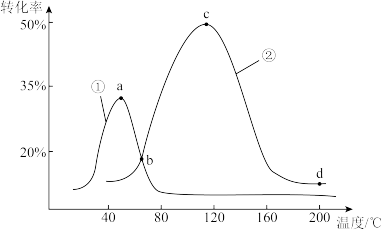
的含量,从而确定 的转化率,结果如下图所示。试判断图像中
的转化率,结果如下图所示。试判断图像中 点是否一定处于平衡状态并分析原因:
点是否一定处于平衡状态并分析原因:_____ 。
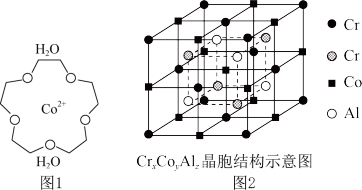
(4)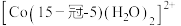 (“15-冠-5”是指冠醚的环上原子总数为15,其中
(“15-冠-5”是指冠醚的环上原子总数为15,其中 原子数为5)是一种配位离子,该配位离子的结构示意图如图1所示(
原子数为5)是一种配位离子,该配位离子的结构示意图如图1所示( 也是配体之一),该配位离子中含有的
也是配体之一),该配位离子中含有的 键数目为
键数目为_____ 。全惠斯勒合金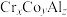 的晶胞结构如图2所示,其化学式为
的晶胞结构如图2所示,其化学式为_____ ;已知该晶胞的边长为 ,则全惠斯勒合金的密度为
,则全惠斯勒合金的密度为_____  。
。
 和
和 的减排及有效处理,显得尤为重要。
的减排及有效处理,显得尤为重要。(1)在汽车上安装三元催化转化器可实现反应:

 。
。已知:
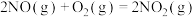
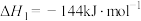 ;
;
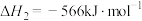

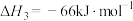 。
。则

(2)用金作催化剂,
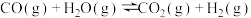 的反应历程如下图所示,其中吸附在金催化剂表面上的微粒用“*”标注。该历程中最大能垒
的反应历程如下图所示,其中吸附在金催化剂表面上的微粒用“*”标注。该历程中最大能垒
 ,写出该步骤的化学方程式:
,写出该步骤的化学方程式:
(3)将相同量的
 和
和 分别充入盛有催化剂(1)和(2)的体积相同的密闭容器,进行反应:
分别充入盛有催化剂(1)和(2)的体积相同的密闭容器,进行反应: ,经过相同时间内测量两容器中
,经过相同时间内测量两容器中 的含量,从而确定
的含量,从而确定 的转化率,结果如下图所示。试判断图像中
的转化率,结果如下图所示。试判断图像中 点是否一定处于平衡状态并分析原因:
点是否一定处于平衡状态并分析原因:
(4)
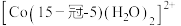 (“15-冠-5”是指冠醚的环上原子总数为15,其中
(“15-冠-5”是指冠醚的环上原子总数为15,其中 原子数为5)是一种配位离子,该配位离子的结构示意图如图1所示(
原子数为5)是一种配位离子,该配位离子的结构示意图如图1所示( 也是配体之一),该配位离子中含有的
也是配体之一),该配位离子中含有的 键数目为
键数目为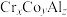 的晶胞结构如图2所示,其化学式为
的晶胞结构如图2所示,其化学式为 ,则全惠斯勒合金的密度为
,则全惠斯勒合金的密度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:
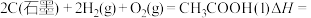
______ 
| 物质 |  (l) (l) | C(石墨) |  |
标准燃烧焓 | -870.3 | -393.5 | -285.8 |
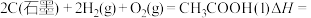

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】通过生物柴油副产物甘油制取 正成为将其高值化利用的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):
正成为将其高值化利用的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):
Ⅰ.
Ⅱ.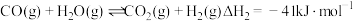
甘油水蒸气重整制氢时,其他条件不变,在不同水醇比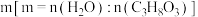 时
时 的平衡产率与温度的关系如图所示。
的平衡产率与温度的关系如图所示。
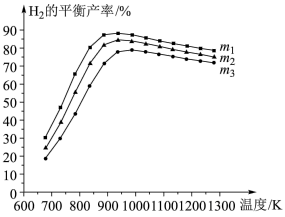
(1)水醇比从大到小的顺序是____________ ;在水醇比不变时 的平衡产率随温度的升高先增大后又减小的主要原因是
的平衡产率随温度的升高先增大后又减小的主要原因是______________ 。
(2)该工艺中 、
、 与
与 反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制
反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制 的生成,提高氢气的产率,可采取的措施有(不考虑压强的影响)
的生成,提高氢气的产率,可采取的措施有(不考虑压强的影响)____________________________________ (列举2条)。
 正成为将其高值化利用的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):
正成为将其高值化利用的一个重要研究方向。生物甘油水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):Ⅰ.

Ⅱ.
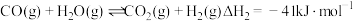
甘油水蒸气重整制氢时,其他条件不变,在不同水醇比
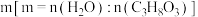 时
时 的平衡产率与温度的关系如图所示。
的平衡产率与温度的关系如图所示。
(1)水醇比从大到小的顺序是
 的平衡产率随温度的升高先增大后又减小的主要原因是
的平衡产率随温度的升高先增大后又减小的主要原因是(2)该工艺中
 、
、 与
与 反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制
反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制 的生成,提高氢气的产率,可采取的措施有(不考虑压强的影响)
的生成,提高氢气的产率,可采取的措施有(不考虑压强的影响)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为了实现“碳中和”的目的,科学家积极探索减少 的排放水平,并通过新技术对
的排放水平,并通过新技术对 进行综合利用。
进行综合利用。
(1) 是一种廉价的碳资源,其综合利用具有重要意义,
是一种廉价的碳资源,其综合利用具有重要意义, 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 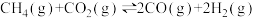
 ,已知上述反应中相关的化学键键能数据如下:
,已知上述反应中相关的化学键键能数据如下:
写出 的电子式
的电子式______ ;则该反应的
______ 。
(2)工业废气中的 可用碱液吸收,所发生的反应如下:
可用碱液吸收,所发生的反应如下:

 ,
,
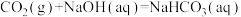
 ,
,
则:
① 的
的
______  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
②标况下,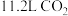 与足量的NaOH溶液充分反应后,放出的热量为
与足量的NaOH溶液充分反应后,放出的热量为______ kJ(用含a或b的代数式表示)。
(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,但同时会释放 ,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
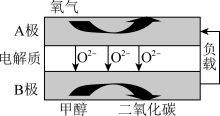
①电极A为______ (填“正”“负”)极;甲醇在电极B上发生的反应式为______ 。
②该电池正常工作一段时间,当电池中有60mol电子转移时,会产生
______ g。
 的排放水平,并通过新技术对
的排放水平,并通过新技术对 进行综合利用。
进行综合利用。(1)
 是一种廉价的碳资源,其综合利用具有重要意义,
是一种廉价的碳资源,其综合利用具有重要意义, 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 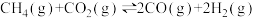
 ,已知上述反应中相关的化学键键能数据如下:
,已知上述反应中相关的化学键键能数据如下:| 化学键 | C—H | C=O | H—H | 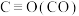 |
键能 | 413 | 745 | 436 | 1075 |
 的电子式
的电子式
(2)工业废气中的
 可用碱液吸收,所发生的反应如下:
可用碱液吸收,所发生的反应如下:
 ,
,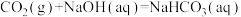
 ,
,则:
①
 的
的
 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。②标况下,
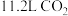 与足量的NaOH溶液充分反应后,放出的热量为
与足量的NaOH溶液充分反应后,放出的热量为(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,但同时会释放
 ,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
①电极A为
②该电池正常工作一段时间,当电池中有60mol电子转移时,会产生

您最近一年使用:0次
【推荐1】CO、CO2的回收和综合利用有利于实现“碳中和”。
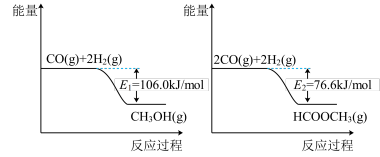
(1)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算2CH3OH(g) HCOOCH3(g)+2H2(g)ΔH=
HCOOCH3(g)+2H2(g)ΔH=_______ 。
已知键能数据如下表。
则C O的键能为
O的键能为 _______ 。
(2)已知:反应1:2CO(g)+4H2(g)═CH3CH2OH(g)+H2O(g)ΔH=-128.8kJ⋅mol﹣1
反应2:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)ΔH=-78.1kJ⋅mol﹣1
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是 _______(填字母)。
(3)CO2催化加氢制甲醇可分两步完成,反应历程如图所示。已知CO(g)+2H2(g)═CH3OH(g)ΔH=-106kJ⋅mol﹣1,则CO2(g)+3H2(g)═CH3OH(g)+H2O(g)ΔH=_______ 。
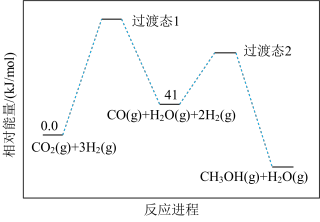
该反应进程中总反应速率由第_______ (“1”或“2”)步决定。
(1)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算2CH3OH(g)
 HCOOCH3(g)+2H2(g)ΔH=
HCOOCH3(g)+2H2(g)ΔH=
已知键能数据如下表。
| 化学键 | H﹣H | C﹣O | C O O | H﹣O | C﹣H |
| 键能/(kJ⋅mol﹣1) | 436 | 326 | a | 464 | 414 |
 O的键能为
O的键能为 (2)已知:反应1:2CO(g)+4H2(g)═CH3CH2OH(g)+H2O(g)ΔH=-128.8kJ⋅mol﹣1
反应2:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)ΔH=-78.1kJ⋅mol﹣1
假设某温度下,反应1的速率大于反应2的速率,则下列反应过程中的能量变化示意图正确的是 _______(填字母)。
A.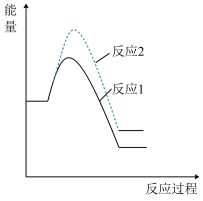 | B. |
C.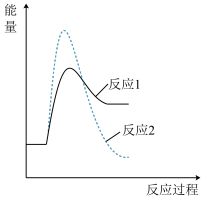 | D.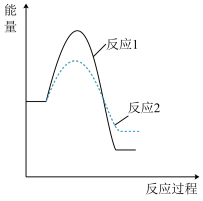 |

该反应进程中总反应速率由第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气嚢内一般充入的是叠氮化钠(NaN3)、硝酸铵(NH4NO3)、硝酸钾(KNO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解或发生反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。请回答下列问题:
(1)下列判断正确的是_______。
(2)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:
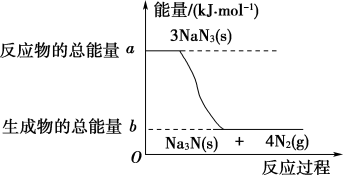
①叠氮化钠的爆炸反应属于_______ (填“吸热”或“放热”)反应。
②若爆炸过程中有30mol非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为_______ kJ(用含a、b的代数式表示),消耗叠氮化钠的质量为_______ g。
(3)若安全气囊内充的是叠氮酸钠和硝酸钾,撞击时发生的反应是10NaN3+2KNO3=K2O+5Na2O+16N2↑。当该反应的氧化产物比还原产物多1.4mol时,转移电子的物质的量是_______ mol;同时气囊内还必须充入一定量的SiO2粉末,其在安全气囊内所起的作用可能是_______ 。
(1)下列判断正确的是_______。
| A.道路起雾与H2O分子的化学键断裂有关 |
| B.NH4NO3、KNO3中均含有离子键和共价键 |
| C.NaN3不会和酸性高锰酸钾或次氯酸钠溶液反应 |
| D.NaN3、NH4NO3固体在储存和使用时都必须格外小心,以免发生爆炸 |

①叠氮化钠的爆炸反应属于
②若爆炸过程中有30mol非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为
(3)若安全气囊内充的是叠氮酸钠和硝酸钾,撞击时发生的反应是10NaN3+2KNO3=K2O+5Na2O+16N2↑。当该反应的氧化产物比还原产物多1.4mol时,转移电子的物质的量是
您最近一年使用:0次