碳的单质及化合物在人类生产生活中起着非常重要的作用。请回答下列问题:
(1)已知CH3OH(l)的燃烧热 ,
,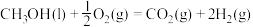
 ,则
,则
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___________ 。
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为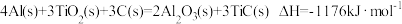 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为_________ kJ。
(4)工业上乙烯催化氧化制乙醛的反应原理为: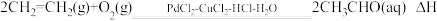 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:
I.
II.……
III.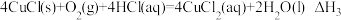
若第II步反应的反应热为 ,且
,且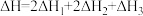 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为__ 。
(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为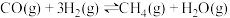 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
该反应的
__________  。
。
(1)已知CH3OH(l)的燃烧热
 ,
,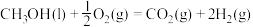
 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
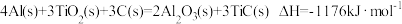 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为(4)工业上乙烯催化氧化制乙醛的反应原理为:
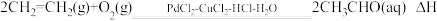 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:I.

II.……
III.
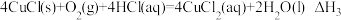
若第II步反应的反应热为
 ,且
,且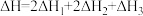 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为
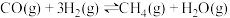 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):| 化学键 |  |  |  |  |  |  |
键能/( ) ) | 347.7 | 413.4 | 436 | 351 | 1065 | 462.8 |

 。
。
更新时间:2021/11/11 22:41:03
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题:
(1)将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol−1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0kJ·mol−1
O2(g)=H2O(g) ΔH=-242.0kJ·mol−1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol−1
O2(g)=CO2(g) ΔH=-283.0kJ·mol−1
写出C(s)与水蒸气反应的热化学反应方程式。_______
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
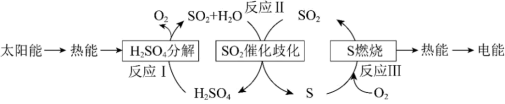
反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297kJ·mol-1
反应II的热化学方程式:_______ 。
(1)将煤转化为水煤气的主要化学反应为C(s)+H2O(g)
 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol−1
H2(g)+
 O2(g)=H2O(g) ΔH=-242.0kJ·mol−1
O2(g)=H2O(g) ΔH=-242.0kJ·mol−1CO(g)+
 O2(g)=CO2(g) ΔH=-283.0kJ·mol−1
O2(g)=CO2(g) ΔH=-283.0kJ·mol−1写出C(s)与水蒸气反应的热化学反应方程式。
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:

反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297kJ·mol-1
反应II的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5 、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5试样的pH=_____________ 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
C(s)+ O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:______________________________________ 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是________ 。(填字母)
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g) ⇌2NO(g) ΔH>0。汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是___________________ 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g) = 2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:____________________ 。
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO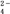 | NO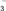 | Cl- |
| 浓度(mol·L-1) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5试样的pH=
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+
 O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1C(s)+
 O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
O2(g) = CO(g) ΔH=-110.5 kJ·mol-1写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气。以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g) ⇌2NO(g) ΔH>0。汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g) = 2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学反应中均伴随有能量变化。
(1)下列反应中,反应物的总能量小于生成物的总能量的为____ (填选项字母)。
(2)已知25℃时,相关物质的相对能量如表所示;
①表示H2(g)燃烧热的热化学方程为____ 。
②0.5molH2O(g)转化为H2O(l)需要____ (填“吸收”或“放出”)____ kJ的热量。
(3)已知:
Ⅰ.2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
根据盖斯定律计算CO(g)+ O2(g)=CO2(g) △H=
O2(g)=CO2(g) △H=____ kJ·mol-1。
(1)下列反应中,反应物的总能量小于生成物的总能量的为
| A.Na与水反应 | B.甲烷的燃烧反应 | C.CaCO3受热分解 | D.锌与盐酸反应 |
| 物质 | H2(g) | O2(g) | H2O(g) | H2O(l) |
| 相对能量(kJ·mol-1) | 0 | 0 | -242 | -286 |
①表示H2(g)燃烧热的热化学方程为
②0.5molH2O(g)转化为H2O(l)需要
(3)已知:
Ⅰ.2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
Ⅱ.C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
根据盖斯定律计算CO(g)+
 O2(g)=CO2(g) △H=
O2(g)=CO2(g) △H=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】试题
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏 mol氧气中的化学键需要吸收249kJ的能量;形成水分子中 1mol H-O 键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。
mol氧气中的化学键需要吸收249kJ的能量;形成水分子中 1mol H-O 键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。
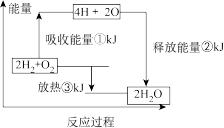
①_________ kJ
②_________ kJ
③_________ kJ
(2)二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。下图是二甲醚、乙烷燃烧过程的能量变化图:
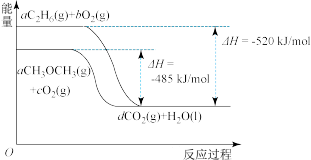
请回答下列问题:
①据图分析,a=__________ ;
②当有3g乙烷完全燃烧时,可放出热量Q =_____________ 。
③请根据该图写出1mol二甲醚完全燃烧的热化学方程式____________ 。
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏
 mol氧气中的化学键需要吸收249kJ的能量;形成水分子中 1mol H-O 键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。
mol氧气中的化学键需要吸收249kJ的能量;形成水分子中 1mol H-O 键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。
①
②
③
(2)二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。下图是二甲醚、乙烷燃烧过程的能量变化图:

请回答下列问题:
①据图分析,a=
②当有3g乙烷完全燃烧时,可放出热量Q =
③请根据该图写出1mol二甲醚完全燃烧的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题。
(1)在101kPa时,1mol CH4完全燃烧生成 和液态
和液态 ,放出890.3kJ的热量,
,放出890.3kJ的热量, 的燃烧热为
的燃烧热为___________ 。11.2LCH4(标准状况)燃烧后所产生的热量为___________
(2)已知0.5mol甲烷与0.5mol水蒸气在t℃、pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量,该反应的热化学方程式是:___________
(1)在101kPa时,1mol CH4完全燃烧生成
 和液态
和液态 ,放出890.3kJ的热量,
,放出890.3kJ的热量, 的燃烧热为
的燃烧热为(2)已知0.5mol甲烷与0.5mol水蒸气在t℃、pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量,该反应的热化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)根据下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH= - 393.5 kJ·mol-1
②H2(g)+ O2(g)===H2O(l) ΔH= - 285.8 kJ·mol-1
O2(g)===H2O(l) ΔH= - 285.8 kJ·mol-1
③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH= - 870.3 kJ·mol-1
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为_____________
(2)已知在101 kPa时,CO的燃烧热为283 kJ·mol-1。相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧的热化学方程式是______________ 。
(3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,C6H6的燃烧热ΔH=________ kJ·mol,该反应的热化学方程式为______________ 。
①C(s)+O2(g)===CO2(g) ΔH= - 393.5 kJ·mol-1
②H2(g)+
 O2(g)===H2O(l) ΔH= - 285.8 kJ·mol-1
O2(g)===H2O(l) ΔH= - 285.8 kJ·mol-1③CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH= - 870.3 kJ·mol-1
可以计算出2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为
(2)已知在101 kPa时,CO的燃烧热为283 kJ·mol-1。相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧的热化学方程式是
(3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,C6H6的燃烧热ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
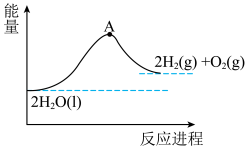
【推荐1】自科学家们开始研究物质的结构与性质以来,氢元素时常担任主角,例如氢原子光谱启发了人们对原子结构的探索。此外,氢气与氢能源也是时下热门的一种绿色能源。氢能是最具发展潜力的清洁能源,但当下的生产条件非常苛刻且纯度不高。因此,科学家们正在寻找更经济、环境友好的方法,电解水便是其中一种。
(1)已知在298K和100kPa的条件下,液态水分解生成氢气:
 。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如
。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如 ,那么图中A点将
,那么图中A点将___________ (填“升高”、“降低”或“不变”)。
(2)部分化学键的键能和反应焓变的数据如下:
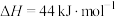 ,
, ,
,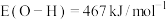 ,
,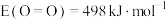 ,由此可计算得上述反应的
,由此可计算得上述反应的 为
为___________ 。又知该反应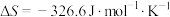 ,那么该反应在298K条件下能否自发进行?
,那么该反应在298K条件下能否自发进行?___________ 。
(3)试从绿色化学的角度比较并评价直接电解海水与太阳能( 作催化剂)分解淡水两种制备氢气的方案
作催化剂)分解淡水两种制备氢气的方案___________ 。
(1)已知在298K和100kPa的条件下,液态水分解生成氢气:

 。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如
。下图为该反应的能量变化示意图,而在实际生产生活中常会使用催化剂,例如 ,那么图中A点将
,那么图中A点将
(2)部分化学键的键能和反应焓变的数据如下:

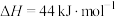 ,
, ,
,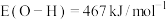 ,
,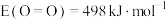 ,由此可计算得上述反应的
,由此可计算得上述反应的 为
为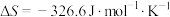 ,那么该反应在298K条件下能否自发进行?
,那么该反应在298K条件下能否自发进行?(3)试从绿色化学的角度比较并评价直接电解海水与太阳能(
 作催化剂)分解淡水两种制备氢气的方案
作催化剂)分解淡水两种制备氢气的方案
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】 是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。
1. 的分子构型为
的分子构型为___________ ; 与
与 互为等电子体,等电子体的化学键类型和空间结构相同,则
互为等电子体,等电子体的化学键类型和空间结构相同,则 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为___________ 。
2.已知拆开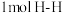 、
、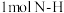 、
、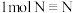 分别需要的能量是
分别需要的能量是 、
、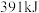 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为___________ 。若该反应的焓变和熵变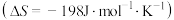 随温度变化很小,则该反应在常温下
随温度变化很小,则该反应在常温下___________ (填“能”或者“不能”)自发进行。合成氨反应加入催化剂后的反应历程示意图为下图中的___________ (填编号)。 左右高温的原因是
左右高温的原因是___________ 。
 是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。1.
 的分子构型为
的分子构型为 与
与 互为等电子体,等电子体的化学键类型和空间结构相同,则
互为等电子体,等电子体的化学键类型和空间结构相同,则 的中心原子杂化轨道类型为
的中心原子杂化轨道类型为2.已知拆开
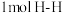 、
、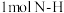 、
、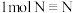 分别需要的能量是
分别需要的能量是 、
、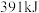 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为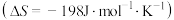 随温度变化很小,则该反应在常温下
随温度变化很小,则该反应在常温下
 左右高温的原因是
左右高温的原因是
您最近一年使用:0次
【推荐3】已知在1×105Pa、298K时断裂1molH—H键吸收的能量为436kJ,断裂1molN—H键吸收的能量为391kJ,断裂1molN≡N键吸收的能量是945kJ。
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)⇌2NH3(g)是_____ (填“吸热”或“放热”)反应。
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为_____ kJ。
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小系为_____
A.Q1<Q2B.Q1>Q2C.Q1=Q2
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)⇌2NH3(g)是
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小系为
A.Q1<Q2B.Q1>Q2C.Q1=Q2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
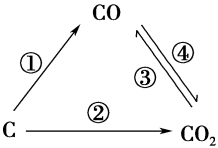
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可以是__________________ 。
(2)把煤作为燃料可通过下列两种途径:
途径 Ⅰ:C(s)+O2(g) =CO2(g) ΔH1<0 ①
途径 Ⅱ:先制成水煤气:C(s)+H2O(g) =CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g) =2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)= 2H2O(g) ΔH4<0 ④
则途径 Ⅰ 放出的热量__________ (填“大于”“等于”或“小于”)途径 Ⅱ 放出的热量;ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是____________________ 。
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
方法二 CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
在25 ℃、101 kPa下,1 g甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式________________________________________________________________ 。
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g) =3Ag2O(s) ΔH=―235.8 kJ·mol―1 ①
已知:2Ag2O(s) =4Ag(s)+O2(g) ΔH=+62.2 kJ·mol―1 ②
则O3转化为O2的热化学方程式为__________________________ 。
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可以是

(2)把煤作为燃料可通过下列两种途径:
途径 Ⅰ:C(s)+O2(g) =CO2(g) ΔH1<0 ①
途径 Ⅱ:先制成水煤气:C(s)+H2O(g) =CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g) =2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)= 2H2O(g) ΔH4<0 ④
则途径 Ⅰ 放出的热量
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)方法二 CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)在25 ℃、101 kPa下,1 g甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g) =3Ag2O(s) ΔH=―235.8 kJ·mol―1 ①
已知:2Ag2O(s) =4Ag(s)+O2(g) ΔH=+62.2 kJ·mol―1 ②
则O3转化为O2的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应都伴有能量变化,请回答下列问题:
(1)书写下列反应的热化学方程式。(每个热化学方程式3分)
①1L1mol/L稀盐酸跟1L1mol/LNaOH溶液发生中和反应放出57.3kJ热量。___________ 。
②24 与足量
与足量 反应生成
反应生成 和
和 ,吸收262.6kJ热量。
,吸收262.6kJ热量。___________
③已知16g固体硫完全燃烧时放出148.4kJ的热量,写出表示硫的燃烧的热化学方程式:___________ 。
④如图是298K、101kPa时, 与
与 反应过程中能量变化的曲线图。该反应的热化学方程式为:
反应过程中能量变化的曲线图。该反应的热化学方程式为: ___________ 。

(2)比较下列各组热化学方程式中 的大小关系。
的大小关系。
①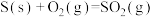

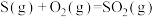


___________ 
②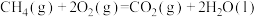

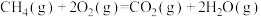


___________ 
③




___________ 
④煤作为燃料有2种途径:
途径1——直接燃烧:

途径2——先制水煤气:

再燃烧水煤气;

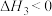
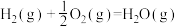
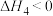
 、
、 、
、 、
、 的关系式是
的关系式是___________ 。
(1)书写下列反应的热化学方程式。(每个热化学方程式3分)
①1L1mol/L稀盐酸跟1L1mol/LNaOH溶液发生中和反应放出57.3kJ热量。
②24
 与足量
与足量 反应生成
反应生成 和
和 ,吸收262.6kJ热量。
,吸收262.6kJ热量。③已知16g固体硫完全燃烧时放出148.4kJ的热量,写出表示硫的燃烧的热化学方程式:
④如图是298K、101kPa时,
 与
与 反应过程中能量变化的曲线图。该反应的热化学方程式为:
反应过程中能量变化的曲线图。该反应的热化学方程式为: 
(2)比较下列各组热化学方程式中
 的大小关系。
的大小关系。①
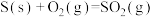

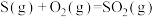



②
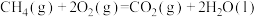

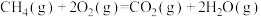



③






④煤作为燃料有2种途径:
途径1——直接燃烧:


途径2——先制水煤气:


再燃烧水煤气;

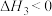
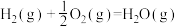
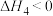
 、
、 、
、 、
、 的关系式是
的关系式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】依据事实,写出下列反应的热化学方程式。
(1)1molN2(g)与适量 H2(g)起反应,生成NH3(g),放出92.2kJ热量。____________ 。
(2)1molN2(g)与适量 O2(g)起反应,生成NO2(g),吸收68kJ热量。__________________________ 。
(3)16 g甲醇气体燃烧生成CO2和液态水时放热362.88 kJ,则该反应的热化学方程式应为___________ 。
(4)已知CO(g)的燃烧热为283kJ/mol,则它的燃烧热的热化学方程式为__________________ 。
(5)1gCH4完全燃烧生成液态水和CO2,放出55.6kJ热量,则CH4的燃烧热的热化学方程式为_____ 。
(6)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol–1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol–1
写出Na2CO3·H2O脱水反应的热化学方程式___________ 。
(7)下列三组溶液
①20mL、0.1mol/LHCl + 20mL、0.1mol/LNH3·H2O ②10mL、0.2mol/LHCl + 30mL、0.1mol/LNaOH
③10mL、0.1mol/L H2SO4 + 30mL、0.1mol/LNH3·H2O
发生反应的反应热ΔH1、ΔH2、ΔH3大小关系为_______________________________ 。
(1)1molN2(g)与适量 H2(g)起反应,生成NH3(g),放出92.2kJ热量。
(2)1molN2(g)与适量 O2(g)起反应,生成NO2(g),吸收68kJ热量。
(3)16 g甲醇气体燃烧生成CO2和液态水时放热362.88 kJ,则该反应的热化学方程式应为
(4)已知CO(g)的燃烧热为283kJ/mol,则它的燃烧热的热化学方程式为
(5)1gCH4完全燃烧生成液态水和CO2,放出55.6kJ热量,则CH4的燃烧热的热化学方程式为
(6)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol–1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol–1
写出Na2CO3·H2O脱水反应的热化学方程式
(7)下列三组溶液
①20mL、0.1mol/LHCl + 20mL、0.1mol/LNH3·H2O ②10mL、0.2mol/LHCl + 30mL、0.1mol/LNaOH
③10mL、0.1mol/L H2SO4 + 30mL、0.1mol/LNH3·H2O
发生反应的反应热ΔH1、ΔH2、ΔH3大小关系为
您最近一年使用:0次



