溶液中的反应大多都是离子反应,请按要求回答下列问题:
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是___ (填字母标号)。
(2)泡沫灭火器的反应原理是盐类水解,请写出其离子方程式:___ 。
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是___ 。
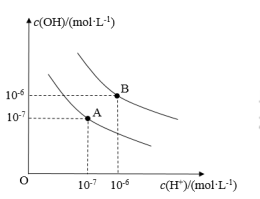
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为___ 。
(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是___ (用a、b、c表示,下同)。
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为___ 。
(1)要求设计实验证明盐类水解是吸热过程,有四位学生分别做了以下实验,其中根据实验现象得出的结论正确的是
| A.甲学生:在醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深,说明盐类水解是吸热的 |
| B.乙学生:将硝酸铵晶体溶于水,水温下降,说明硝酸铵水解是吸热的 |
| C.丙学生:在盐酸中加入同温度的氨水,混合液温度下降,说明盐类水解是吸热的 |
| D.丁学生:在醋酸钠溶液中加入醋酸钠晶体,溶液温度下降,说明盐类水解是吸热的 |
(3)将一定浓度的CH3COOH溶液和NaOH溶液等体积混合,测得所得溶液的pH=7,则该溶液中离子浓度的大小关系是
(4)已知水在25℃和95℃时的电离平衡曲线如图所示:95℃时,将pH=9的NaOH溶液与pH=4的H2SO4,溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4,溶液的体积比为

(5)在一定温度下,有以下三种酸:a.醋酸 b.硫酸 c.盐酸。
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
②当三种酸的pH相同、体积相同时,分别加入足量的锌,产生H2的体积(相同状况)大小关系为
更新时间:2021/11/13 20:30:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知该产业链中,有炭参与的某反应平衡常数表达式为:K=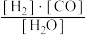 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:________ ,若该反应只有在持续高温下才能自发进行,则该反应为________ (“吸热”或“放热”)反应。
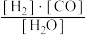 ,写出它所对应反应的化学方程式:
,写出它所对应反应的化学方程式:
您最近一年使用:0次
【推荐2】化学反应伴随能量变化,获取反应能量变化有多种途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
则2H2(g)+O2(g)=2H2O(g)ΔH=___________ kJ·mol-1。
②通过物质所含能量计算。
已知反应A+B=C+D中A、B、C、D所含能量依次可表示为EA、EB、EC、ED,该反应ΔH=___________ 。
③通过盖斯定律计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+ O2(g)=Na2O(s)ΔH=-414kJ·mol-1
O2(g)=Na2O(s)ΔH=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g)=Na2O2(s)ΔH=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol·L-1盐酸,则还需加入___________ (填字母)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.Na2O与水反应 | B.甲烷的燃烧反应 | C.CaCO3受热分解 | D.锌与盐酸反应 |
①通过化学键的键能计算。已知:
| 化学键 | H—H | O=O | O—H |
| 键能/(kJ·mol-1) | 436 | 498 | 463.4 |
②通过物质所含能量计算。
已知反应A+B=C+D中A、B、C、D所含能量依次可表示为EA、EB、EC、ED,该反应ΔH=
③通过盖斯定律计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+
 O2(g)=Na2O(s)ΔH=-414kJ·mol-1
O2(g)=Na2O(s)ΔH=-414kJ·mol-1Ⅱ.2Na(s)+O2(g)=Na2O2(s)ΔH=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50mL0.50mol·L-1盐酸,则还需加入
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
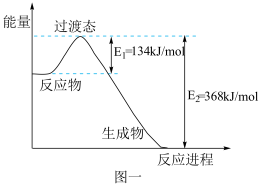
(1)图一是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________ 。在反应体系中加入催化剂,E1和E2的变化是:E1___________ ,E2___________ (填“增大”、“减小”或“不变”),对反应热是否有影响?___________ ,原因是___________ 。
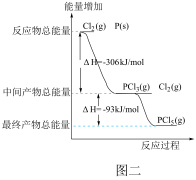
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
① P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式___________ 。
② P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)的△H2关系是:△H2___________ △H1(填“大于”、“小于”或“等于”),原因是___________ 。


(1)图一是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(2)图二是红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)的反应过程与能量关系图(图中的△H表示生成1mol产物的数据)。根据图二回答下列问题:
① P(s)和Cl2(g)反应生成PCl3(g)的热化学方程式
② P(s)和Cl2(g)分两步反应生成1molPCl5(g)的△H1与P(s)和Cl2(g)一步反应生成1molPCl5(g)的△H2关系是:△H2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
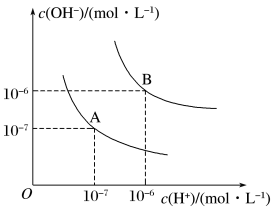
①100℃时1mol/L的NaOH溶液中,由水电离出的
___________  。
。
②25℃时,向水的电离平衡体系中加入少量 固体,对水的电离平衡的影响是
固体,对水的电离平衡的影响是___________ (填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量,已知如表数据,
①25℃时,有等浓度的a.NaCN溶液 b. 溶液 c.
溶液 c. 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为___________ (填序号)。
②25℃时, 的
的 溶液和
溶液和 的NaOH溶液等体积混合,混合后溶液显
的NaOH溶液等体积混合,混合后溶液显___________ (填“酸性”、“碱性”、“中性”)。等浓度的 溶液和NaOH溶液等体积混合,则
溶液和NaOH溶液等体积混合,则
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)25℃时,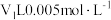 的
的 溶液与
溶液与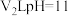 的
的 溶液混合,混合后
溶液混合,混合后 ,求
,求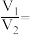
___________ 。
(4)写出将少量 通入NaClO中的化学方程式:
通入NaClO中的化学方程式:___________ 。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。

①100℃时1mol/L的NaOH溶液中,由水电离出的

 。
。②25℃时,向水的电离平衡体系中加入少量
 固体,对水的电离平衡的影响是
固体,对水的电离平衡的影响是(2)电离平衡常数是衡量弱电解质电离程度强弱的量,已知如表数据,
| 化学式 | 电离平衡常数(25℃) |
| HCN |  |
 | 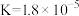 |
 | 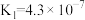 、 、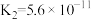 |
| HClO | 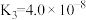 |
①25℃时,有等浓度的a.NaCN溶液 b.
 溶液 c.
溶液 c. 溶液,三种溶液的pH由大到小的顺序为
溶液,三种溶液的pH由大到小的顺序为②25℃时,
 的
的 溶液和
溶液和 的NaOH溶液等体积混合,混合后溶液显
的NaOH溶液等体积混合,混合后溶液显 溶液和NaOH溶液等体积混合,则
溶液和NaOH溶液等体积混合,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)25℃时,
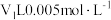 的
的 溶液与
溶液与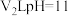 的
的 溶液混合,混合后
溶液混合,混合后 ,求
,求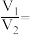
(4)写出将少量
 通入NaClO中的化学方程式:
通入NaClO中的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识填写下列空白。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =__________________ 。
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式____________________________________________ 。
(3)温度下纯水中的c(H+)=1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)=5×10-5mol/L,则由水电离出的c(H+)=__________ mol/L。
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=_________ 。
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-,HB- H++B2-。
H++B2-。
已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是____________________________________ 。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式
(3)温度下纯水中的c(H+)=1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)=5×10-5mol/L,则由水电离出的c(H+)=
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-,HB-
 H++B2-。
H++B2-。已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知水在25 ℃和95 ℃时,水电离平衡曲线如图所示:
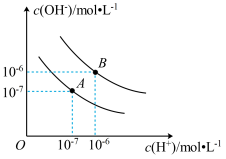
(1)95 ℃时,水的电离平衡曲线应为B,请说明理由:_______________________________ 。25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为____________ 。
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1________ (填“大于”“小于”“等于”或“无法确定”)α2。
(3)曲线B对应温度下,将0.02 mol·L-1Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=________ 。

(1)95 ℃时,水的电离平衡曲线应为B,请说明理由:
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1
(3)曲线B对应温度下,将0.02 mol·L-1Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题:
(1)若浓度均为0.1mol·L-1、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则m______ n (填“>”、“<”或“=”)。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_______ ;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_______ 。
(3)物质的量浓度相同的①NH4Cl,②CH3COONH4,③NH4HSO4,④NH3·H2O四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)____________________________ 。
(4)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液a L与pH=2的H2SO4溶液bL混和(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则出a∶b=_________ 。
(1)若浓度均为0.1mol·L-1、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH都变成9,则m
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(3)物质的量浓度相同的①NH4Cl,②CH3COONH4,③NH4HSO4,④NH3·H2O四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)
(4)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液a L与pH=2的H2SO4溶液bL混和(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则出a∶b=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】食醋是烹饪美食的调味品,能改善调节人体的新陈代谢,其有效成分为 ,为一元弱酸,回答下列问题:
,为一元弱酸,回答下列问题:
(1)25℃时, 的醋酸溶液中,由水电离出的
的醋酸溶液中,由水电离出的
___________  。
。
(2)已知 的
的 ,
, 的
的 ,则
,则 的浓溶液呈
的浓溶液呈___________ 性(酸性、中性或碱性),试解释原因___________ (用文字和方程式说明)。
(3)设计实验证明 为弱酸
为弱酸___________ 。
(4) (醋酸钡晶体)是一种媒染剂。向醋酸溶液中加入
(醋酸钡晶体)是一种媒染剂。向醋酸溶液中加入 溶液,通过一系列操作可以制得
溶液,通过一系列操作可以制得 。
。
①在25℃时,若向醋酸溶液中加入 溶液至溶液的
溶液至溶液的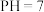 ,此时溶液中
,此时溶液中 ,则溶液中
,则溶液中
_______ 。
②下列有关 醋酸钡溶液中粒子浓度的比较错误的是
醋酸钡溶液中粒子浓度的比较错误的是_______ 。
A.
B.
C.
D.
(5)根据Ka可以判断弱酸的酸性强弱,写出一种无机弱酸及其用途_______ 。
 ,为一元弱酸,回答下列问题:
,为一元弱酸,回答下列问题:(1)25℃时,
 的醋酸溶液中,由水电离出的
的醋酸溶液中,由水电离出的
 。
。(2)已知
 的
的 ,
, 的
的 ,则
,则 的浓溶液呈
的浓溶液呈(3)设计实验证明
 为弱酸
为弱酸(4)
 (醋酸钡晶体)是一种媒染剂。向醋酸溶液中加入
(醋酸钡晶体)是一种媒染剂。向醋酸溶液中加入 溶液,通过一系列操作可以制得
溶液,通过一系列操作可以制得 。
。①在25℃时,若向醋酸溶液中加入
 溶液至溶液的
溶液至溶液的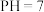 ,此时溶液中
,此时溶液中 ,则溶液中
,则溶液中
②下列有关
 醋酸钡溶液中粒子浓度的比较错误的是
醋酸钡溶液中粒子浓度的比较错误的是A.

B.

C.

D.

(5)根据Ka可以判断弱酸的酸性强弱,写出一种无机弱酸及其用途
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】菠菜口感清甜软滑,含有较高的蛋白质、维生素、胡萝卜素、铁等营养物质。菠菜中富含草酸(乙二酸H2C2O4)而有苦涩味,烹饪菠菜的时候,先把菠菜在开水中焯(chao)一下,可去除苦涩味。
已知:乙二酸电离平衡常数(25℃)Ka1=5.6×10-2,Ka2=5.4×10-5;草酸溶解度9.5g/100g水(20℃);草酸钙Ksp=2.57×109(25°C)
1.写出草酸在水中的电离方程式_____ 。
2.食用菠菜后,在胃部草酸主要的存在形式是_____ (单选)
A.H2C2O4 B. C.
C.
3.为什么烹饪菠菜把菠菜在开水中焯(chao)一下,可去除苦涩味?_____ 。
4.要使溶液中H2C2O4的电离程度增大,可以采取措施_____(不定项)
5.通过计算判断常温下(25℃)NaHC2O4溶液酸碱性_____ 。
6.0.1mol/L草酸溶液中c(H2C2O4)、c( )、c(
)、c( )、c(H+)的大小_____(单选)
)、c(H+)的大小_____(单选)
7.关于K2C2O4溶液中有关离子浓度的说法正确的是_____。
8.25℃时,在草酸钙(CaC2O4)的饱和溶液中存在平衡:CaC2O4(s) Ca2+(aq)+
Ca2+(aq)+ (aq),下列说法错误的是_____。
(aq),下列说法错误的是_____。
9.为什么过量吃菠菜会造成人体缺钙?_____ 。
10.若0.1mol/L的H2C2O4溶液中第二步电离的c(H+)=amol/L,则0.1mol/L的NaHC2O4溶液中 电离出来的c(H+)
电离出来的c(H+)_____ amol/L(单选)
A.= B.< C.>
已知:乙二酸电离平衡常数(25℃)Ka1=5.6×10-2,Ka2=5.4×10-5;草酸溶解度9.5g/100g水(20℃);草酸钙Ksp=2.57×109(25°C)
1.写出草酸在水中的电离方程式
2.食用菠菜后,在胃部草酸主要的存在形式是
A.H2C2O4 B.
 C.
C.
3.为什么烹饪菠菜把菠菜在开水中焯(chao)一下,可去除苦涩味?
4.要使溶液中H2C2O4的电离程度增大,可以采取措施_____(不定项)
| A.加水 | B.加热 | C.加压 | D.通入HC1气体 |
6.0.1mol/L草酸溶液中c(H2C2O4)、c(
 )、c(
)、c( )、c(H+)的大小_____(单选)
)、c(H+)的大小_____(单选)A.c(H2C2O4)>c( )>c( )>c( )>c(H+) )>c(H+) |
B.c(H2C2O4)>c(H+)>c( )>c( )>c( ) ) |
C.c( )>c( )>c( )>c(H+)>c(H2C2O4) )>c(H+)>c(H2C2O4) |
D.c(H+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
A.c(K+)+c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
B.2c(K+)=c( )+c( )+c( )+c(H2C2O4) )+c(H2C2O4) |
C.c( )+c(H2C2O4)+c(H+)= c(OH-) )+c(H2C2O4)+c(H+)= c(OH-) |
D.对溶液进行稀释,c( )与c( )与c( )的比值减小 )的比值减小 |
 Ca2+(aq)+
Ca2+(aq)+ (aq),下列说法错误的是_____。
(aq),下列说法错误的是_____。| A.胃酸能使沉淀溶解平衡向右移动 |
B.加入少量CaCl2固体,溶液中 浓度减小 浓度减小 |
| C.加入少量CaCl2固体,溶度积常数Ksp减小 |
| D.CaC2O4在CaCl2溶液中的溶解度比在水中小 |
10.若0.1mol/L的H2C2O4溶液中第二步电离的c(H+)=amol/L,则0.1mol/L的NaHC2O4溶液中
 电离出来的c(H+)
电离出来的c(H+)A.= B.< C.>
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铁粉、活性炭等成分可与空气中的氧气接触发生化学反应并产生热量,采用先进的自发热控温技术,可以制成蒸汽眼罩。高铁酸钠(Na2FeO4)是水处理过程中使用的一种净水剂。
(1)基态铁原子中有_______ 种能量不同的电子,铁原子次外层的电子云有_______ 种不同的伸展方向。
(2)结合图,补充完整Fe2+的核外电子排布式[Ar]_______ 。
(4)写出使用蒸汽眼罩时,所发生的还原反应的半反应方程式_______。
(5)与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为_______ 。
(6)配平制取高铁酸钠的化学方程式:_______ 。
_____Fe(NO3)3+_______NaOH+_______Cl2=_______Na2FeO4+______NaNO3+______NaCl+ ______H2O。
(7)高铁酸钠(Na2FeO4) 可用作净水剂,其原因是_______。
(1)基态铁原子中有
(2)结合图,补充完整Fe2+的核外电子排布式[Ar]

| A.a1%表示54Fe的质量分数 |
| B.a4%表示58Fe的原子个数百分比 |
| C.55.85表示56Fe的质量数 |
| D.A表示铁元素的近似相对原子质量 |
(4)写出使用蒸汽眼罩时,所发生的还原反应的半反应方程式_______。
A.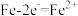 |
B.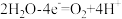 |
C. |
D. |
(5)与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为
(6)配平制取高铁酸钠的化学方程式:
_____Fe(NO3)3+_______NaOH+_______Cl2=_______Na2FeO4+______NaNO3+______NaCl+ ______H2O。
(7)高铁酸钠(Na2FeO4) 可用作净水剂,其原因是_______。
| A.可消毒杀菌,还原产物能吸附水中杂质 |
| B.可消毒杀菌,氧化产物能吸附水中杂质 |
| C.能吸附水中杂质,还原产物能消毒杀菌 |
| D.能吸附水中杂质,氧化产物能消毒杀菌 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电絮凝技术(EC)是一种集混凝、气浮、电化学于一体的新兴水处理技术,实验表明电絮凝技术能除去废水中96%以上的磷(主要以PO 形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
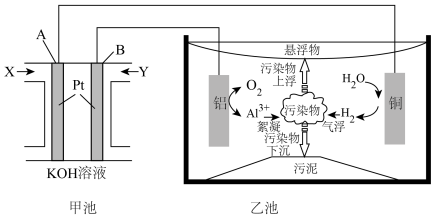
回答下列问题:
(1)燃料电池中OH-向___________ 极(填A或B)移动。写出A电极反应式___________ 。
(2)乙池中铜电极发生___________ 反应(填“氧化”或“还原”)。
(3)乙池铝电极上存在两个竞争反应,电极反应式分别为___________ ,___________ 。
(4)乙池由于电解过程中产生能吸附水中油污等污染物。用离子方程式说明净水的原因为___________ 。
 形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
形式存在)和油污,某化学兴趣小组用CH4燃料电池作为电源模拟电絮凝净水,装置如图所示。
回答下列问题:
(1)燃料电池中OH-向
(2)乙池中铜电极发生
(3)乙池铝电极上存在两个竞争反应,电极反应式分别为
(4)乙池由于电解过程中产生能吸附水中油污等污染物。用离子方程式说明净水的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As( Ⅲ)亚砷酸盐和As(V)砷酸盐形式存在。
(1)砷与磷为同一主族元素,磷的原子结构示意图为___________________ 。
(2)根据元素周期律,下列说法正确的是____________________ (填字母代号)。
a.最高价氧化物对应水化物的酸性:S>P>As b. 原子半径:S>P>As c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为_________________________ 。
(4)去除水体中的砷,可先将As(Ⅲ )转化为As(V),选用NaClO可实现该转化。
已知:投料前水样pH=5.81,0.1 mol/L NaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸。
研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:
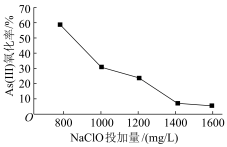
产生此结果的原因是_________________________ 。
(5)强阴离子交换柱可以吸附以阴离子形式存在的As(V),从而达到去除As的目的。
已知:一定条件下,As(V)的存在形式如下表所示:
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是_____________________ 。
(1)砷与磷为同一主族元素,磷的原子结构示意图为
(2)根据元素周期律,下列说法正确的是
a.最高价氧化物对应水化物的酸性:S>P>As b. 原子半径:S>P>As c.非金属性:S>P>As
(3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为
(4)去除水体中的砷,可先将As(Ⅲ )转化为As(V),选用NaClO可实现该转化。
已知:投料前水样pH=5.81,0.1 mol/L NaClO溶液pH=10.5,溶液中起氧化作用的物质是次氯酸。
研究NaClO投加量对As(Ⅲ)氧化率的影响得到如下结果:

产生此结果的原因是
(5)强阴离子交换柱可以吸附以阴离子形式存在的As(V),从而达到去除As的目的。
已知:一定条件下,As(V)的存在形式如下表所示:
| pH | <2 | 2~7 | 7~11 | 11~14 |
| 存在形式 | H3AsO4 | H2AsO4- | HAsO42- | HAsO42-、AsO43- |
pH=6时,NaClO氧化亚砷酸(H3AsO3)的离子方程式是
您最近一年使用:0次



