合成氨工业对国民经济和社会发展具有重要的意义。其原理为: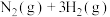


据此回答以下问题:
(1)当有0.5molN2反应完,放出的热量是___________ kJ
(2)此反应能自发进行的条件是___________
(3)某温度下,若把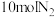 与
与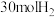 置于体积为
置于体积为 的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为
的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为 ,则用N2表示该反应的平均反应速率为
,则用N2表示该反应的平均反应速率为___________ ,能说明该反应达到化学平衡状态的是___________ (填字母)。
 容器内的密度保持不变
容器内的密度保持不变  容器内压强保持不变
容器内压强保持不变
 υ正
υ正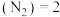 υ逆(NH3) d.混合气体中
υ逆(NH3) d.混合气体中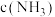 不变
不变
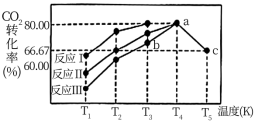
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)___________ 。
a.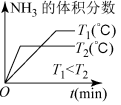 b.
b. c.
c.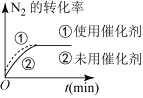
(5)相同温度下,有恒容密闭容器 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量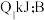 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量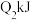 。则:a
。则:a_______ b填“ ”、“
”、“ ”或“
”或“ ”,下同Q1
”,下同Q1______ Q2
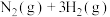


据此回答以下问题:
(1)当有0.5molN2反应完,放出的热量是
(2)此反应能自发进行的条件是
(3)某温度下,若把
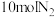 与
与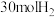 置于体积为
置于体积为 的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为
的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为 ,则用N2表示该反应的平均反应速率为
,则用N2表示该反应的平均反应速率为 容器内的密度保持不变
容器内的密度保持不变  容器内压强保持不变
容器内压强保持不变 υ正
υ正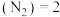 υ逆(NH3) d.混合气体中
υ逆(NH3) d.混合气体中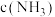 不变
不变(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)
a.
 b.
b. c.
c.
(5)相同温度下,有恒容密闭容器
 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量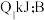 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量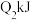 。则:a
。则:a ”、“
”、“ ”或“
”或“ ”,下同Q1
”,下同Q1
更新时间:2021/12/02 10:44:55
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
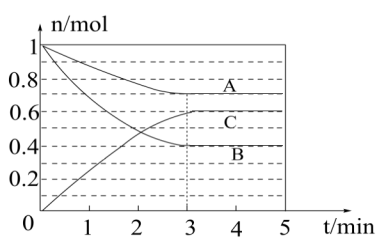
【推荐1】某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
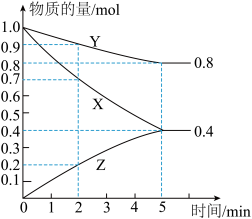
①该反应的化学方程式是______ 。
②0~2min时用X来表示该反应的平均速率为______ 。
③该反应达到平衡状态的标志是______ (填字母)。
A.X、Y的反应速率比为3∶1
B.Y的物质的量浓度在混合气体中保持不变
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ

①该反应的化学方程式是
②0~2min时用X来表示该反应的平均速率为
③该反应达到平衡状态的标志是
A.X、Y的反应速率比为3∶1
B.Y的物质的量浓度在混合气体中保持不变
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在一定温度下,密闭容器中发生反应:2NO2 2NO+O2,经2 min后,测得混合气中NO2浓度为0.06 mol·L-1,O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
2NO+O2,经2 min后,测得混合气中NO2浓度为0.06 mol·L-1,O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
求:
(1)NO2的起始浓度__________ 。
(2)2 min时NO2的转化率_________ 。
(3)2 min内生成NO的化学反应速率_________ 。
 2NO+O2,经2 min后,测得混合气中NO2浓度为0.06 mol·L-1,O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
2NO+O2,经2 min后,测得混合气中NO2浓度为0.06 mol·L-1,O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。求:
(1)NO2的起始浓度
(2)2 min时NO2的转化率
(3)2 min内生成NO的化学反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】一定条件下2L的密闭容器中,反应aA(g)+bB(g) cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。
(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为________ mol/(L·min)
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b_____ c+d(选填“>”、“<”或“=”),v逆_____ (选填“增大”、“减小”或“不变”)
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是______ 。(选填编号)
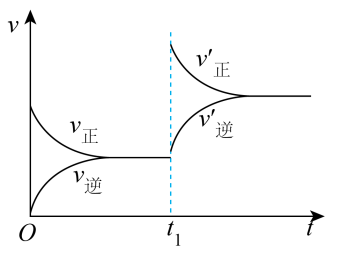
a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
 cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是

a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
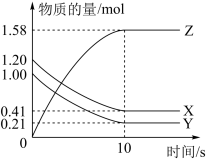
(1)写出该反应的化学方程式_______ 。
(2)下列叙述中能说明上述反应达到平衡状态的是_______ 。
a.当X与Y的反应速率之比为1:1
b.混合气体的压强不变
c.X、Y、Z的浓度之比为1∶1∶2
d.X的浓度保持不变
(3)为使该反应的反应速率增大,可采取的措施是_______ 。
a.降低温度
b.减小容器的体积
c.保持体积不变,充入一定量Z
d.保持压强不变,充入He使容器的体积增大

(1)写出该反应的化学方程式
(2)下列叙述中能说明上述反应达到平衡状态的是
a.当X与Y的反应速率之比为1:1
b.混合气体的压强不变
c.X、Y、Z的浓度之比为1∶1∶2
d.X的浓度保持不变
(3)为使该反应的反应速率增大,可采取的措施是
a.降低温度
b.减小容器的体积
c.保持体积不变,充入一定量Z
d.保持压强不变,充入He使容器的体积增大
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】甲在某一容积为 5L 的密闭容器内加入 0.2mol 的 CO 和 0.2mol 的 H2O,发生如下反应: CO(g)+H2O(g) CO2(g)+H2(g)△H>0,反应中 CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g)△H>0,反应中 CO2的浓度随时间变化情况如下图:
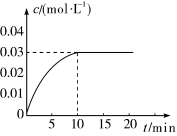
(1)反应开始至达到平衡时,CO 的平均反应速率为______ ; 反应达到平衡时,c(H2O)= ______ 。
(2)判断该反应达到平衡的依据是______ 。
①CO减少的质量和CO2减少的质量相等;
②CO、H2O、CO2、H2的浓度都相等;
③CO、H2O、CO2、H2的浓度都不再发生变化;
(3)若该反应使用催化剂加快反应速率,该反应的ΔH______ (填“变大”“变小”或“不变”)。
 CO2(g)+H2(g)△H>0,反应中 CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g)△H>0,反应中 CO2的浓度随时间变化情况如下图:
(1)反应开始至达到平衡时,CO 的平均反应速率为
(2)判断该反应达到平衡的依据是
①CO减少的质量和CO2减少的质量相等;
②CO、H2O、CO2、H2的浓度都相等;
③CO、H2O、CO2、H2的浓度都不再发生变化;
(3)若该反应使用催化剂加快反应速率,该反应的ΔH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
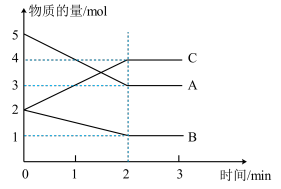
(1)该反应的化学方程式为___________ 。
(2)反应开始至2min时,B的平均反应速率为___________ ,A的转化率为___________ 。
(3)能说明该反应已达到平衡状态的是___________(填字母)。
(4)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是___________ (填序号)。
①降低温度 ②加入催化剂(正) ③增大容器容积

(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是___________(填字母)。
| A.v(A)=2v(B) |
| B.容器内压强保持不变 |
| C.2v逆(A)=v正(B) |
| D.容器内混合气体的密度保持不变 |
①降低温度 ②加入催化剂(正) ③增大容器容积
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.以下是生产、生活中常见的物质。①冰醋酸;② ;③NaOH;④盐酸溶液;⑤
;③NaOH;④盐酸溶液;⑤ ;⑥
;⑥ ;⑦石墨;⑧酒精;⑨
;⑦石墨;⑧酒精;⑨ ;⑩
;⑩
(1)属于强电解质的有___________ ,属于非电解质的有___________ ,能导电的物质有___________ 。(用序号填空)
(2)写出⑥在水溶液中的电离方程式:___________
Ⅱ.在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:
(3)能判断该反应是否达到化学平衡状态的依据是___________。(填字母)
(4)下列措施可以提高 的平衡转化率的是___________(填字母)。
的平衡转化率的是___________(填字母)。
Ⅲ.工业合成氨是人类科学技术的一项重大突破,反应的化学方程式为 。某科研小组研究发现:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图:
。某科研小组研究发现:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图:
①a、b、c三点所处的平衡状态中,反应物 的转化率最高的是:
的转化率最高的是:___________
②合成氨工业中,为提高氨气的平衡产率,除适当控制反应的温度和压强外,还可采取的措施是___________ 。
 ;③NaOH;④盐酸溶液;⑤
;③NaOH;④盐酸溶液;⑤ ;⑥
;⑥ ;⑦石墨;⑧酒精;⑨
;⑦石墨;⑧酒精;⑨ ;⑩
;⑩
(1)属于强电解质的有
(2)写出⑥在水溶液中的电离方程式:
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度T的关系如表:
,其化学平衡常数K和温度T的关系如表:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)能判断该反应是否达到化学平衡状态的依据是___________。(填字母)
A.容器内 、 、 、CO、 、CO、 物质的量浓度之比为1∶1∶1∶1 物质的量浓度之比为1∶1∶1∶1 |
| B.混合气体密度不变 |
C.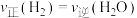 |
D. 和CO的物质的量之比保持不变 和CO的物质的量之比保持不变 |
(4)下列措施可以提高
 的平衡转化率的是___________(填字母)。
的平衡转化率的是___________(填字母)。| A.选择适当的催化剂 | B.增大压强 | C.及时分离出 (g) (g) | D.升高温度 |
Ⅲ.工业合成氨是人类科学技术的一项重大突破,反应的化学方程式为
 。某科研小组研究发现:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图:
。某科研小组研究发现:在其他条件不变的情况下,不同温度时,固定氮气的投入量,起始氢气的物质的量与平衡时氨气的百分含量关系如图: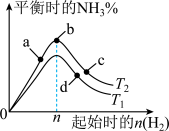
①a、b、c三点所处的平衡状态中,反应物
 的转化率最高的是:
的转化率最高的是:②合成氨工业中,为提高氨气的平衡产率,除适当控制反应的温度和压强外,还可采取的措施是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】恒温恒容下,A容器中加入1g 和1g
和1g 反应达到平衡,
反应达到平衡, 的转化率为a%,另一同温同容的B容器中加入2g
的转化率为a%,另一同温同容的B容器中加入2g 和2g
和2g 反应达到平衡,
反应达到平衡, 的转化率为b%,则比较大小:a%
的转化率为b%,则比较大小:a% ___________ b%。
 和1g
和1g 反应达到平衡,
反应达到平衡, 的转化率为a%,另一同温同容的B容器中加入2g
的转化率为a%,另一同温同容的B容器中加入2g 和2g
和2g 反应达到平衡,
反应达到平衡, 的转化率为b%,则比较大小:a%
的转化率为b%,则比较大小:a%
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Ⅰ:如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:
2A(g)+B(g) 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
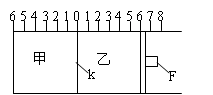
(1)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是___________ 。
(2)若达到平衡时,隔板K最终停留在左侧刻度1处,此时甲容积为2L,反应化学平衡常数为___________ 。
(3)若达到平衡时,隔板K最终停留在左侧刻度靠近0处, 则乙中可移动活塞F最终停留在右侧的刻度不大于________ ;
Ⅱ:若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(4)测得甲中A的转化率为b,则乙中C的转化率为________ ;
(5)假设乙、甲两容器中的压强比用d表示,则d的取值范围是______________ 。
2A(g)+B(g)
 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
(1)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是
(2)若达到平衡时,隔板K最终停留在左侧刻度1处,此时甲容积为2L,反应化学平衡常数为
(3)若达到平衡时,隔板K最终停留在左侧刻度靠近0处, 则乙中可移动活塞F最终停留在右侧的刻度不大于
Ⅱ:若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(4)测得甲中A的转化率为b,则乙中C的转化率为
(5)假设乙、甲两容器中的压强比用d表示,则d的取值范围是
您最近一年使用:0次
【推荐3】氨的合成是最重要的化工生产之一。
已知: N2(g)+ 3H2(g) 2NH3(g) △H =-92.4 kJ/mol
2NH3(g) △H =-92.4 kJ/mol
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始温度和容积相同,相关数据如下表所示:
则平衡时容器的体积V甲_____ V丙, 平衡常数K丙_______ K乙(填>、<或=)。
已知: N2(g)+ 3H2(g)
 2NH3(g) △H =-92.4 kJ/mol
2NH3(g) △H =-92.4 kJ/mol在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始温度和容积相同,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1 mol N2、3 molH2 | 2 mol NH3 | 2 mol NH3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
则平衡时容器的体积V甲
您最近一年使用:0次