AgBr具有感光性,能用来制做感光材料,其在水溶液中存在沉淀溶解平衡,下列关于该溶液中离子浓度变化曲线说法不正确的是
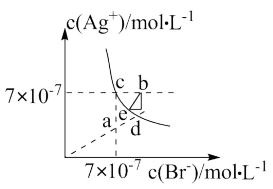

| A.a点为不饱和溶液,恒温蒸发后,由a点到d点 |
| B.向c点溶液中加入NaBr固体,将由c点到e点再到d点 |
| C.b点是该温度下的过饱和溶液,析出结晶时将沿45度角回到此曲线上的e点 |
| D.向d点饱和溶液中加入Na2S固体,将由d点到e点再到c点 |
更新时间:2021/12/05 08:11:18
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某温度下,CuS和 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中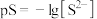 ,
,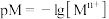 ,
, 为
为 或
或 ,下列说法正确的是
,下列说法正确的是
 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中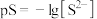 ,
,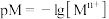 ,
, 为
为 或
或 ,下列说法正确的是
,下列说法正确的是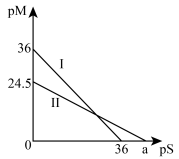
| A.a=48 |
| B.曲线Ⅱ代表的是CuS |
C.此温度下 的 的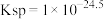 |
D.在同浓度的 和 和 混合溶液中滴加 混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
您最近一年使用:0次
【推荐2】常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L 悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是


| A.常温下,Ksp(BaSO4)=2.5×10-9 |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
| C.若要使BaSO4全部转化为BaCO3至少要加入0.65mol Na2CO3 |
D.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小关系为:c( )>c( )>c( )>c(Ba2+)>c(OH-) )>c(Ba2+)>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
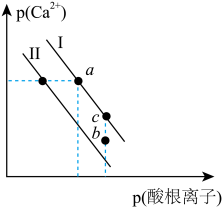
【推荐1】常温时,碳酸钙和硫酸钙的沉淀溶解平衡关系如图所示,已知 ,
, (酸根离子)
(酸根离子) (酸根离子)。下列说法
(酸根离子)。下列说法不正确 的是
 ,
, (酸根离子)
(酸根离子) (酸根离子)。下列说法
(酸根离子)。下列说法
A.曲线Ⅱ为 沉淀溶解曲线 沉淀溶解曲线 |
| B.加入适量的氯化钙固体,可使溶液由c点变到a点 |
| C.b点对应的硫酸钙溶液不饱和 |
D.向碳酸钙饱和溶液中通入 气体,溶液中 气体,溶液中 不变 不变 |
您最近一年使用:0次
【推荐2】 时,用
时,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为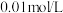 的
的 溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述不正确 的是

 时,用
时,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为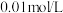 的
的 溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
A.a点对 或 或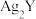 都是过饱和溶液 都是过饱和溶液 |
B.向b点的溶液中加入少量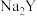 固体,b点可变到c点 固体,b点可变到c点 |
C. 时, 时,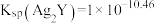 |
D.向 的混合液中滴入 的混合液中滴入 溶液时, 溶液时, 先沉淀 先沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
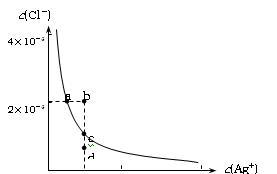
【推荐3】某温度时,AgCl在水中的沉淀溶解平衡曲线如图所示(提示:AgCl(s) Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
 Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
| A.加入NaCl可以使溶液由a点变到b点 |
| B.b点和d点均无AgCl沉淀生成 |
| C.a点对应的Ksp大于c点对应的Ksp |
D.向0.1mol/L的硝酸银溶液中滴加0.1mol/L的NaCl溶液至不再有白色沉淀生成,再向其中滴加0.1mol/L的Na2S溶液,白色沉淀转化为黑色沉淀。其沉淀转化的反应方程式为:2AgCl(s)+S2-(aq) Ag2S(s)+2Cl-(aq) 。 Ag2S(s)+2Cl-(aq) 。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法中不正确 的是


A.图中各点对应的 即的关系为: 即的关系为: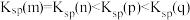 |
B.向m点的溶液中加入少量 固体,溶液组成由m沿mpn线向p方向移动 固体,溶液组成由m沿mpn线向p方向移动 |
| C.图中a和b可分别表示T1、T2温度下CdS在水中的溶解能力 |
| D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】当氢氧化镁固体在水中达到溶解平衡 Mg(OH)2(s) Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
 Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使固体的量减少,可加入少量的| A.NH3 ·H2O | B.NaOH | C.MgSO4 | D.NaHSO4 |
您最近一年使用:0次

 以及铁、铝、硅的氧化物)制备
以及铁、铝、硅的氧化物)制备 的工艺流程如下:
的工艺流程如下: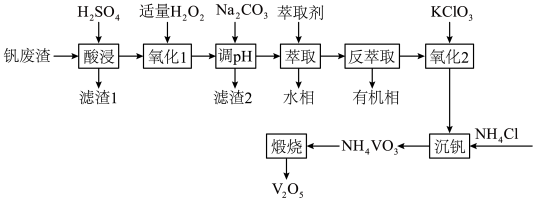
 的形式存在;过量
的形式存在;过量 可氧化
可氧化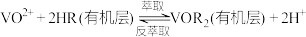 ;
; 与
与 可相互转化:
可相互转化: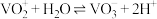 。
。 和
和
 调节溶液的酸碱性
调节溶液的酸碱性

