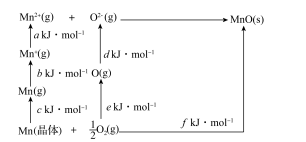
电动汽车、燃料电池汽车等逐步进入人们的生活,其中钴酸锂、锰酸锂、磷酸铁锂电池是目前主流的锂离子电池。
(1)①写出基态 原子的价层电子表示式
原子的价层电子表示式___________ 。 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
②比较第四电离能大小
___________ 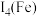 (填“>”“<”或“=”)。(原子序数
(填“>”“<”或“=”)。(原子序数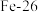
 )
)
(2)某公司研发的甲醇汽车,是利用甲醇 ——空气燃料电池,其工作原理如图:
——空气燃料电池,其工作原理如图:
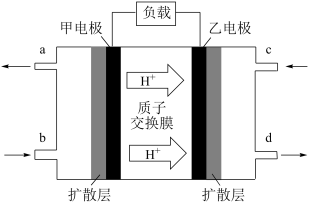
①图中甲电极为___________ (填“负极”、“正极”),乙电极的电极反应式为:___________ 。
②标准状况下,通入 甲醇(
甲醇( 其中C的化合价为
其中C的化合价为 )蒸汽,测得电路中转移
)蒸汽,测得电路中转移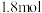 电子,则甲醇的利用率为
电子,则甲醇的利用率为___________ 。
(1)①写出基态
 原子的价层电子表示式
原子的价层电子表示式 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为②比较第四电离能大小

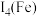 (填“>”“<”或“=”)。(原子序数
(填“>”“<”或“=”)。(原子序数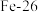
 )
)(2)某公司研发的甲醇汽车,是利用甲醇
 ——空气燃料电池,其工作原理如图:
——空气燃料电池,其工作原理如图:
①图中甲电极为
②标准状况下,通入
 甲醇(
甲醇( 其中C的化合价为
其中C的化合价为 )蒸汽,测得电路中转移
)蒸汽,测得电路中转移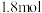 电子,则甲醇的利用率为
电子,则甲醇的利用率为
更新时间:2022/01/20 09:48:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g) CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________ (填序号)。
a. 恒温、恒容条件下,容器内的压强不发生变化
b. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c. 一定条件下,CO、H2和CH3OH的浓度保持不变
d. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
① 该反应的焓变ΔH____________ 0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________ K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________ 。
a. 升高温度
c. 使用合适的催化剂
d. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如图所示。
①请写出c口通入的物质发生的相应电极反应式_____________________________ 。
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________ NA个电子转移。
(4)以上述电池做电源,用上图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用相关的电极反应式和离子方程式表示):
_________________________________________________ 。
CO(g)+2H2(g)
 CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。(1)下列各项中,不能够说明该反应已达到平衡的是
a. 恒温、恒容条件下,容器内的压强不发生变化
b. 一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c. 一定条件下,CO、H2和CH3OH的浓度保持不变
d. 一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH
② T1和T2温度下的平衡常数大小关系是K1
③ 若容器容积不变,下列措施可增加甲醇产率的是
a. 升高温度
b. 将CH3OH(g)从体系中分离
c. 使用合适的催化剂
d. 充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如图所示。

①请写出c口通入的物质发生的相应电极反应式
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有

(4)以上述电池做电源,用上图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用相关的电极反应式和离子方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.完成下列问题
(1)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应为:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其正极电极反应式为___________ 。
(2)甲醇(CH3OH)燃料电池碱性电解质条件下的负极电极反应式___________ 。
Ⅱ.根据铅蓄电池放电时的工作原理,用物质的量浓度为 5.2mol/L,体积为1L的硫酸作电解质溶液,(假设反应前后溶液体积变化忽略不计)组装成原电池如图所示。
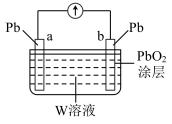
(3)在 a 电极上发生的反应可表示为___________ 。
(4)若电池工作一段时间后,a 极消耗 0.05molPb,b电极的质量变化为___________ g,则此时W溶液的浓度为___________ mol/L。
(1)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应为:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其正极电极反应式为
(2)甲醇(CH3OH)燃料电池碱性电解质条件下的负极电极反应式
Ⅱ.根据铅蓄电池放电时的工作原理,用物质的量浓度为 5.2mol/L,体积为1L的硫酸作电解质溶液,(假设反应前后溶液体积变化忽略不计)组装成原电池如图所示。

(3)在 a 电极上发生的反应可表示为
(4)若电池工作一段时间后,a 极消耗 0.05molPb,b电极的质量变化为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月。下图是一个电化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O

请填空:
(1)放电时:负极的电极反应式为_____________________________________________ 。
(2)充电时:①原电池的负极与电源_________ 极相连。
②阳极的电极反应为__________________ 。
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2_________ L(标准状况下)。
 2K2CO3+6H2O
2K2CO3+6H2O
请填空:
(1)放电时:负极的电极反应式为
(2)充电时:①原电池的负极与电源
②阳极的电极反应为
(3)在此过程中若完全反应,乙池中B极的质量升高648g,则甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)①元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为___________ nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
②基态K原子中,核外电子占据最高能层的符号是___________ ,占据该能层电子的电子云轮廓图形状为___________ 。
(2)①氮原子价层电子的轨道表达式(电子排布图)为___________ 。
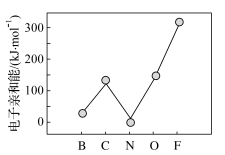
②元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________ ;氮元素的E1呈现异常的原因是___________
(3)①Fe3+基态核外电子排布式为___________
②C、H、O三种元素的电负性由小到大的顺序为___________ 。
(1)①元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
②基态K原子中,核外电子占据最高能层的符号是
(2)①氮原子价层电子的轨道表达式(电子排布图)为
②元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是

(3)①Fe3+基态核外电子排布式为
②C、H、O三种元素的电负性由小到大的顺序为
您最近一年使用:0次
【推荐2】生活污水中氮是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180mg/L。
(1)写出NH4Cl电子式:___ 。
(2)氮原子的电子排布式是:___ ,写出与氯同周期,有2个未成对电子的原子的元素符号为___ 、___ 。
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为___ L(计算结果保留两位小数)。
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目___ 。
___ Fe+___ NO3-+___ H+→___ Fe2++___ NH4++___ H2O
(1)写出NH4Cl电子式:
(2)氮原子的电子排布式是:
(3)为除去废水中的NH4+,向103L该污水中加入0.1mol/LNaOH溶液,理论上需要NaOH溶液的体积为
(4)可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】N元素能形成多种化合物,它们之间可以发生相互转化,如: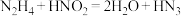 。请回答下列问题:
。请回答下列问题:
(1)N与O的第一电离能较小的是___________ 。
(2)N的基态原子的电子排布中,有___________ 个运动状态不同的未成对电子。
(3)叠氮酸 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是___________ 。
(4) 中N原子的杂化类型是
中N原子的杂化类型是___________ 。
(5)① 是一种很好的配体,则能提供孤电子对的
是一种很好的配体,则能提供孤电子对的___________ (填字母)。
A.仅有氧原子
B.仅有氮原子
C.是氧原子或氮原子
② 与钴盐通过配位键形成的
与钴盐通过配位键形成的 能与
能与 结合生成黄色
结合生成黄色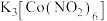 沉淀,此方法可用于检验溶液中的
沉淀,此方法可用于检验溶液中的 ,写出该配合物中钴离子的电子排布式:
,写出该配合物中钴离子的电子排布式:___________ 。
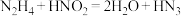 。请回答下列问题:
。请回答下列问题:(1)N与O的第一电离能较小的是
(2)N的基态原子的电子排布中,有
(3)叠氮酸
 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是(4)
 中N原子的杂化类型是
中N原子的杂化类型是(5)①
 是一种很好的配体,则能提供孤电子对的
是一种很好的配体,则能提供孤电子对的A.仅有氧原子
B.仅有氮原子
C.是氧原子或氮原子
②
 与钴盐通过配位键形成的
与钴盐通过配位键形成的 能与
能与 结合生成黄色
结合生成黄色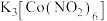 沉淀,此方法可用于检验溶液中的
沉淀,此方法可用于检验溶液中的 ,写出该配合物中钴离子的电子排布式:
,写出该配合物中钴离子的电子排布式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为周期表中部分元素某种性质(X值)随原子序数变化的关系。___ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是___ ;同周期内,随着原子序数的增大,X值的变化总趋势是___ 。周期表中X值的这种变化特点体现了元素性质的___ 变化规律。
(3)X值较小的元素集中在元素周期表的___ (填序号,下同)。
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是___ 。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱

(2)同主族内不同元素的X值变化的特点是
(3)X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为  。
。
(1)“中国蓝”“中国紫”中均有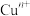 离子,
离子,
___________ ,基态时该阳离子的价电子排布式为___________ 。
(2)与铜元素位于同一周期的元素中,基态原子的未成对电子数最多的元素为___________ 。
(3)已知 的第二电离能分别为
的第二电离能分别为 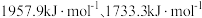 ,前者高于后者的原因是
,前者高于后者的原因是___________ 。
(4)铜常用作有机反应的催化剂。例如,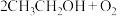
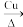
 。
。
①乙醇的沸点高于乙醛,其主要原因是___________ ;乙醛分子中  键与
键与  键的个数比为
键的个数比为___________ 。
②乙醛分子中碳原子的杂化轨道类型是___________ 。
 。
。(1)“中国蓝”“中国紫”中均有
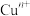 离子,
离子,
(2)与铜元素位于同一周期的元素中,基态原子的未成对电子数最多的元素为
(3)已知
 的第二电离能分别为
的第二电离能分别为 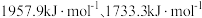 ,前者高于后者的原因是
,前者高于后者的原因是(4)铜常用作有机反应的催化剂。例如,
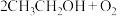
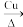
 。
。①乙醇的沸点高于乙醛,其主要原因是
 键与
键与  键的个数比为
键的个数比为②乙醛分子中碳原子的杂化轨道类型是
您最近一年使用:0次