题型:解答题-结构与性质
难度:0.65
引用次数:423
题号:15262921
硫氰酸甲基铵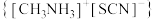 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(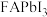 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物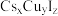 。请回答下列问题:
。请回答下列问题:
(1)基态Cu原子的电子排布式为_______ 。基态I原子的价电子排布图为_______ 。
(2)硫氰酸甲基铵所含元素中第一电离能最大的是_______ (填元素符号)。
(3)Cs、Cu、I的电负性由大到小的顺序是_______ 。
(4)甲脒( )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是_______ 。甲脒中碳原子的杂化方式为_______ 。
(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。_______ 。
②该络合物分子内不存在的微粒间作用力有_______ (填标号)。
a. 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键
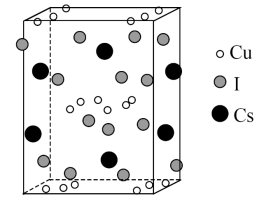
(6)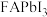 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为_______ 。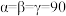 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为_______  。
。
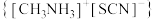 用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(
用于抗生素的分离、分析农药含量、硫氰酸络盐的合成以及用作聚合催化剂。通过气相辅助生长技术,利用硫氰酸甲基铵可制得钙钛矿型甲脒铅碘(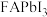 )和一种新型光电材料铯铜卤化物
)和一种新型光电材料铯铜卤化物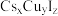 。请回答下列问题:
。请回答下列问题:(1)基态Cu原子的电子排布式为
(2)硫氰酸甲基铵所含元素中第一电离能最大的是
(3)Cs、Cu、I的电负性由大到小的顺序是
(4)甲脒(
 )与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是
)与丙烷的相对分子质量相同,但甲脒的熔点比丙烷的熔点高得多,其原因是(5)水中铅的测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(结构如图)。
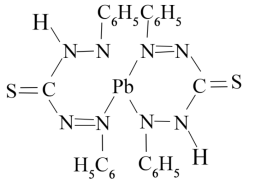
②该络合物分子内不存在的微粒间作用力有
a.
 键 b.
键 b. 键 c.非极性键 d.离子键 e.配位键
键 c.非极性键 d.离子键 e.配位键(6)
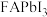 的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为
的晶体结构单元如图所示,图中X表示FA,Y表示Pb,位于八面体中心,则X的碘配位数为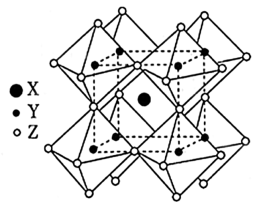
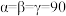 °,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为
°,晶胞的棱上有8个Cu原子,面上有8个Cu原子、4个Cs原子和4个I原子,其余原子均位于体内,该晶体的密度为 。
。
更新时间:2022/03/08 20:38:41
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有四种短周期元素,它们的结构、性质等信息如下表所述,请根据表中信息填写:
(1)A原子的核外电子排布式___________ 。
(2)离子半径:B___________ A(填“大于”或“小于”)。
(3)C原子的外围电子轨道式___________ ,其原子核外有 ___________ 个未成对电子,能量最高的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(4)D原子占据最高能层符号为___________ ,能量不同的电子数为___________ ,空间运动状态不同电子数为___________ ,运动状态不同电子数为___________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(2)离子半径:B
(3)C原子的外围电子轨道式
(4)D原子占据最高能层符号为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。
(1)e和f的I1大小关系是___________>___________(填元素符号,下同) ___________ ,理由是___________
(2)上述元素中,原子中未成对电子数最多的是___________ ,写出该元素基态原子的核外电子排布式:___________ 。
(3)X、Y是上述a—j中的两种元素,根据下表所提供的电离能数据,回答下列问题:
①X的元素符号是___________ ,X和c 以原子个数之比1:1形成的一种化合物的电子式是___________
②Y与h形成的化合物是___________ (填“共价化合物”或“离子化合物”)
| a | |||||||||||||||||
| b | c | ||||||||||||||||
| d | e | f | g | h | |||||||||||||
| i | j |
(2)上述元素中,原子中未成对电子数最多的是
(3)X、Y是上述a—j中的两种元素,根据下表所提供的电离能数据,回答下列问题:
| 锂 | X | Y | |
| I1 | 520 | 496 | 580 |
| I2 | 7296 | 4570 | 1820 |
| I3 | 11799 | 6920 | 2750 |
| I4 | 9550 | 11600 |
②Y与h形成的化合物是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(一)Na、Cu、O、Si、S、Cl是常见的六种元素.
(1)Na位于元素周期表第__ 周期第__ 族;S的基态原子核外有__ 个未成对电子;
Si的基态原子核外电子排布式为__ .
(2)用“>”或“<”填空:
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取。写出该反应的离子方程式,并标出电子转移的方向和数目___
(二).某元素的原子序数为33,请回答:
(1)该元素原子核外有_______ 个电子层,______ 个能级,______ 个原子轨道。
(2)它的最外层电子排布式为____________ ,它的电子排布式为________ ,轨道表示式为_______________ 。
(1)Na位于元素周期表第
Si的基态原子核外电子排布式为
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |
(二).某元素的原子序数为33,请回答:
(1)该元素原子核外有
(2)它的最外层电子排布式为
您最近一年使用:0次
【推荐1】碳族元素及其化合物有及其重要的应用。请回答:
(1)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,有关这些微粒的叙述,正确的是___________。
(2)Ge与C是同族元素,在电子、材料等领域应用广泛。
①基态Ge原子的核外价层电子的轨道表示式为___________
②C原子间可以形成双键、三键,但Ge原子之间难以形成双键或三键。原因是___________ 。
(3)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],下列说法不正确 的是___________
(4)有以下几种羧酸:①丙酸(C2H5COOH)②三氯乙酸(CCl3COOH)③氯乙酸(CH2ClCOOH)④三氟乙酸(CF3COOH)⑤乙酸(CH3COOH)。这些羧酸的pKa(pKa=-lgKa)由大到小的顺序是___________
(5)甲醇(CH3OH)的沸点64.7℃,介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(1)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,有关这些微粒的叙述,正确的是___________。
| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.得电子能力:①>② |
| D.电离一个电子所需最低能量:①>②>③ |
①基态Ge原子的核外价层电子的轨道表示式为
②C原子间可以形成双键、三键,但Ge原子之间难以形成双键或三键。原因是
(3)Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],下列说法
| A.CH3CN与Mn原子配位时,提供孤电子对的是C原子 |
| B.电负性:H<C<N<O |
| C.CH3CN中两个C原子的杂化类型均为sp3 |
| D.CH3CN中σ键与π键数目之比为5:2 |
(5)甲醇(CH3OH)的沸点64.7℃,介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Cu是一种重要的金属元素,许多铜的化合物在医药、工农业生产中有重要作用。回答下列问题:
(1)基态Cu原子的价电子排布式为___________ ;比较Cu2+和Zn2+稳定性并分析原因:___________ 。
(2)一种铜的配合物结构如图1所示,其对肿瘤有明显的抑制作用,该配合物中几种非金属元素的电负性由大到小的顺序为___________ ,配位原子的杂化方式为___________ 。

(3)金属铜单独与氨水或过双氧水都不反应,但可与氨气和双氧水的混合溶液反应,其原因___________ 。
(4)NH3分子中H-N-H键角为107° ,在[Cu(NH3)4]2+中的H-N-H键角为109.5° ,键角变大的原因是___________ 。
(5)Cu2O 晶体结构与CsCl (图2)相似,只是利用Cu4O占据CsCl晶体中C1的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有___________ 个 “Cu2O”;Cu2O晶胞中Cu的配位数是___________ ;若①处Cu原子坐标为( ,
, ,
, ),则Cu2O晶胞中Cu4O四面体中O原子坐标为
),则Cu2O晶胞中Cu4O四面体中O原子坐标为___________ 。

(1)基态Cu原子的价电子排布式为
(2)一种铜的配合物结构如图1所示,其对肿瘤有明显的抑制作用,该配合物中几种非金属元素的电负性由大到小的顺序为

(3)金属铜单独与氨水或过双氧水都不反应,但可与氨气和双氧水的混合溶液反应,其原因
(4)NH3分子中H-N-H键角为107° ,在[Cu(NH3)4]2+中的H-N-H键角为109.5° ,键角变大的原因是
(5)Cu2O 晶体结构与CsCl (图2)相似,只是利用Cu4O占据CsCl晶体中C1的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有
 ,
, ,
, ),则Cu2O晶胞中Cu4O四面体中O原子坐标为
),则Cu2O晶胞中Cu4O四面体中O原子坐标为
您最近一年使用:0次
【推荐3】原子是肉眼和一般仪器都看不到的微粒,科学家们是根据可观察、可测量的宏观实验事实,经过分析和推理,揭示了原子结构的奥秘。
(1)下列说法中正确的个数是__________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
⑤基态碳原子的轨道表示式: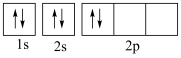
⑥ⅢB族到ⅡB族的10个纵列的元素都是金属元素
⑦用电子式表示 的形成过程:
的形成过程: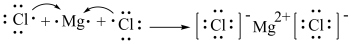
⑧基态钒原子的结构示意图为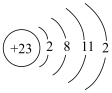
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为__________ 、__________ 。
A.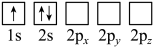 B.
B.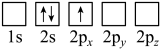
C.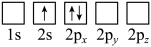 D.
D.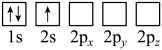
(3)研究发现,正离子的颜色与未成对电子数有关,例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是__________ (从微粒结构的角度进行描述)。
(4)钠在火焰上灼烧产生的黄光是一种原子__________ 光谱(选填“发射”或“吸收”)。
(5)第四周期的元素形成的化合物在生产生活中有着重要的用途。
①镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为__________ ,按照电子排布式,镍元素在周期表中位于__________ 区。
②“玉兔二号”月球车通过砷化镓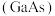 太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为__________ 形。砷的电负性比镓__________ (填“大”或“小”)。
(6)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期的几种元素的部分性质:
①预测x值的区间:______ ~______ 。
②表中五种元素的第一电离能由大到小的顺序是__________ (写元素符号)。
(1)下列说法中正确的个数是__________。
①同一原子中,s电子的能量总是低于p电子的能量
②任何s轨道形状均是球形,只是能层不同,球的半径大小不同而己
③2p、3p、4p能级的轨道数依次增多
④原子核外电子排布,先排满K层再排L层,排满M层再排N层
⑤基态碳原子的轨道表示式:

⑥ⅢB族到ⅡB族的10个纵列的元素都是金属元素
⑦用电子式表示
 的形成过程:
的形成过程:
⑧基态钒原子的结构示意图为

| A.2 | B.3 | C.4 | D.5 |
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(3)研究发现,正离子的颜色与未成对电子数有关,例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是(4)钠在火焰上灼烧产生的黄光是一种原子
(5)第四周期的元素形成的化合物在生产生活中有着重要的用途。
①镍铬钢抗腐蚀性能强,基态铬原子的价电子排布式为
②“玉兔二号”月球车通过砷化镓
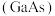 太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为
太阳能电池提供能量进行工作。基态砷原子的电子占据最高能级的电子云轮廓图为(6)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期的几种元素的部分性质:
元素编号 | a | b | c | d | e |
电负性 | 3.0 | 2.5 | x | 1.5 | 0.9 |
主要化合价 |
|
|
|
|
|
②表中五种元素的第一电离能由大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】(1)基态铜原子的电子排布式为_____ ;价电子中成对电子数有_____ 个。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是_____ 。
②P 与 N 同主族,其最高价氧化物对应水化物的酸性:HNO3_____ H3PO4(填“>”或“<”),
(3)某磷青铜晶胞结构如下图所示。
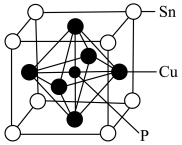
①则其化学式为_____ 。
②该晶体中距离 Cu 原子最近的 Sn 原子有_____ 个,这些 Sn 原子所呈现的构型为_____ 。
③若晶体密度为 8.82 g/cm3,最近的 Cu 原子核间距为_____ pm(用含 NA的代数式表示)。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是
②P 与 N 同主族,其最高价氧化物对应水化物的酸性:HNO3
(3)某磷青铜晶胞结构如下图所示。

①则其化学式为
②该晶体中距离 Cu 原子最近的 Sn 原子有
③若晶体密度为 8.82 g/cm3,最近的 Cu 原子核间距为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钴的化合物在工业生产、生命科技等行业有重要应用。
(1)基态钴原子的价电子排布式为____ ,Co的第四电离能比Fe的第四电离能要小得多,原因是____ 。Co与Ca属于同一周期,且最外层电子数相同,但金属Co的熔点、沸点均比金属Ca的高,原因是____ 。
(2)以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构简式如图所示。

①该多齿配体中所含元素(除氢以外)第一电离能由大到小的顺序为____ (填元素符号)。
②下列化合物与上述配合物中C和N原子的杂化类型均相同的是____ (填标号)。
A.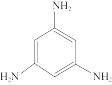 B.
B.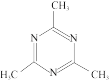 C.
C.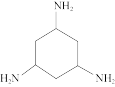 D.
D.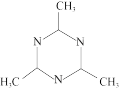
(3)[Co(NO3)4]2-中Co2+的配位数为4,1mol该配离子中含σ键数目为____ NA,配体中与钴进行配位的原子是____ ,原因是____ 。
(4)稀土钴系(Sm—Co)永磁合金的六方晶胞结构如图所示(晶体结构可看成如图(a)、(b)两种原子层交替堆积排列而成图(c))。已知同一原子层的Sm—Sm的最近距离为apm,不同原子层间的Sm—Sm最近距离为bpm。
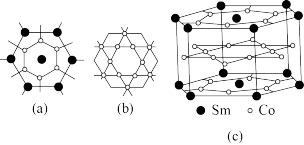
①Sm—Co永磁合金的化学式为____ 。
②已知阿伏加德罗常数的值为NA,则该合金的密度ρ为____ g·cm-3。(只要求列出计算式)
(1)基态钴原子的价电子排布式为
(2)以无水乙醇作溶剂,Co(NO3)2可与某多齿配体结合形成具有催化活性的配合物,其结构简式如图所示。

①该多齿配体中所含元素(除氢以外)第一电离能由大到小的顺序为
②下列化合物与上述配合物中C和N原子的杂化类型均相同的是
A.
 B.
B. C.
C. D.
D.
(3)[Co(NO3)4]2-中Co2+的配位数为4,1mol该配离子中含σ键数目为
(4)稀土钴系(Sm—Co)永磁合金的六方晶胞结构如图所示(晶体结构可看成如图(a)、(b)两种原子层交替堆积排列而成图(c))。已知同一原子层的Sm—Sm的最近距离为apm,不同原子层间的Sm—Sm最近距离为bpm。
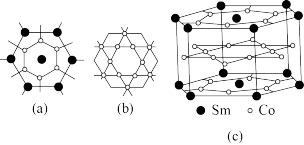
①Sm—Co永磁合金的化学式为
②已知阿伏加德罗常数的值为NA,则该合金的密度ρ为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种用硫铜矿(主要含CuS、 及少量FeO、
及少量FeO、 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下: ;
;
②CuCl在潮湿的空气中易被氧化,生成的碱式盐为 ;
;
③已知 、
、 、
、 开始生成沉淀和沉淀完全时的pH如下表:
开始生成沉淀和沉淀完全时的pH如下表:
回答下列问题:
(1)“酸浸”时,富氧空气的作用_______ 。
(2)“酸浸”时,CuS反应的化学方程式为_______ 。
(3)用氨水调pH时,应将溶液的范围调整为_______ 。
(4)“合成”时, 生成CuCl发生反应的离子方程式为
生成CuCl发生反应的离子方程式为_______ 。
(5)准确称取所制备的氯化亚铜样品m g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,用x mol⋅L
溶液中,待样品完全溶解后,加入适量稀硫酸,用x mol⋅L 的
的 溶液滴定到终点,发生反应为
溶液滴定到终点,发生反应为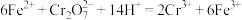
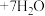 ,消耗
,消耗 溶液V mL,样品中CuCl的质量分数为
溶液V mL,样品中CuCl的质量分数为_______ (杂质不参与反应,列出计算式即可)。
(6)如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a nm。 ,B为
,B为 ,则C的坐标参数为
,则C的坐标参数为_______ 。
② 与
与 最短的距离是
最短的距离是_______ nm。
 及少量FeO、
及少量FeO、 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下: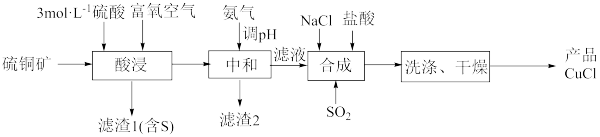
 ;
;②CuCl在潮湿的空气中易被氧化,生成的碱式盐为
 ;
;③已知
 、
、 、
、 开始生成沉淀和沉淀完全时的pH如下表:
开始生成沉淀和沉淀完全时的pH如下表:| 金属离子 |  |  |  |
| 开始沉淀pH | 4.7 | 8.1 | 1.2 |
| 完全沉淀pH | 6.7 | 9.6 | 3.2 |
(1)“酸浸”时,富氧空气的作用
(2)“酸浸”时,CuS反应的化学方程式为
(3)用氨水调pH时,应将溶液的范围调整为
(4)“合成”时,
 生成CuCl发生反应的离子方程式为
生成CuCl发生反应的离子方程式为(5)准确称取所制备的氯化亚铜样品m g,将其置于过量的
 溶液中,待样品完全溶解后,加入适量稀硫酸,用x mol⋅L
溶液中,待样品完全溶解后,加入适量稀硫酸,用x mol⋅L 的
的 溶液滴定到终点,发生反应为
溶液滴定到终点,发生反应为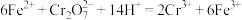
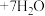 ,消耗
,消耗 溶液V mL,样品中CuCl的质量分数为
溶液V mL,样品中CuCl的质量分数为(6)如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a nm。
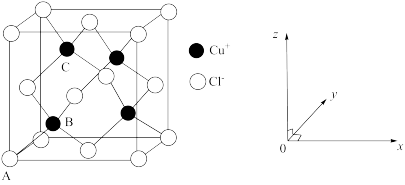
 ,B为
,B为 ,则C的坐标参数为
,则C的坐标参数为②
 与
与 最短的距离是
最短的距离是
您最近一年使用:0次

 ,
,
 ,
,
 ,
,




