A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A的一种核素的原子核内无中子,B的一种核素被考古学家用于测定文物的年代,D原子的最外层电子数比次外层多4,D的阴离子与E的阳离子具有相同的电子排布,两元素可形成化合物E2D,D、F同主族。用化学用语回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)G的离子结构示意图为___________ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为___________ 。
(4)由A、C、D三元素按原子个数4:2:3之比形成物质的化学式为___________ ,其中所含化学键的类型有___________ 。
(5)B、D、F可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为___________ 。
(6)下列实验操作对应的实验现象中,不正确的是___________ 。
(1)D在元素周期表中的位置为
(2)G的离子结构示意图为
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为
(4)由A、C、D三元素按原子个数4:2:3之比形成物质的化学式为
(5)B、D、F可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为
(6)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| A | 将E单质投入到 溶液中 溶液中 | 有红色固体析出 |
| B | 向 溶液中通入过量C的气态氢化物 溶液中通入过量C的气态氢化物 | 先产生白色沉淀,后沉淀溶解 |
| C | 将G的单质通入到 溶液中充分反应后,加入四氯化碳,振荡,静置 溶液中充分反应后,加入四氯化碳,振荡,静置 | 下层溶液变为橙色 |
| D | 过量B的最高价氧化物通入到饱和 溶液中 溶液中 | 有白色晶体析出 |
更新时间:2022/04/23 15:44:01
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学在探究废干电池内的黑色固体回收利用时,进行如图示实验:
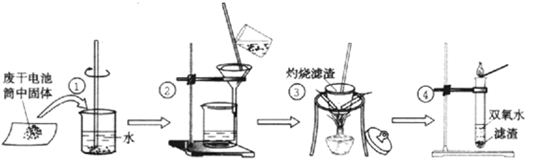
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、三角架、________ 、________ ;
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气
体,据此可初步认定黑色固体为________ 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测
滤渣中还存在的物质为________ 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
(5)根据以上的实验报告,关于滤液的成分,你的结论是:________ 。通过一定的操作从滤液中得到固体溶质, 若要将所得固体溶质中的物质加以分离,可用________ 法。

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、三角架、
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气
体,据此可初步认定黑色固体为
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测
滤渣中还存在的物质为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1、检验Cl— | 取少许滤液于试管中,加入 | 含有Cl— | |
| 2、检验NH4+ | 取少许滤液于试管中,加入 | 含有NH4+ | |
| 3、检验Zn2+ | 取少许滤液于试管中,加入 稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
(5)根据以上的实验报告,关于滤液的成分,你的结论是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图中A~J分别代表相关反应的一种物质。已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。请填写以下空白:
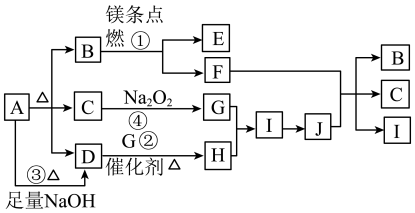
(1)A中含有的化学键是________ 。
(2)写出铜与J反应制取H的化学方程式:__________________________________________ 。
(3)写出反应③的离子方程式:_________________________________________ 。
(4)写出物质B的电子式:_______________ ;写出物质E的电子式:_______________ 。
(5)在反应④中,当生成标况下22.4 L 物质G时,转移电子数为________ mol。

(1)A中含有的化学键是
(2)写出铜与J反应制取H的化学方程式:
(3)写出反应③的离子方程式:
(4)写出物质B的电子式:
(5)在反应④中,当生成标况下22.4 L 物质G时,转移电子数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
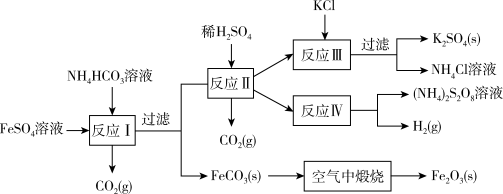
(1)反应Ⅰ前需在 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;
(2)反应Ⅰ需控制反应温度低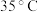 ,其目的是
,其目的是___________ 。
(3)反应Ⅳ常被用于电解生产 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为___________ 。
(4)反应Ⅰ的离子方程式为___________ 。
(5)空气中煅烧的化学方程式为___________ 。

(1)反应Ⅰ前需在
 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;| A.锌粉 | B.铁屑 | C. 溶液 溶液 | D. |
(2)反应Ⅰ需控制反应温度低
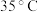 ,其目的是
,其目的是(3)反应Ⅳ常被用于电解生产
 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为(4)反应Ⅰ的离子方程式为
(5)空气中煅烧的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以废旧催化剂(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
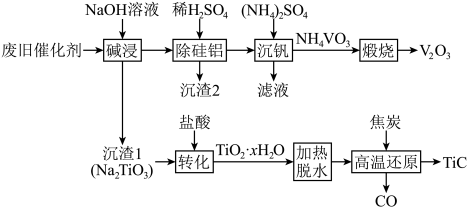
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是_______ (填化学式),实验室中将“沉渣1”从“碱浸”所得的悬浊液中分离出来所需玻璃仪器的名称为_______ 。
(2)“沉渣2”中含有两种成分,它们的化学式为_______ 。
(3)“转化”时发生反应的化学方程式为_______ 。
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为_______ 。
(5)“高温还原”时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,若生成30g还原产物,则转移电子的物质的量为_______ 。
 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是
(2)“沉渣2”中含有两种成分,它们的化学式为
(3)“转化”时发生反应的化学方程式为
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为
(5)“高温还原”时
 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
【推荐2】氮和砷(As)都是第VA族元素,运用相关知识回答以下问题:
(1)已知:①2O2(g) + N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=______ ,联氨和N2O4可作为火箭推进剂的主要原因为_______ 。
(2)联氨为二元弱碱,在水中的电离方式与氨相似。请写出联氨与硫酸形成的所有盐的化学式_______ 。
(3)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上lkg的联氨可处理_______ L水(假设水中溶解O2量为10mg/L)
(4)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在。雌黄可被浓硝酸氧化为H3AsO4与S,硝酸被还原为NO2,反应中氧化剂与还原剂物质的量之比为____________ 。
(1)已知:①2O2(g) + N2(g)=N2O4(l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=
(2)联氨为二元弱碱,在水中的电离方式与氨相似。请写出联氨与硫酸形成的所有盐的化学式
(3)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上lkg的联氨可处理
(4)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在。雌黄可被浓硝酸氧化为H3AsO4与S,硝酸被还原为NO2,反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的最低负化合价为-2。回答下列问题:
(1)Y-的结构示意图为____________ 。
(2)写出含有10个中子的X原子的原子符号_____________ 。
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目________________ 。
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为___________ 。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为_____________ 。
(6)ZX2与NaOH溶液反应的化学方程式为_____________________ 。
(1)Y-的结构示意图为
(2)写出含有10个中子的X原子的原子符号
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为
(6)ZX2与NaOH溶液反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F为短周期的主族元素,它们的原子序数按A、B、C、D、E、F的顺序增大。A是原子半径最小的原子;B的最外层电子数是次外层电子数的2倍,D与F最外层电子数相等,E与D可形成 、
、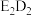 两种离子化合物。填写下列空白:
两种离子化合物。填写下列空白:
(1)C元素在元素周期表中的位置为:___________
(2)C、D、E、F原子半径由小到大的顺序为___________ (用元素符号表示)
(3)A与D形成的含有非极性键的化合物的结构式为___________ ; 的电子式为:
的电子式为:___________ ,EDA中含有的化学键类型为:___________ 。
(4)B单质与F的最高价氧化物对应的水化物的浓溶液反应的化学反应方程式为___________ 。
 、
、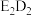 两种离子化合物。填写下列空白:
两种离子化合物。填写下列空白:(1)C元素在元素周期表中的位置为:
(2)C、D、E、F原子半径由小到大的顺序为
(3)A与D形成的含有非极性键的化合物的结构式为
 的电子式为:
的电子式为:(4)B单质与F的最高价氧化物对应的水化物的浓溶液反应的化学反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________ ,碱性最强的化合物的电子式是___________ 。
(2)最高价氧化物是两性氧化物的元素原子结构示意图是___________ ;写出它的氧化物与氢氧化钠反应的离子方程式___________ 。
(3)①与⑦组成的化合物的电子式___________ ,该化合物是由___________ (填“极性”“非极性”)键形成的。
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是___________ (用离子符号表示)。
(5)过量的元素②的氢化物和元素⑦的单质反应的化学方程式___________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)最高价氧化物是两性氧化物的元素原子结构示意图是
(3)①与⑦组成的化合物的电子式
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
(5)过量的元素②的氢化物和元素⑦的单质反应的化学方程式
您最近一年使用:0次
【推荐1】W、X、Y、Z为短周期主族元素,原子序数依次增大。W、X、Y、Z的价电子数之和为10,Z的最外层电子数为其K层的一半,W与Y可形成个数比为2:1的18e-分子。
(1)下列有关叙述正确的是_______ 。
a.ZXW4中含有离子键、配位键和共价键
b.Y的最高化合价氧化物的水化物为弱酸
c.X的氟化物XF3中原子均为8电子稳定结构
(2)①基态Z原子的电子排布式为_______ 。
②基态Z原子电子占据最高能级的电子云为_______ 形。
(3)①W、X、Y中,原子半径最大的是_______ 。(填元素符号,下同)。
②根据对角线规则,X的一些化学性质与元素_______ 的相似。
③在XF3分子中F-X-F的键角是_______ 。
④XF3和过量NaF作用可生成NaXF4, 的立体构型为
的立体构型为_______ 。
⑤路易斯酸碱理论认为,任何可接受电子对的分子或离子叫做路易斯酸,任何可给出电子对的分子或离子叫做路易斯碱。从结构角度分析XF3是路易斯酸的原因:_______ 。
(4)YH3XH3分子中,①Y-X化学键称为_______ 键。
②YH3XH3中X原子的杂化轨道类型为_______ 。
③从原子结构角度解释Y的非金属性强于X的原因:_______ 。
(5)YH3XH3分子中,与Y原子相连的H呈正电性(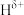 ),与X原子相连的H呈负电性(
),与X原子相连的H呈负电性(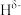 )。
)。
①与YH3XH3原子总数相等的等电子体是_______ (写分子式)。
②该等电子的熔点比YH3XH3的低,其原因是_______ ,也称为二氢键。
(6)研究发现,YH3XH3在低温高条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm, ,YH3XH3的2×2×2超晶胞结构如图所示。
,YH3XH3的2×2×2超晶胞结构如图所示。

YH3XH3晶体的密度ρ=_______ g/cm3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关叙述正确的是
a.ZXW4中含有离子键、配位键和共价键
b.Y的最高化合价氧化物的水化物为弱酸
c.X的氟化物XF3中原子均为8电子稳定结构
(2)①基态Z原子的电子排布式为
②基态Z原子电子占据最高能级的电子云为
(3)①W、X、Y中,原子半径最大的是
②根据对角线规则,X的一些化学性质与元素
③在XF3分子中F-X-F的键角是
④XF3和过量NaF作用可生成NaXF4,
 的立体构型为
的立体构型为⑤路易斯酸碱理论认为,任何可接受电子对的分子或离子叫做路易斯酸,任何可给出电子对的分子或离子叫做路易斯碱。从结构角度分析XF3是路易斯酸的原因:
(4)YH3XH3分子中,①Y-X化学键称为
②YH3XH3中X原子的杂化轨道类型为
③从原子结构角度解释Y的非金属性强于X的原因:
(5)YH3XH3分子中,与Y原子相连的H呈正电性(
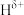 ),与X原子相连的H呈负电性(
),与X原子相连的H呈负电性(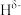 )。
)。①与YH3XH3原子总数相等的等电子体是
②该等电子的熔点比YH3XH3的低,其原因是
(6)研究发现,YH3XH3在低温高条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,
 ,YH3XH3的2×2×2超晶胞结构如图所示。
,YH3XH3的2×2×2超晶胞结构如图所示。
YH3XH3晶体的密度ρ=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)X能形成多种常见单质,在硬度最大的单质中,原子的杂化方式为_______ 。
(2)Z位于元素周期表的位置是___ ,Y的氢化物空间构型是_____ 。
(3)在H-Y、H-Z两种共价键中,键的极性较强的是______ ,X所在周期元素中氢化物最稳定的是______ (用具体元素符号表示)。
(4)下列有关X2H4的说法正确的是_____ 。
A.分子中所有原子都满足8电子稳定结构
B.每个分子中σ键和π键数目之比为4:1
C.它是由极性键和非极性键构成的非极性分子
D.分子的空间构型为直线形
(5)向含有 W2+的溶液中逐滴加入氨水至过量,期间出现的现象是________ ,写出最后所得配离子的结构式,要求标出配位键____ 。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积,其氧化物是形成酸雨的重要原因 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)Z位于元素周期表的位置是
(3)在H-Y、H-Z两种共价键中,键的极性较强的是
(4)下列有关X2H4的说法正确的是
A.分子中所有原子都满足8电子稳定结构
B.每个分子中σ键和π键数目之比为4:1
C.它是由极性键和非极性键构成的非极性分子
D.分子的空间构型为直线形
(5)向含有 W2+的溶液中逐滴加入氨水至过量,期间出现的现象是
您最近一年使用:0次



