三碘化磷( )是易水解的橙红色晶体。研究小组先以海藻为原料制备
)是易水解的橙红色晶体。研究小组先以海藻为原料制备 ,再用
,再用 和红磷(P)在加热条件下直接反应制备
和红磷(P)在加热条件下直接反应制备 ,其主要实验过程及其装置示意图如图所示(夹持装置略)。
,其主要实验过程及其装置示意图如图所示(夹持装置略)。
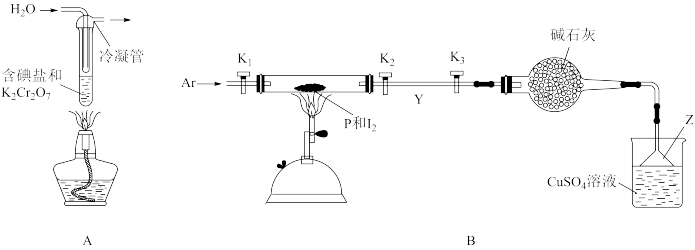
回答下列问题:
(1) 的制备
的制备
①以干燥的海藻为原料制得A装置中所需含碘盐的实验步骤是___________ (按顺序填标号)。
a.海藻灰化 b.干燥称量 c.酸化浸取 d.蒸发结晶
②A装置中含碘盐的主要成分是___________ (填标号)。
a. b.
b.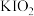 c.
c.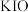 d.
d.
③A装置中 发生反应生成
发生反应生成 ,其化学方程式为
,其化学方程式为___________ 。
④A装置中紫黑色晶体碘的凝结部位是___________ ;
(2)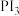 的制备
的制备
①B装置中反应物 和P均需干燥的目的是
和P均需干燥的目的是___________ ;玻璃仪器Z的作用是___________ 。
②B装置中反应前,打开活塞___________ ,通入 气;一段时间后,停止通入
气;一段时间后,停止通入 气,同时关闭活塞
气,同时关闭活塞___________ ,开始加热;反应结束后,停止加热,同时关闭活塞___________ ;冷却后卸下玻璃管Y,在干燥箱中取出产品。
③如果在玻璃管Y外包裹经冷水湿润的毛巾,将对产品的影响是___________ 。
 )是易水解的橙红色晶体。研究小组先以海藻为原料制备
)是易水解的橙红色晶体。研究小组先以海藻为原料制备 ,再用
,再用 和红磷(P)在加热条件下直接反应制备
和红磷(P)在加热条件下直接反应制备 ,其主要实验过程及其装置示意图如图所示(夹持装置略)。
,其主要实验过程及其装置示意图如图所示(夹持装置略)。
回答下列问题:
(1)
 的制备
的制备①以干燥的海藻为原料制得A装置中所需含碘盐的实验步骤是
a.海藻灰化 b.干燥称量 c.酸化浸取 d.蒸发结晶
②A装置中含碘盐的主要成分是
a.
 b.
b.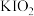 c.
c.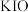 d.
d.
③A装置中
 发生反应生成
发生反应生成 ,其化学方程式为
,其化学方程式为④A装置中紫黑色晶体碘的凝结部位是
(2)
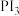 的制备
的制备①B装置中反应物
 和P均需干燥的目的是
和P均需干燥的目的是②B装置中反应前,打开活塞
 气;一段时间后,停止通入
气;一段时间后,停止通入 气,同时关闭活塞
气,同时关闭活塞③如果在玻璃管Y外包裹经冷水湿润的毛巾,将对产品的影响是
更新时间:2022/05/29 14:56:22
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】二氧化碲主要用于制备二氧化碲单晶、红外器件、声光器件红外窗口材料、电子元件材料及防腐剂等。一种从锑铋碲合金粉中制取二氧化碲的工艺流程如下:
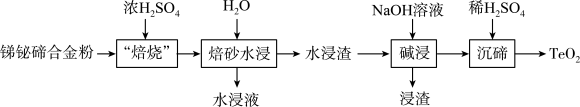
已知: Sb2O3和Bi2O3不能与碱反应,TeO2能与碱反应。
回答下列问题:
(1)TeO2中Te的化合价为______ 。
(2)锑铋碲合金粉在450℃左右加入浓H2SO4“焙烧”时,单质锑、铋和碲分别转化为Sb2O3、Bi2O3和TeO2,其中单质锑转化为Sb2O3的化学方程式为________ 。
(3)碱浸时发生反应的化学方程式为________ ,浸渣的主要成分为_____ 。
(4)沉碲时发生反应的离子方程式为__________ 。
(5)沉碲后经过过滤洗涤、干燥可得TeO2,其中检验TeO2是否洗涤干净的操作为_______ 。

已知: Sb2O3和Bi2O3不能与碱反应,TeO2能与碱反应。
回答下列问题:
(1)TeO2中Te的化合价为
(2)锑铋碲合金粉在450℃左右加入浓H2SO4“焙烧”时,单质锑、铋和碲分别转化为Sb2O3、Bi2O3和TeO2,其中单质锑转化为Sb2O3的化学方程式为
(3)碱浸时发生反应的化学方程式为
(4)沉碲时发生反应的离子方程式为
(5)沉碲后经过过滤洗涤、干燥可得TeO2,其中检验TeO2是否洗涤干净的操作为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料合成新型的环保催化剂(OMS-2)的工艺流程如图:
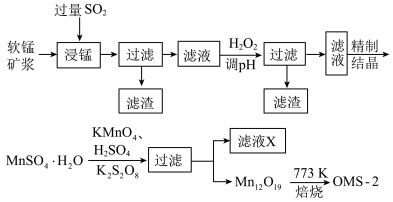
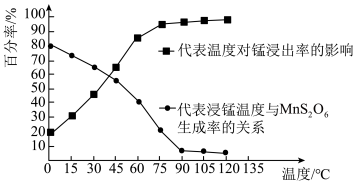
(1)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是_____ ;调pH后再过滤主要除去_____ 元素。
(2)Mn12O19中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn(III)、Mn(IV)物质的量之比为_____ 。生产过程中KMnO4、MnSO4•H2O按物质的量之比1∶5与K2S2O8反应,产物中硫元素全部以SO 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为______ 。
(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作_____ 。
(4)甲醛(HCHO)在OMS-2催化氧化作用下生成CO2和H2O,现利用OMS-2对某密闭空间的甲醛进行催化氧化实验。实验开始时,该空间内甲醛含量为1.22mg•L-1,CO2含量为0.59mg•L-1,一段时间后测得CO2含量升高至1.47mg•L-1,该实验中甲醛的转化率为______ (保留三位有效数字)。

(1)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示。为减少MnS2O6的生成,“浸锰”的适宜温度是

(2)Mn12O19中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn(III)、Mn(IV)物质的量之比为
 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作
(4)甲醛(HCHO)在OMS-2催化氧化作用下生成CO2和H2O,现利用OMS-2对某密闭空间的甲醛进行催化氧化实验。实验开始时,该空间内甲醛含量为1.22mg•L-1,CO2含量为0.59mg•L-1,一段时间后测得CO2含量升高至1.47mg•L-1,该实验中甲醛的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某兴趣小组用部分氧化的 为原料,制取高纯度的
为原料,制取高纯度的 ,并测定产品中铁元素含量,主要操作步骤如下:
,并测定产品中铁元素含量,主要操作步骤如下:
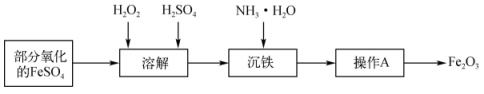
(1)写出沉铁反应的化学方程式:___________ 。
(2)写出加入 发生反应的离子方程式:
发生反应的离子方程式:___________ 。
(3)简述检验 是否洗净的操作:
是否洗净的操作:___________ 。
(4)准确称取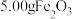 产品,经酸溶、还原为
产品,经酸溶、还原为 ,准确配成
,准确配成 溶液。取
溶液。取 于锥形瓶中,加入
于锥形瓶中,加入 溶液恰好完全反应。(
溶液恰好完全反应。( 与
与 反应产物为
反应产物为 ,假设
,假设 不与杂质反应)
不与杂质反应)
①配成 溶液所用的主要仪器有:烧杯、胶头滴管、
溶液所用的主要仪器有:烧杯、胶头滴管、___________ 。
②产品中铁元素的含量为___________ (保留小数点后两位小数)。
 为原料,制取高纯度的
为原料,制取高纯度的 ,并测定产品中铁元素含量,主要操作步骤如下:
,并测定产品中铁元素含量,主要操作步骤如下:
(1)写出沉铁反应的化学方程式:
(2)写出加入
 发生反应的离子方程式:
发生反应的离子方程式:(3)简述检验
 是否洗净的操作:
是否洗净的操作:(4)准确称取
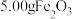 产品,经酸溶、还原为
产品,经酸溶、还原为 ,准确配成
,准确配成 溶液。取
溶液。取 于锥形瓶中,加入
于锥形瓶中,加入 溶液恰好完全反应。(
溶液恰好完全反应。( 与
与 反应产物为
反应产物为 ,假设
,假设 不与杂质反应)
不与杂质反应)①配成
 溶液所用的主要仪器有:烧杯、胶头滴管、
溶液所用的主要仪器有:烧杯、胶头滴管、②产品中铁元素的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】化学实验小组同学设计的苯与溴反应制取溴苯的实验方案和装置如下:

①把苯和少量液态溴放在烧瓶里,同时加入少量铁。
②用带导管的瓶塞寒紧瓶口,跟瓶口垂直的一段导管可以兼起冷凝的作用。
③观察并记录实验现象。
请回答相关问题:
(1)铁屑的本反应中的作用是________________ 。实验开始后,可以看到的现象是______________________ 。
(2)能说明该反应是取代反应而不是加成反应的现象是_______________ 。
(3)纯净的溴苯是无色的,但本实验中得到的溴苯是褐色的,原因是____________________ 。

①把苯和少量液态溴放在烧瓶里,同时加入少量铁。
②用带导管的瓶塞寒紧瓶口,跟瓶口垂直的一段导管可以兼起冷凝的作用。
③观察并记录实验现象。
请回答相关问题:
(1)铁屑的本反应中的作用是
(2)能说明该反应是取代反应而不是加成反应的现象是
(3)纯净的溴苯是无色的,但本实验中得到的溴苯是褐色的,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】芒硝(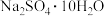 )易溶于水,常用于制革、制玻璃、制碱工业。一种利用含钠废料(主要含
)易溶于水,常用于制革、制玻璃、制碱工业。一种利用含钠废料(主要含 和Nal,还含有少量碳粉)制备芒硝的工艺流程如下图所示:
和Nal,还含有少量碳粉)制备芒硝的工艺流程如下图所示:
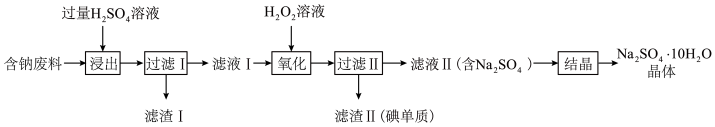
回答下列问题:
(1)滤渣Ⅰ的主要成分为_______ 。
(2)“浸出”过程中, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)已知“氧化”过程中, 的还原产物为
的还原产物为 ,则
,则 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)用实验制得的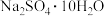 晶体准确配制1L 0.1
晶体准确配制1L 0.1 的
的 溶液,需用托盘天平称量
溶液,需用托盘天平称量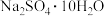 的质量为
的质量为_______ g,配制过程中,不需要用到的玻璃仪器为_______ (填序号)。
A.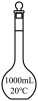 B.
B. 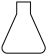 C.
C.  D.
D. 
(5)将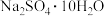 加热至失去其全部结晶水时,固体残留率的理论值为
加热至失去其全部结晶水时,固体残留率的理论值为_______ %。(固体残留率=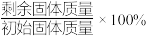 ,结果保留3位有效数字)。
,结果保留3位有效数字)。
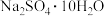 )易溶于水,常用于制革、制玻璃、制碱工业。一种利用含钠废料(主要含
)易溶于水,常用于制革、制玻璃、制碱工业。一种利用含钠废料(主要含 和Nal,还含有少量碳粉)制备芒硝的工艺流程如下图所示:
和Nal,还含有少量碳粉)制备芒硝的工艺流程如下图所示:
回答下列问题:
(1)滤渣Ⅰ的主要成分为
(2)“浸出”过程中,
 发生反应的化学方程式为
发生反应的化学方程式为(3)已知“氧化”过程中,
 的还原产物为
的还原产物为 ,则
,则 发生反应的离子方程式为
发生反应的离子方程式为(4)用实验制得的
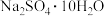 晶体准确配制1L 0.1
晶体准确配制1L 0.1 的
的 溶液,需用托盘天平称量
溶液,需用托盘天平称量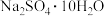 的质量为
的质量为A.
 B.
B.  C.
C.  D.
D. 
(5)将
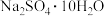 加热至失去其全部结晶水时,固体残留率的理论值为
加热至失去其全部结晶水时,固体残留率的理论值为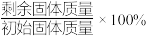 ,结果保留3位有效数字)。
,结果保留3位有效数字)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】高纯碘化钠晶体是核医学、大型安防设备、暗物质探测等领域的核心材料。某研究小组在实验室制备高纯NaI的简化流程如图:

已知:①I2(s)+I-(aq) I
I (aq)。
(aq)。
②水合肼(N2H4·H2O)具有强还原性,可将各种价态的碘还原为I-,氧化产物为N2。
③NaI易被氧化,易溶于水、酒精,在酒精中的溶解度随温度的升高增加不大。
回答下列问题:
(1)①步骤Ⅰ,I2与Na2CO3溶液同时发生两个反应,生成物除NaI外,还分别生成NaIO和NaIO3,一个反应为:I2+Na2CO3=NaI+NaIO+CO2↑,另一个反应为:___________ 。
②I2与Na2CO3溶液的反应很慢,加入NaI固体能使开始反应时的速率明显加快,原因可能是___________ 。
(2)步骤Ⅱ,水合肼与IO 反应的离子方程式为
反应的离子方程式为___________ 。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH时依次加入的试剂为___________ 、___________ 、___________ 。
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,蒸发操作为减压蒸发。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有___________ 。
A.直形冷凝管 B.球形冷凝管
B.球形冷凝管
C.烧杯 D.抽气泵
D.抽气泵
②采用“减压蒸发”的优点有:减小压强,降低沸点,利于水的蒸发;___________ 。
(5)将制备的NaI•2H2O粗品以无水乙醇为溶剂进行重结晶。请选择合理的操作并排序:加热乙醇→___________ →___________ →___________ →___________ →纯品(选填序号)。
①高纯水洗涤 ②减压蒸发结晶 ③真空干燥 ④NaI•2H2O粗品溶解 ⑤趁热过滤 ⑥降温结晶

已知:①I2(s)+I-(aq)
 I
I (aq)。
(aq)。②水合肼(N2H4·H2O)具有强还原性,可将各种价态的碘还原为I-,氧化产物为N2。
③NaI易被氧化,易溶于水、酒精,在酒精中的溶解度随温度的升高增加不大。
回答下列问题:
(1)①步骤Ⅰ,I2与Na2CO3溶液同时发生两个反应,生成物除NaI外,还分别生成NaIO和NaIO3,一个反应为:I2+Na2CO3=NaI+NaIO+CO2↑,另一个反应为:
②I2与Na2CO3溶液的反应很慢,加入NaI固体能使开始反应时的速率明显加快,原因可能是
(2)步骤Ⅱ,水合肼与IO
 反应的离子方程式为
反应的离子方程式为(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH时依次加入的试剂为
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,蒸发操作为减压蒸发。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有
A.直形冷凝管
 B.球形冷凝管
B.球形冷凝管
C.烧杯
 D.抽气泵
D.抽气泵
②采用“减压蒸发”的优点有:减小压强,降低沸点,利于水的蒸发;
(5)将制备的NaI•2H2O粗品以无水乙醇为溶剂进行重结晶。请选择合理的操作并排序:加热乙醇→
①高纯水洗涤 ②减压蒸发结晶 ③真空干燥 ④NaI•2H2O粗品溶解 ⑤趁热过滤 ⑥降温结晶
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
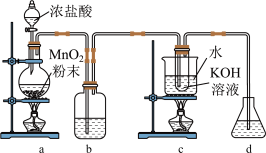
【推荐1】很多化学反应条件不同,产物不同,如Cl2与KOH反应,常温下生成KClO,加热生成KClO3.实验室利用下图装置制备KClO3,然后进一步探究其性质。
(1)盛装浓盐酸的仪器名称为___________ ,a装置中发生反应的化学方程式为___________ ,装置b的作用是___________ 。
(2)c中反应的离子方程式为___________ ,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(3)d装置的作用是___________ ,其中反应的离子方程式为___________ 。
(4)取c中溶液,滴加浓盐酸并加热,可产生黄绿色气体,结合上述KClO3的制备实验,可说明在碱性条件下氧化性:Cl2___________ KClO3(填“>”“<”或“=”,下同),酸性条件下氧化性:Cl2___________ KClO3。
(1)盛装浓盐酸的仪器名称为
(2)c中反应的离子方程式为
(3)d装置的作用是
(4)取c中溶液,滴加浓盐酸并加热,可产生黄绿色气体,结合上述KClO3的制备实验,可说明在碱性条件下氧化性:Cl2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】其同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、A12O3),不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如图流程:
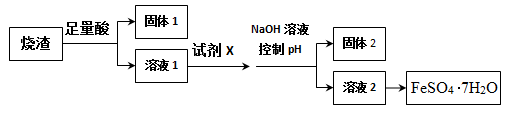
已知,某些金属阳离子可以通过“控制pH”[既调节溶液的酸碱性,pH=-lgc(H+)),pH值越大,碱性越强]使其转化为沉淀。固体2为白色沉淀。
(1)加足量酸之前,烧渣需经过进一步粉碎处理,粉碎的目的是__________ 。
(2)溶解烧渣选用的足量酸能否是盐酸,并说明理由_____ 。
(3)固体1有诸多用途,请列举其中一个____ ,试剂X的作用是______ 。
(4)某同学在控制pH这步操作时不慎将氢氧化钠溶液加过量了,结果得到的白色沉淀迅速转化为灰绿色,最终变为红褐色沉淀。请用化学用语解释固体2白色变成红褐色的原_____________ 。
(5)从溶液2中得到绿矾的过程中除需控制温度,防止产品分解外还应注意______ 。
(6)唐代苏敬《新修本草》对绿矾有如下描述:“本来绿色,新出窑未见风者,正如琉璃。陶及今人谓之石胆,烧之赤色。”另已知1mol绿矾隔绝空气高温煅烧完全分解,转移NA个电子。试写出绿矾隔绝空气高温煅烧分解的化学反应方程式____________ 。

已知,某些金属阳离子可以通过“控制pH”[既调节溶液的酸碱性,pH=-lgc(H+)),pH值越大,碱性越强]使其转化为沉淀。固体2为白色沉淀。
(1)加足量酸之前,烧渣需经过进一步粉碎处理,粉碎的目的是
(2)溶解烧渣选用的足量酸能否是盐酸,并说明理由
(3)固体1有诸多用途,请列举其中一个
(4)某同学在控制pH这步操作时不慎将氢氧化钠溶液加过量了,结果得到的白色沉淀迅速转化为灰绿色,最终变为红褐色沉淀。请用化学用语解释固体2白色变成红褐色的原
(5)从溶液2中得到绿矾的过程中除需控制温度,防止产品分解外还应注意
(6)唐代苏敬《新修本草》对绿矾有如下描述:“本来绿色,新出窑未见风者,正如琉璃。陶及今人谓之石胆,烧之赤色。”另已知1mol绿矾隔绝空气高温煅烧完全分解,转移NA个电子。试写出绿矾隔绝空气高温煅烧分解的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学课外兴趣小组根据学习的相关知识,设计了氯气的制取、净化和收集实验,其装置如下图所示,请根据题意回答下列问题:

(1)F 中盛装试剂的名称是:____________ ,圆底烧瓶中发生反应的化学方程式为:________________ 。
(2)从A装置中产生的氯气主要含有氯化氢杂质,因此选用装置B进行除杂,B中应该盛装的试剂名称为:______________ ,C 装置中盛装的是浓硫酸,其作用是:_______________ 。
(3) E 装置中盛装的是烧碱溶液,其作用是:________________ ,发生反应的离子方程式为:____________________ 。

(1)F 中盛装试剂的名称是:
(2)从A装置中产生的氯气主要含有氯化氢杂质,因此选用装置B进行除杂,B中应该盛装的试剂名称为:
(3) E 装置中盛装的是烧碱溶液,其作用是:
您最近一年使用:0次



