X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)写出下列元素的名称:X_______ ,Y_______ ,Z_______ 。
(2)X—H和Y—H属于极性共价键,其中极性较强的是_______ (X、Y用元素符号表示)。X的第一电离能比Y的_______ (填“大”或“小”)。
(3)X的最简单氢化物的空间结构为_______ 形,该分子为_______ (填“极性分子”或“非极性分子”)。
(4)基态Y元素的核外未成对的电子有___ 个,基态Y元素的电子轨道表示式为_____ 。
(1)写出下列元素的名称:X
(2)X—H和Y—H属于极性共价键,其中极性较强的是
(3)X的最简单氢化物的空间结构为
(4)基态Y元素的核外未成对的电子有
更新时间:2022/08/23 20:30:26
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A___________ ,B___________ ,C___________ ,D___________ ,E___________
(2)写出A与B、B与E两元素最高价氧化物的水化物之间反应的离子方程式:
A与B:___________
B与E:___________
(3)比较C、D的最高价氧化物的水化物的酸性:___________ (用化学式表示)。
(1)写出下列元素符号:A
(2)写出A与B、B与E两元素最高价氧化物的水化物之间反应的离子方程式:
A与B:
B与E:
(3)比较C、D的最高价氧化物的水化物的酸性:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
(1)1的元素符号是___________
(2)1、2两种元素的原子半径大小关系:1___________ 2(填“>”或“<”);
(3)3、4和5中,金属性最强的元素是___________ (填元素符号);
(4)5、6的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。
| 族 周期 | IA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | 1 | 2 | |||||||
| 3 | 3 | 4 | 5 | 6 | Ar | ||||
(2)1、2两种元素的原子半径大小关系:1
(3)3、4和5中,金属性最强的元素是
(4)5、6的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
【推荐3】X、Y、Z、M、Q是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
(1)X最外层电子的轨道表达式是 ___________ 。
(2)M元素的名称是___________ 。
(3)Z元素基态原子中能量最高的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:___________ ,
②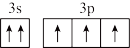 :
:___ 。
(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是___ 。
| 元素 | 相关信息 |
| X | 次外层电子数是最外层电子数的 |
| Y | 形成的氧化物和强酸、强碱都可以反应 |
| Z | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| M | 前4周期元素原子核外电子排布中未成对电子数最多的元素 |
| Q | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(2)M元素的名称是
(3)Z元素基态原子中能量最高的电子的电子云在空间有
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:
②
 :
:(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是___________________________________
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:___________________________________
(3)在一定条件下,甲与O2反应的化学方程式是_______________________
(4)丁的元素符号是_________ ,它的核外电子排布式为 _______________________
(5)丁的氧化物的晶体结构与_________________ 的晶体结构相似。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
(3)在一定条件下,甲与O2反应的化学方程式是
(4)丁的元素符号是
(5)丁的氧化物的晶体结构与
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】以金红石(主要成分为 ,含少量铝、硅、钒的氧化物杂质)为原材料,制取金属钛的流程如下:
,含少量铝、硅、钒的氧化物杂质)为原材料,制取金属钛的流程如下: 中可能含有的物质沸点如下:
中可能含有的物质沸点如下: :136℃,
:136℃, :127℃,
:127℃, :57℃,
:57℃, :180℃
:180℃
(1)Ti的价电子轨道表示式:____ ,写出由金红石在高温下制得 的化学方程式
的化学方程式____ 。
(2)除钒过程中的化学方程式为_______ 。
(3)蒸馏的目的是为了除去_____ 元素(填元素符号)。“加铝”和“蒸馏”的顺序不能交换,理由是_______ 。
(4)下列冶炼方法与用Mg冶炼Ti的方法最相似的是_______。
(5)金属钛可制得Ti-Fe合金,该合金主要应用于新型_______ 合金材料。
 ,含少量铝、硅、钒的氧化物杂质)为原材料,制取金属钛的流程如下:
,含少量铝、硅、钒的氧化物杂质)为原材料,制取金属钛的流程如下: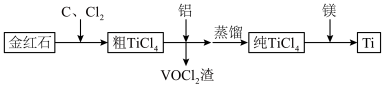
 中可能含有的物质沸点如下:
中可能含有的物质沸点如下: :136℃,
:136℃, :127℃,
:127℃, :57℃,
:57℃, :180℃
:180℃(1)Ti的价电子轨道表示式:
 的化学方程式
的化学方程式(2)除钒过程中的化学方程式为
(3)蒸馏的目的是为了除去
(4)下列冶炼方法与用Mg冶炼Ti的方法最相似的是_______。
| A.钠高温与KCl制钾 | B.电解熔融氯化钠制钠 |
| C.铝热反应制钒 | D.氧化汞分解制汞 |
(5)金属钛可制得Ti-Fe合金,该合金主要应用于新型
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】X、Y、Z、T四种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,T在元素周期表的各元素中电负性最大。请回答下列问题。
(1)X元素符号为___________ ,Y属于___________ 区元素,Z元素基态原子的电子排布式为___________ 。
(2) 与
与 分子的空间结构分别是
分子的空间结构分别是___________ 和___________ ,相同条件下两者在水中的溶解度较大的是___________ (写分子式),理由是___________ 。
(3) 中X原子采取的杂化方式是
中X原子采取的杂化方式是___________ 。
(4)X、Y、Z的最简单气态氢化物的沸点由高到低的排列顺序是___________ ,原因是___________ 。
(5)T的氢化物水溶液中存在的氢键___________ 种。
(1)X元素符号为
(2)
 与
与 分子的空间结构分别是
分子的空间结构分别是(3)
 中X原子采取的杂化方式是
中X原子采取的杂化方式是(4)X、Y、Z的最简单气态氢化物的沸点由高到低的排列顺序是
(5)T的氢化物水溶液中存在的氢键
您最近一年使用:0次
【推荐1】使用铜基催化剂(Cu/ZnO/Al2O3),以 CO2和 H2 合成 CH3OH 是大规模实现 低碳减排和清洁能源再生产的有效路径。回答下列问题:
(1)Cu的价电子排布图___________ ,C、 O、H三种元素第一电离能由小到大的顺序为___________ 。
(2)CO2的空间构型为___________ ;CH3OH 分子中 O 的杂化轨道类型是___________ ,
(3)CO2、H2 和 CH3OH 中,属于极性分子的是___________ ,由非极性键结合成的非极性 分子是___________ 。
(4)CH3OH 的沸点(64.7 ℃)大于CH3SH(7.6 ℃),其原因 是___________ 。
(5)CH3OH晶体属于___________ 晶体,
(6)立方CuO晶胞结构如图所示。其中Cu2+的配位数为___________ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
(1)Cu的价电子排布图
(2)CO2的空间构型为
(3)CO2、H2 和 CH3OH 中,属于极性分子的是
(4)CH3OH 的沸点(64.7 ℃)大于CH3SH(7.6 ℃),其原因 是
(5)CH3OH晶体属于
(6)立方CuO晶胞结构如图所示。其中Cu2+的配位数为
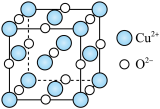
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)基态e原子中电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形,核外共有___________ 种不同运动状态的电子。
(2)元素b在元素周期表中的位置为___________ ,元素i位于元素周期表的___________ 区。
(3)g的元素符号为___________ ,其基态原子的价电子排布式为___________ 。
(4)元素b、c、d的第一电离能从大到小的顺序是___________ (用元素符号表示)。
(5)元素h的价层电子排布图为___________ 。
(6)元素d的简单氢化物的空间构型为___________ ,该分子属于___________ (填“极性”或“非极性”)分子,d原子采取的杂化方式为___________ 。
(7)元素b、c的简单氢化物中,沸点较高的是___________ (填化学式),原因是___________ 。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | |||||||||||||||||
| g | h | i | |||||||||||||||
(2)元素b在元素周期表中的位置为
(3)g的元素符号为
(4)元素b、c、d的第一电离能从大到小的顺序是
(5)元素h的价层电子排布图为
(6)元素d的简单氢化物的空间构型为
(7)元素b、c的简单氢化物中,沸点较高的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】新冠期间受“谣言”影响蒙脱石散曾一度脱销。蒙脱石散的有效成分可表示(AlMg)2(SixOy)(OH)z•nH2O,常用于成人及儿童急、慢性腹泻。
(1)基态Si原子的电子排布式为_______ 。
(2)比较B、Al第一电离能大小:I1(Al)_______ I1(B)(填“>”或“<”),说明判断理由_______ 。
(3)SiCl4能用于制取纯硅、硅酸乙酯等,也能用于制取烟幕剂。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液流_______ (填“会”或“不会”)发生偏转。
②SiH4、CH4中较稳定的是_______ ;SiCl4、CCl4中沸点较高是_______ 。
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。
①蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图所示:

据此分析,x:y=_______ 。
②SiO2晶胞可理解成将金刚石晶胞(如图)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。若SiO2晶胞的密度为dg•cm-3,NA表示阿伏加德罗常数的值,则晶胞中Si与Si之间的最短距离为_______ nm(用含NA表和d的式子表示)。

(1)基态Si原子的电子排布式为
(2)比较B、Al第一电离能大小:I1(Al)
(3)SiCl4能用于制取纯硅、硅酸乙酯等,也能用于制取烟幕剂。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液流
②SiH4、CH4中较稳定的是
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。
①蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图所示:

据此分析,x:y=
②SiO2晶胞可理解成将金刚石晶胞(如图)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。若SiO2晶胞的密度为dg•cm-3,NA表示阿伏加德罗常数的值,则晶胞中Si与Si之间的最短距离为

您最近一年使用:0次



