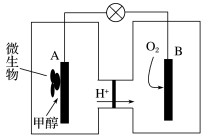
人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为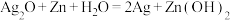 。
。
(1)工作时电流从___________ 极流向___________ 极(填“ ”或“Zn”)。
”或“Zn”)。
(2)电极反应式:
正极:___________ ,发生___________ 反应;
负极:___________ ,发生___________ 反应。
(3)工作时电池正极区的pH___________ (填“增大”、“减小”或“不变”)。
电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为
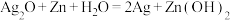 。
。(1)工作时电流从
 ”或“Zn”)。
”或“Zn”)。(2)电极反应式:
正极:
负极:
(3)工作时电池正极区的pH
更新时间:2022/10/15 07:05:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】电能是现代社会应用最广泛的能源之一。_______ 。
a.负极反应是 b.电子由Zn片通过导线流向Cu片
b.电子由Zn片通过导线流向Cu片
c.一段时间后,溶液的pH减小 d.溶液中的 向Cu片移动
向Cu片移动
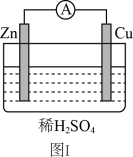
(2)图Ⅰ所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为_______ mol。
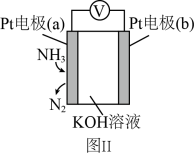
(3)图Ⅱ所示装置为电化学气敏传感器,通过电压表示数可测量环境中 的含量。电极b是
的含量。电极b是_______ (填“正”或“负”)极;溶液中 向电极
向电极_______ (填“a”或“b”)移动。
(4)图Ⅱ所示原电池中b极的电极反应式为_______ 。
a.负极反应是
 b.电子由Zn片通过导线流向Cu片
b.电子由Zn片通过导线流向Cu片c.一段时间后,溶液的pH减小 d.溶液中的
 向Cu片移动
向Cu片移动(2)图Ⅰ所示原电池中,当Cu表面析出4.48L氢气(标准状况)时,导线中通过的电子的物质的量为
(3)图Ⅱ所示装置为电化学气敏传感器,通过电压表示数可测量环境中
 的含量。电极b是
的含量。电极b是 向电极
向电极(4)图Ⅱ所示原电池中b极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请根据反应Fe+CuSO4==Cu+FeSO4设计一个原电池,画出装置图
_____________________

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
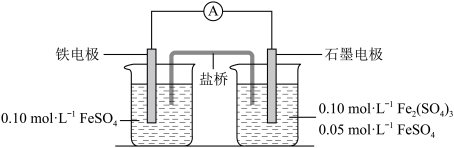
回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________ 电极溶液中。
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________ 。
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为___________________ ,铁电极的电极反应式为_______________________________ 。因此,验证了Fe2+氧化性小于________ 、还原性小于________ 。

回答下列问题:
(1)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(2)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(3)根据(1)、(2)实验结果,可知石墨电极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,镁条做原电池的___________ 极。
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________ 。
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质是溶解在溶液中的O2,则该电极反应式为___________ 。
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________ 。
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)。
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关。
【实验1】
| 装置 | 实验现象 |
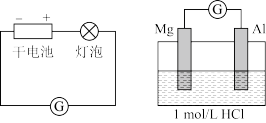 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 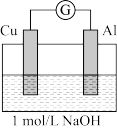 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 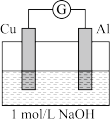 煮沸冷却后的溶液 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象:约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| A.上述两装置中,开始时铜片表面得电子的物质是O2 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
| C.铜片表面产生的气泡为H2 |
| D.由“铝条表面气泡略有减少”能推测H+在铜片表面得电子 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图所示,将 、
、 和电解质溶液组成一种原电池。试回答下列问题:
和电解质溶液组成一种原电池。试回答下列问题:________ 。
(2)若电解质溶液为 溶液,则负极为
溶液,则负极为________ (填“Mg”或“Al”)。
(3)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:________ (填“a极到b极”或“b极到a极”)。
② 电极的电极方程式为
电极的电极方程式为________ 。
③若转移的电子为0.4mol,标准状况下消耗的氧气体积为________ 。
 、
、 和电解质溶液组成一种原电池。试回答下列问题:
和电解质溶液组成一种原电池。试回答下列问题: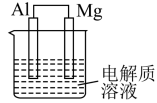
(2)若电解质溶液为
 溶液,则负极为
溶液,则负极为(3)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:
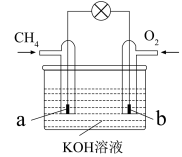
②
 电极的电极方程式为
电极的电极方程式为③若转移的电子为0.4mol,标准状况下消耗的氧气体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
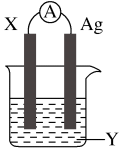
(1)电极X的材料是______ ;电解质溶液Y是________ ;
(2)银电极为电池的____ 极,发生的电极反应式为______ ; X电极上发生的电极反应为______ ;(填反应类型)
(3)外电路中的电子是从_______ 电极流向________ 电极。Ag+向_______ (填正极或负极)移动。
(4)当有1.6g铜溶解时,银棒增重_________________ 。
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O; B极:O2+4e-=2O2-。则A极是电池的______ 极;电子从该极____ (填“流入”或“流出”),该电池的总反应为_______ 。

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
(4)当有1.6g铜溶解时,银棒增重
(5)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2--2e-=H2O; B极:O2+4e-=2O2-。则A极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及铁的化合物应用广泛。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式___________ 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图___________ ,标出电极名称及电极材料、电解质溶液、电流方向,并写出正极反应式___________ ,负极反应式___________ 。
(3)高铁酸钾(K2FeO4)是一种理想的水处理剂,目前高铁电池的研制正在进行中。如图甲所示是高铁电池的模拟实验装置。
①该电池放电时正极产生Fe(OH)3,正极电极反应为___________ 。
②电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择___________ 作为电解质。
③图乙为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________ 。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图
(3)高铁酸钾(K2FeO4)是一种理想的水处理剂,目前高铁电池的研制正在进行中。如图甲所示是高铁电池的模拟实验装置。

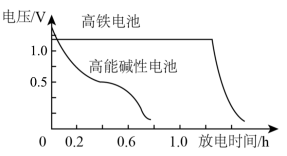
①该电池放电时正极产生Fe(OH)3,正极电极反应为
②电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | 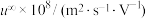 | 阴离子 | 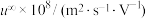 |
| Li+ | 4.07 |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| K+ | 7.62 |  | 8.27 |
您最近一年使用:0次
【推荐3】回答下列问题:
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:
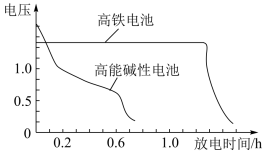
①高铁电池的优点是:_____ 。
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:_____ 。
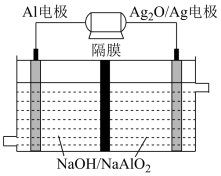
(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:_____ 。
(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的_____ (填“正极”或“负极”),正极附近溶液的pH_____ (填“增大”、“减小”或“不变”)。
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是_____ 。
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:

①高铁电池的优点是:
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:

(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是
您最近一年使用:0次