为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成二氧化硒(SeO2),再用KI溶液处理后回收Se。发生的反应为:
①Se+2H2SO4(浓)=2SO2↑+ SeO2+2H2O;
②SeO2+4KI+4HNO3=4KNO3+Se+2I2+2H2O。
下列说法错误的是
①Se+2H2SO4(浓)=2SO2↑+ SeO2+2H2O;
②SeO2+4KI+4HNO3=4KNO3+Se+2I2+2H2O。
下列说法错误的是
| A.反应①中还原产物和氧化产物的分子数之比为2∶1 |
| B.反应②中KI显示还原性,HNO3显示氧化性 |
| C.反应②中每生成1个I2分子,反应②转移2个电子 |
| D.氧化性:H2SO4(浓)>I2 |
更新时间:2022/11/05 17:57:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】关于反应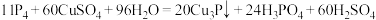 ,下列说法
,下列说法不正确 的是
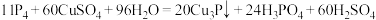 ,下列说法
,下列说法A.还原产物只有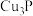 |
B.氧化剂是 和 和 |
C.每消耗11个 ,反应转移120个电子 ,反应转移120个电子 |
| D.氧化产物与还原产物的个数之比为5:6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
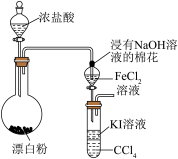
【推荐2】H2S和O2的混合气体,通入FeCl2、CuCl2、FeCl3的混合溶液,转化关系如图所示。下列描述正确的是
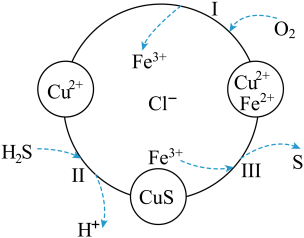

| A.在图示转化关系中化合价不变的元素只有氢、氯、铜 |
| B.转化过程中参加循环反应的离子只有Fe2+、Fe3+ |
| C.过程Ⅱ反应的离子方程式为Cu2++S2-=CuS↓ |
| D.氧化性强弱的顺序为O2>S> Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是
| A.2Fe2++I2=2Fe3++2I- | B.I2+SO2+2H2O=4H++SO42-+2I- |
| C.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ | D.Cl2+2I-=2Cl-+I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性: >Cl2>Fe3+>I2 >Cl2>Fe3+>I2 |
| B.溶液中Fe3+与I-可以大量共存 |
| C.上述实验中,共有两个氧化还原反应 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知X为一种常见酸的浓溶液,加热时与Cu反应能产生使澄清石灰水变浑浊的气体。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是
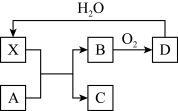

| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水中,一定有白色沉淀产生 |
| D.工业上,B转化为D的反应条件为高温、催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用下图所示装置进行下列实验,能得出相应实验结论的是


| 选项 | ① | ② | ③ | 实验结论 |
| A | 80%硫酸溶液 | Na2SO3 | 酸性高锰酸钾溶液 | SO2有漂白性 |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可生成白色沉淀 |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:N>C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用 催化还原
催化还原 ,可以消除氨氧化物的污染。例如:
,可以消除氨氧化物的污染。例如:
①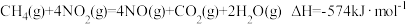
②
下列说法正确的是
 催化还原
催化还原 ,可以消除氨氧化物的污染。例如:
,可以消除氨氧化物的污染。例如:①
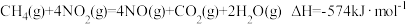
②

下列说法正确的是
A.由反应①可知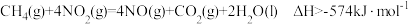 |
B.反应②中当 完全反应时,电子转移数目为 完全反应时,电子转移数目为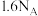 |
C.若用标准状况下 还原 还原 生成 生成 和水蒸气,放出的热量为 和水蒸气,放出的热量为 |
D.一定条件下,若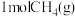 与 与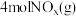 分别发生反应①和②,共放出热量为 分别发生反应①和②,共放出热量为 ,则 ,则 与 与 的体积比为 的体积比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列相关说法正确的是
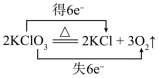
| 化学反应方程式 | 相关说法 | |
| A | 2KClO3 2KCl +3O2↑ 2KCl +3O2↑ | 双线桥: |
| B | 2Fe3++Cu=2Fe2++Cu2+ | 氧化性:Cu>Fe2+ |
| C | 2Na2O2+ 2H2O= 4NaOH+ O2↑ | 每生成1个O2,转移2个电子 |
| D | 除去CO2中的HCl气体 | 将混合气体通入装饱和NaOH溶液的洗气瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼
转化为肼 ,其反应历程如图所示。
,其反应历程如图所示。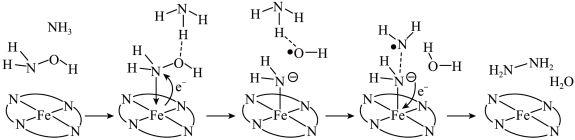
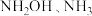 和
和 分子中只含极性键
分子中只含极性键 键断裂和
键断裂和 键生成
键生成 元素价态升高,
元素价态升高, 元素价态降低
元素价态降低 ,反应可得
,反应可得







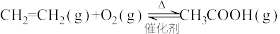
 ,下列有关乙烯直接氧化制乙酸反应的说法正确的是
,下列有关乙烯直接氧化制乙酸反应的说法正确的是 ,降低温度可提高乙酸的平衡转化率
,降低温度可提高乙酸的平衡转化率 (E表示键能)
(E表示键能) 转移电子的数目约等于
转移电子的数目约等于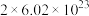
 的平衡转化率
的平衡转化率

