下列有关热化学方程式的描述正确的是
| A.热化学方程式前面的化学计量数既表示分子数也表示物质的量 |
| B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
C.已知在一定条件下,2molSO2与1molO2充分反应后,释放出98kJ的热量,则其热化学方程式为2SO2(g)+O2(g) 2SO3(g) ΔH=-98kJ•mol-1 2SO3(g) ΔH=-98kJ•mol-1 |
| D.已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ•mol-1,则稀Ba(OH)2(aq)和稀H2SO4(aq)完全反应生成1molH2O(l)时,放出57.3kJ热量 |
更新时间:2023/02/02 20:23:47
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】20世纪初,德国化学家哈伯在实验室首次利用氮气和氢气合成了氨:N2(g)+3H2(g)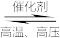 2NH3(g) △H=-92.4kJ·mol-1,从此人类进入了新的农业时代,化肥的使用大大提高了粮食产量。下列有关合成氨反应说法不正确的是
2NH3(g) △H=-92.4kJ·mol-1,从此人类进入了新的农业时代,化肥的使用大大提高了粮食产量。下列有关合成氨反应说法不正确的是
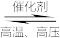 2NH3(g) △H=-92.4kJ·mol-1,从此人类进入了新的农业时代,化肥的使用大大提高了粮食产量。下列有关合成氨反应说法不正确的是
2NH3(g) △H=-92.4kJ·mol-1,从此人类进入了新的农业时代,化肥的使用大大提高了粮食产量。下列有关合成氨反应说法不正确的是| A.NH3既是氧化产物,又是还原产物 |
| B.升温和加压均可加快合成氨的反应速率 |
| C.用E总表示物质能量之和,E总(反应物)<E总(生成物) |
| D.每生成2molNH3(g),反应过程中放出92.4kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应不仅有物质的变化还伴随能量的变化,下列说法错误的是
A.已知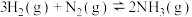  ,则其逆反应的 ,则其逆反应的 一定大于0 一定大于0 |
| B.热化学方程式和化学方程式的化学计量数的意义不完全相同 |
C.常温常压下, 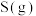 完全燃烧比 完全燃烧比  完全燃烧时的焓变大 完全燃烧时的焓变大 |
D.  ,则 ,则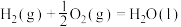 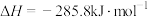 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列关于化学反应与能量的说法不正确的是
A.已知正丁烷的燃烧热ΔH=-2878kJ·mol-1,则表示正丁烷燃烧热的热化学方程式为CH3CH2CH2CH3(g)+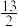 O2(g)=4CO2(g)+5H2O(l) ΔH=-2878kJ·mol-1 O2(g)=4CO2(g)+5H2O(l) ΔH=-2878kJ·mol-1 |
B.已知在一定条件下,2molSO2与1molO2充分反应后,释放出98kJ的热量,则其热化学方程式为2SO2(g)+O2(g) 2SO3(g) ΔH=-98kJ·mol-1 2SO3(g) ΔH=-98kJ·mol-1 |
C.已知稀盐酸与稀NaOH溶液反应的中和热ΔH=-57.3kJ·mol-1,则表示稀硫酸与稀NaOH溶液反应的热化学方程式为 H2SO4(aq)+NaOH(aq)= H2SO4(aq)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH=-57.3kJ·mol-1 Na2SO4(aq)+H2O(l) ΔH=-57.3kJ·mol-1 |
| D.已知CuSO4(s)+5H2O(l)=CuSO4·5H2O(s),该反应为熵减小的反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列热化学方程式中,正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
B.由N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1可知,当反应中转移6 mol电子时,反应放出的热量小于92.4 kJ 2NH3(g) ΔH=-92.4 kJ·mol-1可知,当反应中转移6 mol电子时,反应放出的热量小于92.4 kJ |
| C.甲烷的燃烧热ΔH为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1 |
| D.在101 kPa时,4 g H2完全燃烧生成液态水,放出571.6 kJ热量,氢气燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:①
 ,②
,②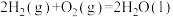
 ,下列有关说法正确的是
,下列有关说法正确的是

 ,②
,②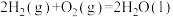
 ,下列有关说法正确的是
,下列有关说法正确的是
A.氢气的燃烧热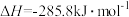 |
B.若反应②中水为气态,则同样条件下的反应热: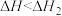 |
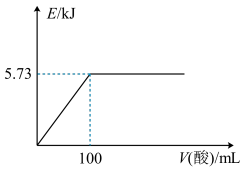
C.向含0.1mol NaOH的溶液中加入一定体积1  的醋酸,反应中的热量变化如图所示 的醋酸,反应中的热量变化如图所示 |
D.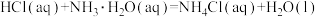 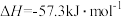 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是
| A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式:2H2(g)+O2(g)=2H2O(l)ΔH=-285.8kJ·mol-1 |
C.根据热化学方程式:S(s)+O2(g) SO2(g)△H=-297.23kJ/mol,可推知1molSO2(g)的能量总和大于1moS(s)和1molO2(g)的能量总和 SO2(g)△H=-297.23kJ/mol,可推知1molSO2(g)的能量总和大于1moS(s)和1molO2(g)的能量总和 |
D.根据稀溶液中反应:H+(aq)+OH-(aq) H2O(l)△H=-57.3kJ/mol;若将含0.5molH2SO4的浓硫酸与含lmolNaOH的稀溶液混合时,放出的热量大于57.3kJ H2O(l)△H=-57.3kJ/mol;若将含0.5molH2SO4的浓硫酸与含lmolNaOH的稀溶液混合时,放出的热量大于57.3kJ |
您最近一年使用:0次
【推荐1】一个化学反应无论是一步完成还是分几步完成,反应热都是一样的。该定律称为盖斯定律。依据图示关系,下列说法不正确 的是
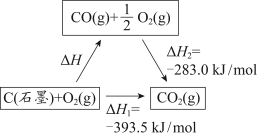
| A.石墨燃烧是放热反应 |
| B.1 mol C(石墨)和1 mol CO分别在足量O2中燃烧,全部转化为CO2,后者放热多 |
C.C(石墨) +  O2(g) = CO(g) ΔH=ΔH1-ΔH2 O2(g) = CO(g) ΔH=ΔH1-ΔH2 |
| D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:
①Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ΔH1
②2H2O(l)=2H2(g)+O2(g) ΔH2
③2H2O2(l)=2H2O(l)+O2(g) ΔH3
④Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH4
则ΔH4的正确表达式为( )
①Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ΔH1
②2H2O(l)=2H2(g)+O2(g) ΔH2
③2H2O2(l)=2H2O(l)+O2(g) ΔH3
④Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH4
则ΔH4的正确表达式为( )
A.ΔH4=ΔH1+ ×ΔH2+ ×ΔH2+ ×ΔH3 ×ΔH3 | B.ΔH4=ΔH1+ ×ΔH2— ×ΔH2— ×ΔH3 ×ΔH3 |
| C.ΔH4=ΔH1+2×ΔH2—2×ΔH3 | D.ΔH4=2×ΔH1+ΔH2+ΔH3 |
您最近一年使用:0次