按要求回答以下问题:
(1)现有 的配合物
的配合物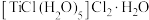 ,其中配离子是
,其中配离子是_______ ,配位数为_______ ,在0.2mol该配合物溶液中滴加足量的 溶液,产生沉淀的物质的量为
溶液,产生沉淀的物质的量为_______ ;
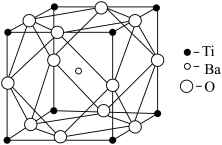
(2)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为_______  。
。
(1)现有
 的配合物
的配合物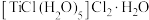 ,其中配离子是
,其中配离子是 溶液,产生沉淀的物质的量为
溶液,产生沉淀的物质的量为(2)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏加德罗常数为
 ,则该晶体的密度为
,则该晶体的密度为 。
。
更新时间:2023/02/27 21:38:10
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】铁及其化合物用途广泛,比如铁元素是人体必需的微量元素,成人体内约有4-5克铁,其中72%以血红蛋白形式存在。请回答下列问题:
(1)基态Fe原子占据最高能层的电子的电子云轮廓图为___________ ,基态Fe3+原子的价电子排布图为___________ 。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为___________ ,其中Fe的配位数为___________ 。
(3)由铁粉与环戊二烯(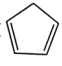 )在300℃的氮气氛中加热可以制得二茂铁(
)在300℃的氮气氛中加热可以制得二茂铁(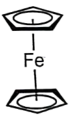 ),已知环戊二烯负离子(C5H
),已知环戊二烯负离子(C5H )中所有C原子均共平面,分子中的大π键可用符号π
)中所有C原子均共平面,分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则环戊二烯负离子中的大π键可表示为
),则环戊二烯负离子中的大π键可表示为___________ 。
(1)基态Fe原子占据最高能层的电子的电子云轮廓图为
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(3)由铁粉与环戊二烯(
 )在300℃的氮气氛中加热可以制得二茂铁(
)在300℃的氮气氛中加热可以制得二茂铁( ),已知环戊二烯负离子(C5H
),已知环戊二烯负离子(C5H )中所有C原子均共平面,分子中的大π键可用符号π
)中所有C原子均共平面,分子中的大π键可用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则环戊二烯负离子中的大π键可表示为
),则环戊二烯负离子中的大π键可表示为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为_________________ ,其最外层电子的电子云形状为___________ 。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为_____________ (用元素符号表示)。
②N、O两元素的的第一电离能由大到小的顺序为___________ (用元素符号表示)。
③SO42-中S原子的杂化方式为___________ ,VSEPR模型名称为___________________ 。
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为_____ ,σ键和π键的数目之比为______________ 。其空间构型为__________ 。
(4)K3[Fe(CN)6]晶体中配离子的配位体为_____ (用化学符号表示)
(1)基态Fe原子的价层电子的电子排布图为
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐。
①O、S两元素的电负性由大到小的顺序为
②N、O两元素的的第一电离能由大到小的顺序为
③SO42-中S原子的杂化方式为
(3)Fe3+可与某阴离子发生特征的显色反应,用于鉴定Fe3+。该阴离子的电子式为
(4)K3[Fe(CN)6]晶体中配离子的配位体为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。

若已知 的原子半径为
的原子半径为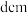 ,
, 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值, 的摩尔质量为
的摩尔质量为 ,请回答:
,请回答:
(1)一个晶胞中 原子的数目为
原子的数目为______ 。
(2)该晶体的密度为______  (用字母表示)。
(用字母表示)。

若已知
 的原子半径为
的原子半径为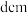 ,
, 代表阿伏加德罗常数的值,
代表阿伏加德罗常数的值, 的摩尔质量为
的摩尔质量为 ,请回答:
,请回答:(1)一个晶胞中
 原子的数目为
原子的数目为(2)该晶体的密度为
 (用字母表示)。
(用字母表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知铜的晶胞结构如图(a)所示。若铜原子的半径为1.29×10−10m,试求:

(1)每个晶胞中含有铜原子的个数为多少_______ ?
(2)铜晶体中晶胞的边长[即图(b)中AB的长度]为多少_______ ?

(1)每个晶胞中含有铜原子的个数为多少
(2)铜晶体中晶胞的边长[即图(b)中AB的长度]为多少
您最近一年使用:0次

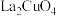 在传感器、汽车尾气催化净化、氮氧化物催化消除、中温固体氧化物燃料电池等领域具有良好的应用前景,回答下列问题:
在传感器、汽车尾气催化净化、氮氧化物催化消除、中温固体氧化物燃料电池等领域具有良好的应用前景,回答下列问题: 原子的核外电子排布式为
原子的核外电子排布式为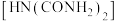 是一种有机化合物,分子中氮、碳两种元素原子的杂化类型分别是
是一种有机化合物,分子中氮、碳两种元素原子的杂化类型分别是 缩二脲中含有
缩二脲中含有 键的数目为
键的数目为 形成稳定离子,其原因是
形成稳定离子,其原因是


