现有以下物质:① 溶液;②液态
溶液;②液态 ;③
;③ 晶体;④熔融
晶体;④熔融 ;⑤Na;⑥氯气;⑦淀粉胶体。
;⑤Na;⑥氯气;⑦淀粉胶体。
(1)以上物质中属于电解质的是________ (填序号)。
(2)将淀粉溶于水,要判定得到的分散系是胶体还是溶液。判定的方法名称是________ 。
(3)写出③ 晶体在生活中的一种应用
晶体在生活中的一种应用________________ 。
(4)写出③在水溶液中的电离方程式:________________ 。
(5)⑤Na的其中一种氧化物可用作呼吸面具和潜艇的供氧剂,写出其与水反应的化学方程式________________ 。
(6)用⑥氯气和石灰乳可以制取漂白粉,漂白粉在空气中生成 的化学方程式为
的化学方程式为________________ 。
 溶液;②液态
溶液;②液态 ;③
;③ 晶体;④熔融
晶体;④熔融 ;⑤Na;⑥氯气;⑦淀粉胶体。
;⑤Na;⑥氯气;⑦淀粉胶体。(1)以上物质中属于电解质的是
(2)将淀粉溶于水,要判定得到的分散系是胶体还是溶液。判定的方法名称是
(3)写出③
 晶体在生活中的一种应用
晶体在生活中的一种应用(4)写出③在水溶液中的电离方程式:
(5)⑤Na的其中一种氧化物可用作呼吸面具和潜艇的供氧剂,写出其与水反应的化学方程式
(6)用⑥氯气和石灰乳可以制取漂白粉,漂白粉在空气中生成
 的化学方程式为
的化学方程式为
更新时间:2023/12/11 19:41:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
(1)下列制备氢氧化铁胶体的操作方法正确的是____________ (填字母);
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c. 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液
d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式__________________________ ;
(3)下列与胶体性质无关的是_____________ (填字母);
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫_____________ 。
(1)下列制备氢氧化铁胶体的操作方法正确的是
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c.
 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式
(3)下列与胶体性质无关的是
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某课外活动小组进行 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。
(1)若将 溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
(2)根据质量守恒定律,写出制备 胶体的化学反应方程式
胶体的化学反应方程式___________ ;
(3)取少量制得的胶体加入试管中,再加入少量 溶液,观察到的现象
溶液,观察到的现象___________ ;
(4) 胶体区别于
胶体区别于 溶液最本质的特征是___________;(填序号)
溶液最本质的特征是___________;(填序号)
(5)下列应用或事实与胶体的性质没有关系的是___________;(填序号)
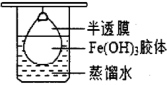
(6)将用(1)用正确方法制得的氢氧化铁胶体,放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察到___________ (填“有”或“无”)丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为___________ 。
 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。(1)若将
 溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)
溶液分别滴入下列物质中,能形成胶体的是___________;(填序号)| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
 胶体的化学反应方程式
胶体的化学反应方程式(3)取少量制得的胶体加入试管中,再加入少量
 溶液,观察到的现象
溶液,观察到的现象(4)
 胶体区别于
胶体区别于 溶液最本质的特征是___________;(填序号)
溶液最本质的特征是___________;(填序号)A. 胶体粒子的直径在1~100nm之间 胶体粒子的直径在1~100nm之间 |
B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 |
D. 胶体的分散质粒子能透过滤纸 胶体的分散质粒子能透过滤纸 |
| A.用明矾净化饮用 |
B.在 溶液中滴加NaOH溶液出现红褐色沉淀 溶液中滴加NaOH溶液出现红褐色沉淀 |
| C.在河流入海处易形成沙洲 |
| D.用石膏或盐卤点制豆腐 |

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十种物质:①盐酸;②小苏打;③硫酸亚铁;④二氧化碳;⑤蔗糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩饱和氯化铁溶液。
(1)上述十种物质中,属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(2)上述物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,发生该反应的两种物质为_______ (填序号)。
(3)在空气中向③的溶液中加入⑥的溶液,观察到的现象为_______ ,请用化学方程式解释产生该现象的原因_______ 。
(4)若在⑦中逐滴加入①至过量,产生的现象为_______ 。
(1)上述十种物质中,属于电解质的有
(2)上述物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,发生该反应的两种物质为
(3)在空气中向③的溶液中加入⑥的溶液,观察到的现象为
(4)若在⑦中逐滴加入①至过量,产生的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填空:
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是___________ 。属于电解质的是___________ 。属于非电解质的是___________ 。
(2)向 沸水中加入
沸水中加入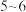 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体,生成胶体的化学方程式为___________ 。
(3)已知:Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
可推知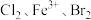 氧化性由强到弱为
氧化性由强到弱为___________ 。若反应Ⅰ中共转移 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为___________ 。
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是
(2)向
 沸水中加入
沸水中加入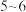 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)已知:Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。可推知
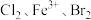 氧化性由强到弱为
氧化性由强到弱为 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下几种物质:①铁丝,②液态HCl;③75%酒精溶液;④稀盐酸;⑤H2SO4;⑥NaOH固体;⑦熔融KNO3。
(1)以上物质属于单质的是___________ (填序号,下同),属于电解质的是___________ 。
(2)①与⑤的稀溶液反应的化学方程式为___________ 。
(3)⑦的电离方程式为___________ 。
(4)在发生离子反应的反应物或生成物中,一定存在的是___________(填字母)。
(5)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
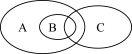
①下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___________ (填字母)。
②有同学认为所有酸碱中和反应均可表示为 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)___________ 。
(1)以上物质属于单质的是
(2)①与⑤的稀溶液反应的化学方程式为
(3)⑦的电离方程式为
(4)在发生离子反应的反应物或生成物中,一定存在的是___________(填字母)。
| A.单质 | B.氧化物 | C.酸 | D.化合物 |
(5)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
①下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是

②有同学认为所有酸碱中和反应均可表示为
 。请举个例子反驳上述观点(用离子方程式表示)
。请举个例子反驳上述观点(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下物质:
①NaOH溶液 ②液氨 ③BaCO3固体 ④NaHSO4溶液 ⑤Fe(OH)3胶体
⑥铜 ⑦CO2 ⑧醋酸(CH3COOH) ⑨饱和NaHCO3溶液
(1)上述物质中属于电解质的是________ (英字号,下同),能导电的是________ 。
(2)写出④和⑨反应的离子方程式________ 。
(3)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为________ 。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是________ 。
①NaOH溶液 ②液氨 ③BaCO3固体 ④NaHSO4溶液 ⑤Fe(OH)3胶体
⑥铜 ⑦CO2 ⑧醋酸(CH3COOH) ⑨饱和NaHCO3溶液
(1)上述物质中属于电解质的是
(2)写出④和⑨反应的离子方程式
(3)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】科学的分类能够反映事物的本质特征,运用分类的方法,可以发现物质及其变化的规律。基于物质类别和元素价态,可以设计物质间转化的途径。请根据下列物质回答相关问题:
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是_______ (填序号)
(2)Ⅰ.某同学用含钠元素的不同类别 物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2 2NaCl
2NaCl
b.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:_______ ;d:_______ 。
Ⅱ.另一位同学从含氯元素的不同价态 考虑,认为Cl2与NaOH溶液反应也可以生成NaCl,请写出此方法的化学反应方程式_______ 。
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为_______ ;请用单线桥法 在离子反应方程式上标出电子转移的方向和数目_______ 。
①小苏打 ②石墨 ③HCl ④酒精 ⑤FeCl3溶液 ⑥氧化钠
(1)上述物质中属于电解质的是
(2)Ⅰ.某同学用
a.2Na+Cl2
 2NaCl
2NaClb.
c.NaOH+HCl=NaCl+H2O
d.
请从上述①~⑥中选择合适反应物补充b、d反应的化学反应方程式b:
Ⅱ.另一位同学从
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,工业上制备Na2FeO4有多种方法,其中一种方法是用NaClO和⑤作为反应物在碱性环境下完成,此方法的化学原理可用离子反应方程式表示为:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】消毒液在我们日常生活中必不可少,请结合相关知识回答下列问题。
(1)生产消毒液时将氯气通入NaOH溶液中,发生反应的离子方程式为__ 。
(2)取少量消毒液滴加到AgNO3溶液中,现象是出现白色沉淀,说明消毒液中有____ 。
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的离子反应方程式:___________ ;
该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学反应方程式:_______________ 。
(1)生产消毒液时将氯气通入NaOH溶液中,发生反应的离子方程式为
(2)取少量消毒液滴加到AgNO3溶液中,现象是出现白色沉淀,说明消毒液中有
(3)消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的离子反应方程式:
该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
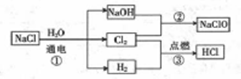
【推荐3】次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-
(1)Cl 元素位于元素周期表第______ 周期___ 族。
(2)写出NaOH的电子式:__________ 。
(3)写出反应②的化学方程式:_______________ 。该反应中每生成1mol NaClO时,转移______ mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________ (用离子方程式表示)。
-

(1)Cl 元素位于元素周期表第
(2)写出NaOH的电子式:
(3)写出反应②的化学方程式:
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题
(1)漂白粉主要成分的化学式:___________ ;
(2)84消毒液和洁厕灵混用产生毒气(离子方程式表示)原理:___________ ;
(3)小苏打用于治疗胃酸过多的离子方程式:___________ ;
(4)过氧化钠加入硫酸铜溶液中的离子方程式;___________ ;
(5)铁和水蒸气反应的化学方程式:___________ 。
(1)漂白粉主要成分的化学式:
(2)84消毒液和洁厕灵混用产生毒气(离子方程式表示)原理:
(3)小苏打用于治疗胃酸过多的离子方程式:
(4)过氧化钠加入硫酸铜溶液中的离子方程式;
(5)铁和水蒸气反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为__ ,其中NaH作__ 剂(填“氧化”或“还原”)
(2)HCO 与H+或OH-在溶液都不能大量共存,试用离子方程式说明原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明原因:__ ;__ 。
(3)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其与人呼出的CO2反应的化学方程式__ 。
(4)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为__ 。
(2)HCO
 与H+或OH-在溶液都不能大量共存,试用离子方程式说明原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明原因:(3)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其与人呼出的CO2反应的化学方程式
(4)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为
您最近一年使用:0次

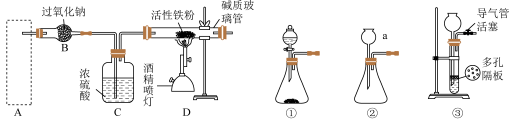
 最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。
最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。