题型:解答题-结构与性质
难度:0.4
引用次数:139
题号:21388522
我国的航空航天事业取得了举世瞩目的成就,近年来硼氢类离子液体作为火箭推进剂燃料得到了广泛使用。硼氢类离子液体的合成如图所示:
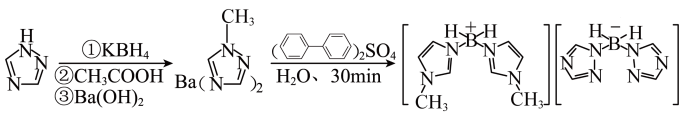
回答下列问题:
(1)基态K原子核外电子的空间运动状态有___________ 种。
(2)C、O、N的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3) 中,
中, 的空间构型为
的空间构型为___________ 。
(4)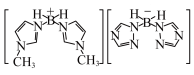 中
中不存在 的作用力有___________ (填字母)。
a.离子键 b.配位键 c. 键 d.
键 d. 键 e.金属键 f.氢键
键 e.金属键 f.氢键
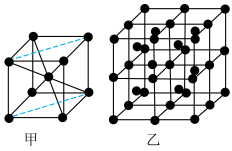
(5)Ba的一种晶体如甲、乙所示,若按甲虚线方向切乙,所得剖面图正确的是___________(填字母标号)。
(6)硼化钙晶胞结构如图所示,B原子构成B6八面体,各个顶点通过B-B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca2+,晶胞密度为ρg·cm-3。
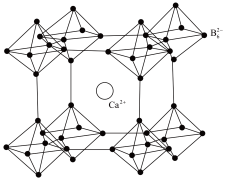
①硼化钙的化学式为___________ 。
②晶胞边长为___________ nm(已知NA为阿伏加德罗常数)。

回答下列问题:
(1)基态K原子核外电子的空间运动状态有
(2)C、O、N的第一电离能由大到小的顺序为
(3)
 中,
中, 的空间构型为
的空间构型为(4)
 中
中a.离子键 b.配位键 c.
 键 d.
键 d. 键 e.金属键 f.氢键
键 e.金属键 f.氢键(5)Ba的一种晶体如甲、乙所示,若按甲虚线方向切乙,所得剖面图正确的是___________(填字母标号)。

A.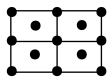 | B.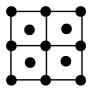 | C.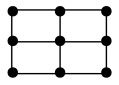 | D. |
(6)硼化钙晶胞结构如图所示,B原子构成B6八面体,各个顶点通过B-B键互相连接成三维骨架,八个B6多面体围成立方体,中心为Ca2+,晶胞密度为ρg·cm-3。

①硼化钙的化学式为
②晶胞边长为
更新时间:2024/01/09 11:47:09
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】氮、磷化合物在科研和生产中有许多重要用途。回答下列问题:
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为_________ ,H、B、N的电负性由大到小的顺序为____ 。与氨硼烷互为等电子体的分子是_______ (写名称),其熔点比NH3BH3低,原因是__________ 。
(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状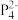 结构与苯相似,
结构与苯相似,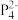 中的大π键可表示为
中的大π键可表示为___________ 。
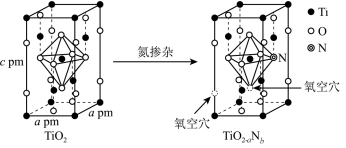
___ 种,TiO2晶胞的密度为_________ g/cm3,TiO2-aNb 晶体中a:b=_________ 。
(1)氨硼烷(NH3BH3)是极具潜力的固体储氢材料,分子中与N原子相连的H呈正电性(H
 +),与B原子相连的H呈负电性(H
+),与B原子相连的H呈负电性(H -)。B原子的杂化方式为
-)。B原子的杂化方式为(2)南开大学某课题组成功合成[FeP6]2-。结构如图,环状
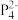 结构与苯相似,
结构与苯相似,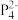 中的大π键可表示为
中的大π键可表示为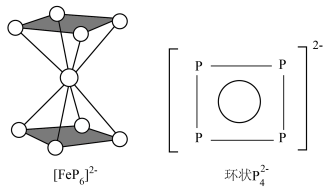
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】2019 年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2和 LiMnO2等都是他们研究锂离子电池的载体。回答下列问题:
(1)基态 Ti 原子的价层电子排布图为____ 。
(2)在第四周期 d 区元素中,与 Ti 原子未成对电子数相同的元素名称________ 。
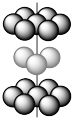
(3)金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为______ 。
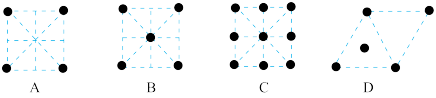
(4)已知第三电离能数据:I3(Mn)=3246 kJ·mol-1,I3(Fe)=2957 kJ·mol-1。锰的第三电离能大于铁的第三电离能,其主要原因是______ 。
(5)据报道,在 MnO2的催化下,甲醛可被氧化成 CO2,在处理含 HCHO 的废水或空气方面有广泛应用。HCHO中键角________ CO2中键角(填“大于”“小于”或“等于”)。
(6)Co3+、Co2+能与 NH3、H2O、SCN-等配体组成配合物。
①1 mol[ Co(NH3)6]3+含______ mol σ键。
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N] -,SCN-与金属离子形成的配离子中配位原子是_______ (填元素符号)。
(7)工业上,采用电解熔融氯化锂制备锂,钠还原 TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为 605℃、-24℃,它们的熔点相差很大,其主要原因是________ 。
(8)钛的化合物晶胞如图所示。
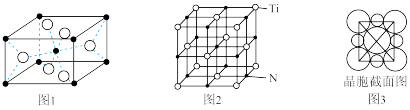
二氧化钛晶胞如图 1 所示,钛原子配位数为______ 。氮化钛的晶胞如图 2 所示, 图 3 是氮化钛的晶胞截面图(相邻原子两两相切)。已知:NA是阿伏加 德罗常数的值,氮化钛晶体密度为 d g·cm-3。氮化钛晶胞中 N 原子半径为________ pm。
(1)基态 Ti 原子的价层电子排布图为
(2)在第四周期 d 区元素中,与 Ti 原子未成对电子数相同的元素名称
(3)金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为


(4)已知第三电离能数据:I3(Mn)=3246 kJ·mol-1,I3(Fe)=2957 kJ·mol-1。锰的第三电离能大于铁的第三电离能,其主要原因是
(5)据报道,在 MnO2的催化下,甲醛可被氧化成 CO2,在处理含 HCHO 的废水或空气方面有广泛应用。HCHO中键角
(6)Co3+、Co2+能与 NH3、H2O、SCN-等配体组成配合物。
①1 mol[ Co(NH3)6]3+含
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N] -,SCN-与金属离子形成的配离子中配位原子是
(7)工业上,采用电解熔融氯化锂制备锂,钠还原 TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为 605℃、-24℃,它们的熔点相差很大,其主要原因是
(8)钛的化合物晶胞如图所示。

二氧化钛晶胞如图 1 所示,钛原子配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】近年来我国航天事业成果显著,其制造材料中包含了铝、镁、锌、钛、锰、铜、镍、铬、硅、氮、氧等多种元素。回答下列问题:
(1)铬元素属于周期表中_______ 区的元素,其基态原子核外电子空间运动状态有_______ 种,
(2)钛能形成多种配合物,如Ti(CO)6、[Ti(H2O)6]Cl3、[Ti(NH3)6]Cl3等。其配合物的配位数均为_______ ,其中配位原子的电负性由小到大的顺序是_______ (写元素符号),[Ti(NH3)6]Cl3中∠H-N-H_______ (填“大于”、“小于”或“等于”)单个氨气分子中∠H-N-H,原因是_______ 。
(3)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为_______ 。
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为_______ ,其配位数为_______ 。已知晶胞参数为a pm,设阿伏加德罗常数的值为NA,晶胞密度
_______  。(列出计算式即可)
。(列出计算式即可)

(1)铬元素属于周期表中
(2)钛能形成多种配合物,如Ti(CO)6、[Ti(H2O)6]Cl3、[Ti(NH3)6]Cl3等。其配合物的配位数均为
(3)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为

 。(列出计算式即可)
。(列出计算式即可) 
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题:
(1)基态Zn原子的价电子轨道表达式为_____ ;基态N原子中未成对电子数为_____ 。
(2)O的第一电离能小于N的第一电离能的原因为_____ ;NH4HF2的组成元素的电负性由大到小的顺序为_____ (用元素符号表示)。
(3)K2CO3中阴离子的立体构型为_____ ;其中C原子的杂化方式为_____ ;HF的沸点远大于HCl的原因是_____ 。
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:
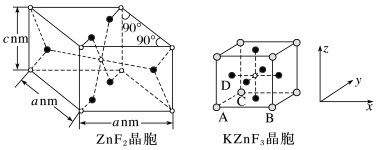
①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为_____ 。
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为_____ g•cm-3(用含a、c、NA的代数式表示)。
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为_____ 。
(1)基态Zn原子的价电子轨道表达式为
(2)O的第一电离能小于N的第一电离能的原因为
(3)K2CO3中阴离子的立体构型为
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】硫、铁及其化合物用途非常广泛。回答下列问题:
(1)基态S原子价电子排布式为________ ,基态Fe原子未成对电子数为________ 个。
(2)团簇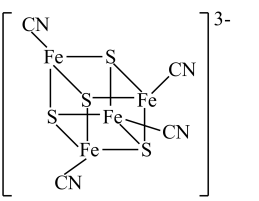 中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为
中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为________ ;与铁形成配位键的原子是________ 。
(3)工业上主要通过反应SO3+SCl2=SOCl2+SO2制备SOCl2(氯化亚砜),上述四种分子中,属于非极性分子的是________ ;SCl2分子空间构型为________ 形;SOCl2分子中心原子杂化方式是________ 。
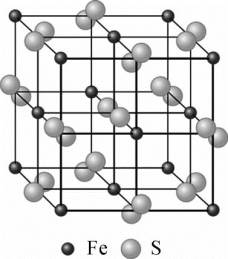
(4)黄铁矿的晶体结构如图所示,已知黄铁矿晶胞参数为a=0.5417nm,阿伏伽德罗常数的值为NA。则黄铁矿的密度为________ g·cm-3(列出计算式)。
(1)基态S原子价电子排布式为
(2)团簇
 中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为
中,S、C、N的化合价依次为-2、+2、-3,Fe2+与Fe3+数目之比为(3)工业上主要通过反应SO3+SCl2=SOCl2+SO2制备SOCl2(氯化亚砜),上述四种分子中,属于非极性分子的是
(4)黄铁矿的晶体结构如图所示,已知黄铁矿晶胞参数为a=0.5417nm,阿伏伽德罗常数的值为NA。则黄铁矿的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】甲硅烷 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。
(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si___________ H(填“>”“<”或“=”), 分子的空间结构名称为
分子的空间结构名称为___________ 。
(2)利用 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。 中
中 的键角
的键角___________  中
中 的键角(填“>”“<”或“=”),其键角差异的原因是
的键角(填“>”“<”或“=”),其键角差异的原因是___________ 。
(3)利用 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。

①热稳定性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②碳化硅晶体中每个Si原子周围距离最近的C原子数目为___________ ,SiC的晶体类型是___________ 。
③已知碳化硅的晶胞边长为a nm(1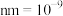 m),阿伏伽德罗常数为
m),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为___________ g⋅cm-3(列出计算式)。
④硅、金刚石和碳化硅晶体的熔点从高到低依次是___________ 。
(4)硅元素最高价氧化物对应的水化物为原硅酸( )。
)。
资料:原硅酸( )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
①原硅酸钠( )溶液吸收空气中的
)溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:___________ 。
②从结构的角度解释 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:___________ 。
 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si
 分子的空间结构名称为
分子的空间结构名称为(2)利用
 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。 中
中 的键角
的键角 中
中 的键角(填“>”“<”或“=”),其键角差异的原因是
的键角(填“>”“<”或“=”),其键角差异的原因是(3)利用
 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
①热稳定性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②碳化硅晶体中每个Si原子周围距离最近的C原子数目为
③已知碳化硅的晶胞边长为a nm(1
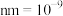 m),阿伏伽德罗常数为
m),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为④硅、金刚石和碳化硅晶体的熔点从高到低依次是
(4)硅元素最高价氧化物对应的水化物为原硅酸(
 )。
)。资料:原硅酸(
 )可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。
)可溶于水,原硅酸中的羟基可发生分子间脱水,逐渐转化为硅酸、硅胶。①原硅酸钠(
 )溶液吸收空气中的
)溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:②从结构的角度解释
 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:

(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________ ,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________ 。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________ ,H3BO3晶体中B原子个数与极性键个数比为________ 。
(3)三种晶体中熔点最低的是________ ,其晶体受热熔化时,克服的微粒之间的相互作用为________________________________________________________________ 。
(4)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为________ g·cm-3。

(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是
(3)三种晶体中熔点最低的是
(4)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】最近James A. Dumesic等研究了负载于TiO2和SiO2表面的Ag-Pd、Cu-Pd合金催化剂对乙炔选择性加氢反应的情况。回答下列问题:
(1)基态Ti、Cu的未成对电子数之比为______ ;基态Si原子的价电子排布式为______ 。
(2)Ag和Cu均位于元素周期表中第I B族,Cu的熔点比Ag的高,硬度比Ag的大,其原因是_______ 。
(3)SiO2中所含共价键的类型是______ (填“σ键”或“π键”)。
(4)乙炔、乙烯中中心原子的杂化方式依次为______ 、______ ,乙炔的空间构型为______ 。
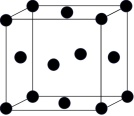
(5)某铜钯合金CuPdx可看作铜晶胞中的两个顶点上的Cu原子被Pd原子取代(如图),则x=______ 。
(1)基态Ti、Cu的未成对电子数之比为
(2)Ag和Cu均位于元素周期表中第I B族,Cu的熔点比Ag的高,硬度比Ag的大,其原因是
(3)SiO2中所含共价键的类型是
(4)乙炔、乙烯中中心原子的杂化方式依次为
(5)某铜钯合金CuPdx可看作铜晶胞中的两个顶点上的Cu原子被Pd原子取代(如图),则x=

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】科学家开发了一种氮掺杂氢化镥(Lu—N—H)材料,在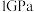 压强下,表现出室温(20℃)超导特性。回答下列问题:
压强下,表现出室温(20℃)超导特性。回答下列问题:
(1)已知基态Lu(镥)原子的价层电子排布式为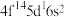 ,它位于元素周期表第
,它位于元素周期表第___________ 周期第___________ 族,有___________ 个未成对电子。
(2)氮族氢化物中,沸点最低的是___________ (填化学式), 的沸点高于
的沸点高于 ,其主要原因是
,其主要原因是___________ 。
(3)一种新药的活性成分的结构简式如图所示。1个该分子含___________ 个手性碳原子。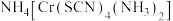 ,其常作分析试剂。
,其常作分析试剂。
①雷氏盐中阳离子的空间结构为___________ ,阴离子中配位原子是___________ (填元素符号)。
②预测:雷氏盐中阴离子的空间结构最可能是___________ (填标号)。 ,
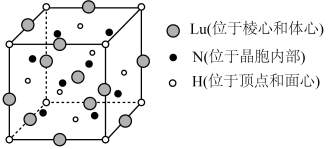
, 代表阿伏加德罗常数的值。在该晶胞中,有
代表阿伏加德罗常数的值。在该晶胞中,有___________ 个Lu原子与H原子等距离且最近。该晶体的密度为___________  。
。
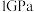 压强下,表现出室温(20℃)超导特性。回答下列问题:
压强下,表现出室温(20℃)超导特性。回答下列问题:(1)已知基态Lu(镥)原子的价层电子排布式为
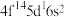 ,它位于元素周期表第
,它位于元素周期表第(2)氮族氢化物中,沸点最低的是
 的沸点高于
的沸点高于 ,其主要原因是
,其主要原因是(3)一种新药的活性成分的结构简式如图所示。1个该分子含
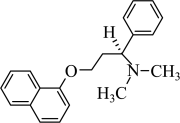
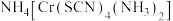 ,其常作分析试剂。
,其常作分析试剂。①雷氏盐中阳离子的空间结构为
②预测:雷氏盐中阴离子的空间结构最可能是
A.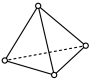 B.
B.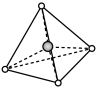 C.
C.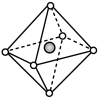 D.
D.
 ,
, 代表阿伏加德罗常数的值。在该晶胞中,有
代表阿伏加德罗常数的值。在该晶胞中,有 。
。
您最近一年使用:0次



