黄铜矿主要成分为 ,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
(1)“溶浸”时,需要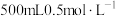 硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为
硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为 的浓硫酸的体积为
的浓硫酸的体积为______ mL(计算结果保留一位小数),“溶浸”时被氧化的元素为_______ (填元素符号)。
(2)“分离Cu”时,Fe与 反应的离子方程式为
反应的离子方程式为________ ,该过程中分离出Fe、Cu的操作名称为_______ 。
(3)“氧化”时,温度不能太高,原因是________ ,反应过程中,参加反应的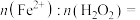
______ 。
(4)硫酸铁铵晶体[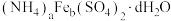 ]组成的测定
]组成的测定
步骤1:准确称取质量为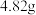 固体在酸性条件下溶于水配成
固体在酸性条件下溶于水配成 溶液A;
溶液A;
步骤2:取 溶液A,加入足量的
溶液A,加入足量的 溶液,过滤得
溶液,过滤得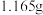 沉淀;
沉淀;
步骤3:取 溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得
溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得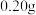 固体。
固体。
通过上述步骤,计算确定该晶体的化学式为___________ 。
 ,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下:
,某研究团队利用氧化亚铁硫杆菌溶浸,通过系列操作可获得铜和硫酸铁铵晶体。工艺流程如下: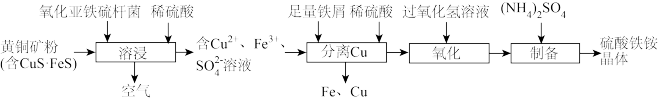
(1)“溶浸”时,需要
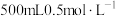 硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为
硫酸溶液,在配制硫酸溶液时:所需质量分数为98%、密度为 的浓硫酸的体积为
的浓硫酸的体积为(2)“分离Cu”时,Fe与
 反应的离子方程式为
反应的离子方程式为(3)“氧化”时,温度不能太高,原因是
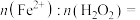
(4)硫酸铁铵晶体[
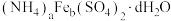 ]组成的测定
]组成的测定步骤1:准确称取质量为
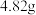 固体在酸性条件下溶于水配成
固体在酸性条件下溶于水配成 溶液A;
溶液A;步骤2:取
 溶液A,加入足量的
溶液A,加入足量的 溶液,过滤得
溶液,过滤得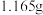 沉淀;
沉淀;步骤3:取
 溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得
溶液A,加入足量氢氧化钠溶液,过滤,洗涤并灼烧得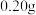 固体。
固体。通过上述步骤,计算确定该晶体的化学式为
更新时间:2024/01/30 13:46:34
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】有一包粉末可能含有K+、Fe3+、Al3+、Cl﹣、SO42﹣、CO32﹣中的若干种,现进行以下实验:
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后,滤液呈中性,在滤液中滴入AgNO3溶液,有白色沉淀生成;
③取②中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤.往得到的沉淀中加入过量的NaOH溶液,沉淀减少.
(1)根据上述实验,这包粉末中一定不含有的离子是_______ ,肯定含有的离子是_______ ,不能确定是否含有的离子是________ ,可通过___________ 实验来进一步确定该离子.
(2)写出⑤中生成有色沉淀反应的离子方程式:___________
(3)写出⑤中沉淀减少反应的离子方程式:______________________ .
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后,滤液呈中性,在滤液中滴入AgNO3溶液,有白色沉淀生成;
③取②中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤.往得到的沉淀中加入过量的NaOH溶液,沉淀减少.
(1)根据上述实验,这包粉末中一定不含有的离子是
(2)写出⑤中生成有色沉淀反应的离子方程式:
(3)写出⑤中沉淀减少反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】有一瓶澄清的溶液,其中可能含有H+、NH4+、K+、Al3+、Mg2+、Ba2+、Fe3+、SO42-、CO32-和I-。取该溶液进行以下实验:
①用pH试纸检验,溶液呈酸性;
②取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;
③另取部分溶液,加入稀NaOH溶液使其变为碱性,溶液中始终无沉淀生成;
④取部分上述碱性溶流,加Na2CO3溶液有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
(1)根据上述实验事实,该溶液中肯定存在的离子是_________ ;肯定不存在的离子是______ 。
(2)对于不确定是否存在的离子,应用___________ 方法进行检验。
(3)实验②中发生反应的离子方程式为____________________ 。
(4)实验④中发生反应的离子方程式为____________________ 。
①用pH试纸检验,溶液呈酸性;
②取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;
③另取部分溶液,加入稀NaOH溶液使其变为碱性,溶液中始终无沉淀生成;
④取部分上述碱性溶流,加Na2CO3溶液有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
(1)根据上述实验事实,该溶液中肯定存在的离子是
(2)对于不确定是否存在的离子,应用
(3)实验②中发生反应的离子方程式为
(4)实验④中发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示:
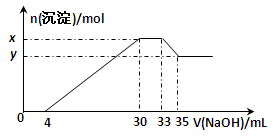
请回答:
(1)x与y的差值为_____________ mol。
(2)原溶液的pH=_____________ 。
(3)原溶液中n(Mg2+)∶n(Al3+)=_____________ 。
(4)原溶液中c(Cl-)=______________ mol·L-1。
(5)写出所加氢氧化钠溶液的体积33~35mL发生反应的离子方程式_____________ 。

请回答:
(1)x与y的差值为
(2)原溶液的pH=
(3)原溶液中n(Mg2+)∶n(Al3+)=
(4)原溶液中c(Cl-)=
(5)写出所加氢氧化钠溶液的体积33~35mL发生反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】辉铜矿主要成分Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,以及少量SiO2、Fe2O3等杂质。研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰和碱式碳酸铜。主要工艺流程如下:
已知:①MnO2有较强的氧化性,能将Cu+氧化成Cu2+
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4。
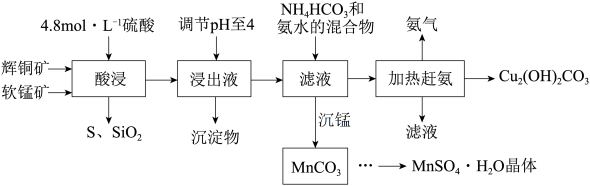
(1)实验室配制250mL 4.8 mol/L的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要_______ 。
(2)酸浸时,为了提高浸取率可采取的措施有_______ (任写一点)。
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式_______ 。
(4)调节浸出液pH=4的作用是_______ 。
(5)本工艺中可循环使用的物质是(写化学式)_______ 。
(6)获得的MnSO4·H2O晶体后常用酒精洗涤,优点是_______ 。
(7)用标准的BaCl2溶液测定样品中MnSO4·H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略)其可能原因有_______ (任写一种)。
已知:①MnO2有较强的氧化性,能将Cu+氧化成Cu2+
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4。

(1)实验室配制250mL 4.8 mol/L的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要
(2)酸浸时,为了提高浸取率可采取的措施有
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式
(4)调节浸出液pH=4的作用是
(5)本工艺中可循环使用的物质是(写化学式)
(6)获得的MnSO4·H2O晶体后常用酒精洗涤,优点是
(7)用标准的BaCl2溶液测定样品中MnSO4·H2O质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略)其可能原因有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正极主要由LiFePO4、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下:
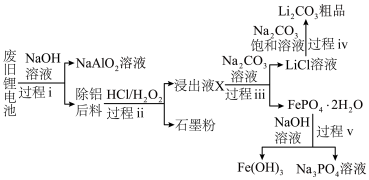
(1)过程ⅰ生成NaAlO2溶液的离子方程式是__ 。
(2)过程ⅱ中HCl/H2O2的作用是__ 。
(3)浸出液X的主要成分为 Li+、Fe3+、H2PO4-等。过程ⅲ控制碳酸钠溶液浓度20%、温度85 ℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。
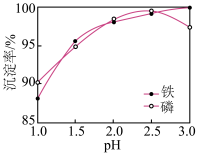
①综合考虑铁和磷沉淀率,最佳pH为__ 。
②结合平衡移动 原理,解释过程ⅲ中pH增大,铁和磷沉淀率增大的原因__ 。
③当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因__ 。
(4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为__ 。

(1)过程ⅰ生成NaAlO2溶液的离子方程式是
(2)过程ⅱ中HCl/H2O2的作用是
(3)浸出液X的主要成分为 Li+、Fe3+、H2PO4-等。过程ⅲ控制碳酸钠溶液浓度20%、温度85 ℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。

①综合考虑铁和磷沉淀率,最佳pH为
②结合
③当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因
(4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】由钛白副产硫酸亚铁[主要成分是 ,还含有
,还含有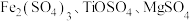 ]制备锂离子电池正极材料的前驱体
]制备锂离子电池正极材料的前驱体 的工艺流程如下图所示:
的工艺流程如下图所示: ,各微粒浓度如下表所示。
,各微粒浓度如下表所示。
②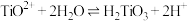 ,
, 时,
时, 沉淀完全;
沉淀完全;
③ ;
;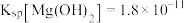 ;
;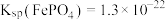 。
。
请回答下列问题:
(1)“除杂过滤”工序中,将 转化为
转化为 除去。
除去。
①加入铁粉的作用是___________ 。
②当 沉淀完全时,滤渣中是否含有
沉淀完全时,滤渣中是否含有 ,请通过计算说明
,请通过计算说明___________ 。
(2)“结晶过滤”时获得的固体是 。请补充完整下列制备方案:将“除杂过滤”后的滤液
。请补充完整下列制备方案:将“除杂过滤”后的滤液___________ ,得 粗产品,多次重结晶、过滤、洗涤、干燥,制得较为纯净的
粗产品,多次重结晶、过滤、洗涤、干燥,制得较为纯净的 (
( 的溶解度随温度变化的曲线如图所示)。
的溶解度随温度变化的曲线如图所示)。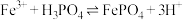 。加入氨水的目的是
。加入氨水的目的是___________ 。
(4)工业上可用电解磷铁渣(主要含 等)制备
等)制备 ,电解原理如图所示。
,电解原理如图所示。___________ 极。
②生成 的电极反应式为
的电极反应式为___________ 。
 ,还含有
,还含有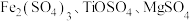 ]制备锂离子电池正极材料的前驱体
]制备锂离子电池正极材料的前驱体 的工艺流程如下图所示:
的工艺流程如下图所示:
 ,各微粒浓度如下表所示。
,各微粒浓度如下表所示。| 微粒 |  元素 元素 |  |  |
浓度 | 1.7 | 0.0043 | 0.07 |
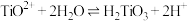 ,
, 时,
时, 沉淀完全;
沉淀完全;③
 ;
;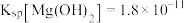 ;
;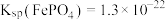 。
。请回答下列问题:
(1)“除杂过滤”工序中,将
 转化为
转化为 除去。
除去。①加入铁粉的作用是
②当
 沉淀完全时,滤渣中是否含有
沉淀完全时,滤渣中是否含有 ,请通过计算说明
,请通过计算说明(2)“结晶过滤”时获得的固体是
 。请补充完整下列制备方案:将“除杂过滤”后的滤液
。请补充完整下列制备方案:将“除杂过滤”后的滤液 粗产品,多次重结晶、过滤、洗涤、干燥,制得较为纯净的
粗产品,多次重结晶、过滤、洗涤、干燥,制得较为纯净的 (
( 的溶解度随温度变化的曲线如图所示)。
的溶解度随温度变化的曲线如图所示)。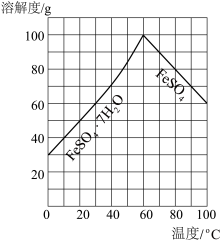
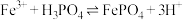 。加入氨水的目的是
。加入氨水的目的是(4)工业上可用电解磷铁渣(主要含
 等)制备
等)制备 ,电解原理如图所示。
,电解原理如图所示。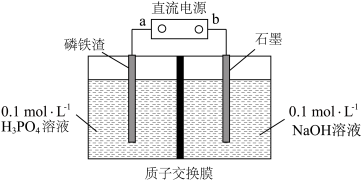
②生成
 的电极反应式为
的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】V2O5(五氧化二钒)可作为化学工业中的催化剂,广泛用于冶金化工等行业,工业上以含钒废料(含有V2O3、Fe2O3、Al2O3、CuO、有机物等)来制备V2O5的一种工艺流程如下:

已知:Ⅰ.含钒离子在溶液中的主要存在形式与溶液pH的关系:
Ⅱ.25°C时,难溶电解质的溶度积常数如下表所示:
Ⅲ. NH4VO3是白色粉末,微溶于冷水,可溶于热水。
回答下列问题:
(1)“焙烧”过程中除了V2O3、Fe2O3、Al2O3、CuO中的物质参加反应外,“焙烧”的另外一个作用为_______ 。
(2)“调pH”的作用除了沉淀某些阳离子外,还有_______ 。
(3)常温下,加适量的氨水调节pH得到滤渣1,若“调pH”为6.5,则Al3+_______ 沉淀完全(填“已”或“未”) (离子浓度≤1.0× 10-5mol·L-1,认为沉淀完全)。
(4)若“净化II”时直接加入足量的( NH4)2CO3,可能导致的后果为_______ 。写出一种与 空间结构相同的分子和离子
空间结构相同的分子和离子_______ 。
(5)“洗涤”NH4VO3沉淀时可选用的洗涤剂为_______ (填“热水”或“冷水”)。
(6)“煅烧”时,除生成V2O5外,还生成参与大气循环的气体,该反应的氧化剂和还原剂的物质的量之比为_______ 。

已知:Ⅰ.含钒离子在溶液中的主要存在形式与溶液pH的关系:
| pH | 4~6 | 6~8 | 8~10 |
| 主要离子 |  |  |  |
| 难溶电解质 | Cu(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| Ksp | 2.2×10- 20 | 4.0×10-38 | 1.3×10-33 | 1.8×10-11 |
回答下列问题:
(1)“焙烧”过程中除了V2O3、Fe2O3、Al2O3、CuO中的物质参加反应外,“焙烧”的另外一个作用为
(2)“调pH”的作用除了沉淀某些阳离子外,还有
(3)常温下,加适量的氨水调节pH得到滤渣1,若“调pH”为6.5,则Al3+
(4)若“净化II”时直接加入足量的( NH4)2CO3,可能导致的后果为
 空间结构相同的分子和离子
空间结构相同的分子和离子(5)“洗涤”NH4VO3沉淀时可选用的洗涤剂为
(6)“煅烧”时,除生成V2O5外,还生成参与大气循环的气体,该反应的氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是_______ (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。溴歧化为Br-和BrO3-并没有产生CO2则反应的离子反应方程式为_______ 。
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的阳离子_______ ,获得产品2的离子反应方程式为_______ ,浓海水的利用率为90%,则1 L浓海水最多可得到产品2的质量为_______ g。
(4)由MgCl2·6H2O制备MgCl2时,往往在HCl的气体氛围中加热。其目的是_______ 。
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。溴歧化为Br-和BrO3-并没有产生CO2则反应的离子反应方程式为
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)由MgCl2·6H2O制备MgCl2时,往往在HCl的气体氛围中加热。其目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如下图所示。

已知:i.PbCl2微溶于水
ii.PbCl2(s)+2Cl-(aq) PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
(1)浸取过程中MnO2与PbS发生如下反应,请将离子反应补充完整并配平:_____
______+___Cl-+___PbS+___MnO2=___PbCl2+__SO42-+_____ +_____
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是__________ 。
(3)调pH的目的是____________ 。
(4)沉降池中获得PbCl2采取的措施有_________ 。
(5)通过电解酸性废液可重新获得MnO2,装置示意图如下:
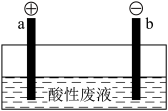
①在_____ 极(填“a”或“b”)获得MnO2,电极反应为_______________ 。
②电解过程中发现有Cl2产生,原因可能是_____________ (用化学用语表示)。

已知:i.PbCl2微溶于水
ii.PbCl2(s)+2Cl-(aq)
 PbCl42-(aq)△H>0
PbCl42-(aq)△H>0(1)浸取过程中MnO2与PbS发生如下反应,请将离子反应补充完整并配平:
______+___Cl-+___PbS+___MnO2=___PbCl2+__SO42-+_____ +_____
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是
(3)调pH的目的是
(4)沉降池中获得PbCl2采取的措施有
(5)通过电解酸性废液可重新获得MnO2,装置示意图如下:

①在
②电解过程中发现有Cl2产生,原因可能是
您最近一年使用:0次



