制取Fe(OH)3胶体的方案如下:向40mL沸腾的蒸馏水中滴入5滴饱和FeCl3溶液(质量分数约为30%)___________ 判断溶液中是否成功制备胶体,能产生该现象的原因是胶体粒子对光波的___________ 所致。
(2)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为___________ ,反应方程式为___________ 。
(3)制得的Fe(OH)3胶体中往往混有 和
和 ,可以利用
,可以利用___________ 的方法来提纯Fe(OH)3胶体。
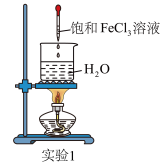
(2)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为
(3)制得的Fe(OH)3胶体中往往混有
 和
和 ,可以利用
,可以利用
更新时间:2024/04/10 20:54:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案并记录了实验现象:取少量Na2CO3固体,加入无水酒精,充分振荡、静置,取上层清液,滴加酚酞试液,溶液仍为无色,然后加入少量水,溶液变为红色。向该红色溶液中滴加足量BaCl2溶液(中性),红色褪去。
(1)该实验表明,Na2CO3溶液显碱性的原因是____ (填代号)。
A.Na2CO3提供Na+
B.Na2CO3提供CO
C.Na2CO3提供OH-
D.CO 与水反应生成OH-
与水反应生成OH-
(2)从形成盐的酸和碱的强弱角度看,Na2CO3属于____ (填代号)。
A.强酸强碱盐 B.强酸弱碱盐 C.弱酸强碱盐 D.弱酸弱碱盐
(3)结合BaCl2溶液呈中性,可以推测,硫酸铝溶液呈____ 性。
(4)硫酸铝具有净水作用,是由于其与水作用产生的Al(OH)3胶体具有____ 性,证明有胶体产生的方法是____ 。
(1)该实验表明,Na2CO3溶液显碱性的原因是
A.Na2CO3提供Na+
B.Na2CO3提供CO

C.Na2CO3提供OH-
D.CO
 与水反应生成OH-
与水反应生成OH-(2)从形成盐的酸和碱的强弱角度看,Na2CO3属于
A.强酸强碱盐 B.强酸弱碱盐 C.弱酸强碱盐 D.弱酸弱碱盐
(3)结合BaCl2溶液呈中性,可以推测,硫酸铝溶液呈
(4)硫酸铝具有净水作用,是由于其与水作用产生的Al(OH)3胶体具有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验小组发现新配制的 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
资料:ⅰ.胶体可以透过滤纸。
ⅱ. 与
与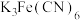 溶液反应,生成蓝色沉淀
溶液反应,生成蓝色沉淀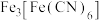 。
。
(1)探究A中的成分,进行如下实验。
取少量A,过滤得到红褐色沉淀和黄色透明液体B。
取少量B于试管中,加入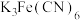 溶液,有蓝色沉淀。
溶液,有蓝色沉淀。
取少量B于试管中,加入___________ (填试剂),液体变为红色。
用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有 、
、 、
、_______ 和_______ 。
进一步探究B显黄色的原因。___________ (用离子方程式表示)。
(3)由上述实验得出:B显黄色的主要原因不是因为含有 ,而是因为含有
,而是因为含有___________ 。理由是:___________ 。
测定A的变质程度并分析对后续实验的影响。
(4)取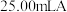 ,加入足量稀硫酸,可与
,加入足量稀硫酸,可与 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为___________  ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。
(5)下列实验可以使用A进行的是___________ (填字母)。
a.向A中滴入 溶液,制备纯净的
溶液,制备纯净的 沉淀
沉淀
b.用A处理含有+6价 的酸性废水,将剧毒的+6价C还原至低毒的+3价
的酸性废水,将剧毒的+6价C还原至低毒的+3价
 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。资料:ⅰ.胶体可以透过滤纸。
ⅱ.
 与
与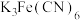 溶液反应,生成蓝色沉淀
溶液反应,生成蓝色沉淀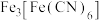 。
。(1)探究A中的成分,进行如下实验。
取少量A,过滤得到红褐色沉淀和黄色透明液体B。
取少量B于试管中,加入
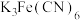 溶液,有蓝色沉淀。
溶液,有蓝色沉淀。取少量B于试管中,加入
用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有
 、
、 、
、进一步探究B显黄色的原因。
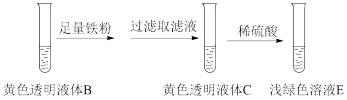
(3)由上述实验得出:B显黄色的主要原因不是因为含有
 ,而是因为含有
,而是因为含有测定A的变质程度并分析对后续实验的影响。
(4)取
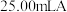 ,加入足量稀硫酸,可与
,加入足量稀硫酸,可与 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为 ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。(5)下列实验可以使用A进行的是
a.向A中滴入
 溶液,制备纯净的
溶液,制备纯净的 沉淀
沉淀b.用A处理含有+6价
 的酸性废水,将剧毒的+6价C还原至低毒的+3价
的酸性废水,将剧毒的+6价C还原至低毒的+3价
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol•L-1的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热.试回答下列问题:
(1)其中操作正确的同学是_________________ 。
(2)证明有Fe(OH)3胶体生成的实验操作是____________ ,利用的胶体性质是___________________ 。
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带______ (填“正”或“负”)电荷。②向其中逐滴加入稀硫酸至过量,产生的现象是_____________________ 。
甲同学:向1 mol•L-1的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热.试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的实验操作是
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
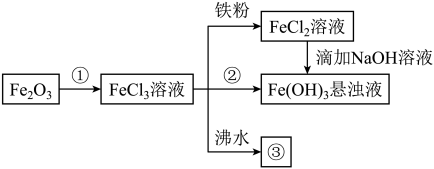
【推荐1】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题: 与①反应的离子方程式
与①反应的离子方程式_______ 。
(2)请写出 与铁粉反应的化学方程式
与铁粉反应的化学方程式_______ 。
(3)向 溶液中滴加NaOH溶液最终生成
溶液中滴加NaOH溶液最终生成 浊液,该过程的现象为
浊液,该过程的现象为_______ ,此过程中发生的氧化还原反应为(用化学方程式表达)_______ 。
(4)将 饱和溶液滴入沸水中,并继续煮沸至红褐色,此过程中发生的化学反应为(用化学方程式表达)
饱和溶液滴入沸水中,并继续煮沸至红褐色,此过程中发生的化学反应为(用化学方程式表达)_______ 。
(5) 溶液能使酸性高锰酸钾溶液褪色,生成二价锰离子,此过程中发生的化学反应为(用离子方程式表达)
溶液能使酸性高锰酸钾溶液褪色,生成二价锰离子,此过程中发生的化学反应为(用离子方程式表达)_______ 。
 与①反应的离子方程式
与①反应的离子方程式(2)请写出
 与铁粉反应的化学方程式
与铁粉反应的化学方程式(3)向
 溶液中滴加NaOH溶液最终生成
溶液中滴加NaOH溶液最终生成 浊液,该过程的现象为
浊液,该过程的现象为(4)将
 饱和溶液滴入沸水中,并继续煮沸至红褐色,此过程中发生的化学反应为(用化学方程式表达)
饱和溶液滴入沸水中,并继续煮沸至红褐色,此过程中发生的化学反应为(用化学方程式表达)(5)
 溶液能使酸性高锰酸钾溶液褪色,生成二价锰离子,此过程中发生的化学反应为(用离子方程式表达)
溶液能使酸性高锰酸钾溶液褪色,生成二价锰离子,此过程中发生的化学反应为(用离子方程式表达)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是__ 。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:___ 。
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是__ 。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质粒子能透过滤纸
(4)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察__  填“有”或“无”
填“有”或“无” 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为__ 。

(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学反应方程式:
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质粒子能透过滤纸
(4)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察
 填“有”或“无”
填“有”或“无” 丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】(1)NaCl中含有少量的Na2SO4,为测定NaCl纯度,某学生取样品a g溶解于水,然后滴入过量的BaCl2溶液使SO42-离子转化为沉淀,然后将所得沉淀过滤、洗涤、转移、干燥、称量质量为b g 。
①确认SO42-已沉淀完全的实验方法是___________________________ ;
②过滤后洗涤沉淀的方法是____________________________________ ;
③判断沉淀已经洗净的方法是___________________________________ ;
④氯化钠纯度(ω)的计算表达式为________________________
(2)Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5 ~ 6滴________ ,继续煮沸至体系呈________ ,停止加热,即制得Fe(OH)3胶体,请写出胶体制备过程的离子方程式_____________ 。
①确认SO42-已沉淀完全的实验方法是
②过滤后洗涤沉淀的方法是
③判断沉淀已经洗净的方法是
④氯化钠纯度(ω)的计算表达式为
(2)Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5 ~ 6滴
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。
已知:Cr3+ Cr(OH)3
Cr(OH)3 CrO
CrO
(1)含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O 与FeSO4溶液在酸性条件下反应的离子方程式
与FeSO4溶液在酸性条件下反应的离子方程式_______
②用离子方程式表示溶液pH不能超过10的原因_______
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和CrO 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
①写出阴极的电极反应式_______ 。
②电解法中加入氯化钠的作用是_______ 。
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:_______ 。
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。则B点时剩余固体的成分是_______ (填化学式)。

已知:Cr3+
 Cr(OH)3
Cr(OH)3 CrO
CrO
(1)含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O
 与FeSO4溶液在酸性条件下反应的离子方程式
与FeSO4溶液在酸性条件下反应的离子方程式②用离子方程式表示溶液pH不能超过10的原因
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和CrO
 发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。①写出阴极的电极反应式
②电解法中加入氯化钠的作用是
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为:
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。则B点时剩余固体的成分是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有失去标签的四瓶溶液A、B、C、D,只知它们分别为 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种,为鉴别它们,进行实验得出以下实验事实:
溶液中的一种,为鉴别它们,进行实验得出以下实验事实:
①A+D→溶液+气体;
②B+C→溶液+沉淀;
③B+D→溶液+沉淀;
④A+B→溶液+沉淀;
⑤将④中得到的沉淀加入③中所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请回答如下问题:
(1) A、B、C、D四种无色溶液分别为A.______ 、B.______ 、C.______ 、D.______ 。
(2)写出下列实验所对应的离子方程式:
①___________ 。
②___________ 。
⑤___________ 。
(3)检验C溶液中阴离子时所用的试剂为___________ ,观察到的现象为___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种,为鉴别它们,进行实验得出以下实验事实:
溶液中的一种,为鉴别它们,进行实验得出以下实验事实:①A+D→溶液+气体;
②B+C→溶液+沉淀;
③B+D→溶液+沉淀;
④A+B→溶液+沉淀;
⑤将④中得到的沉淀加入③中所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请回答如下问题:
(1) A、B、C、D四种无色溶液分别为A.
(2)写出下列实验所对应的离子方程式:
①
②
⑤
(3)检验C溶液中阴离子时所用的试剂为
您最近一年使用:0次
【推荐3】过氧化钙( )微溶于水,可作医用防腐剂、消毒剂,以下是制备
)微溶于水,可作医用防腐剂、消毒剂,以下是制备 的一种方法。
的一种方法。

回答下列问题:
(1)步骤I中反应的离子方程式是________________________________ 。
(2)步骤Ⅱ中反应的化学方程式是(有 生成):
生成):______________________________ 。
(3)反应在冰水浴中进行,是为了防止 分解、
分解、_________________________ 。(答1条即可)
(4) 与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是
与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是____________________________ 。
(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理是: ,某同学称取
,某同学称取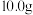 产品于有塞锥形瓶,用适量酸溶解,加入
产品于有塞锥形瓶,用适量酸溶解,加入 高锰酸钾溶液恰好反应。计算:(写计算过程)
高锰酸钾溶液恰好反应。计算:(写计算过程)
①高锰酸钾物质的量______ ;
②标准状况下,生成的氧气体积______ ;
③过氧化钙的百分含量_______ 。
 )微溶于水,可作医用防腐剂、消毒剂,以下是制备
)微溶于水,可作医用防腐剂、消毒剂,以下是制备 的一种方法。
的一种方法。
回答下列问题:
(1)步骤I中反应的离子方程式是
(2)步骤Ⅱ中反应的化学方程式是(有
 生成):
生成):(3)反应在冰水浴中进行,是为了防止
 分解、
分解、(4)
 与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是
与水缓慢反应,常用作鱼塘的供氧剂,其反应的化学方程式是(5)实验室常采用以酸为介质,用高锰酸钾溶液测定过氧化钙的含量。其原理是:
 ,某同学称取
,某同学称取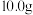 产品于有塞锥形瓶,用适量酸溶解,加入
产品于有塞锥形瓶,用适量酸溶解,加入 高锰酸钾溶液恰好反应。计算:(写计算过程)
高锰酸钾溶液恰好反应。计算:(写计算过程)①高锰酸钾物质的量
②标准状况下,生成的氧气体积
③过氧化钙的百分含量
您最近一年使用:0次



