已知 的浓硫酸与亚硫酸钠反应可以制备
的浓硫酸与亚硫酸钠反应可以制备 。实验室可用如下装置(略去部分夹持仪器)制取
。实验室可用如下装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。
 溶液的仪器名称为
溶液的仪器名称为___________ 。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若___________ ,则整个装置气密性良好。
(2)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择___________(填字母)。
生成的快慢,其中的液体最好选择___________(填字母)。
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验
方案Ⅰ 向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ 向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ 向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案合理的是方案___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式___________ 。
(5)装置E的作用是___________ 。装置F中为___________ 溶液。
 的浓硫酸与亚硫酸钠反应可以制备
的浓硫酸与亚硫酸钠反应可以制备 。实验室可用如下装置(略去部分夹持仪器)制取
。实验室可用如下装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。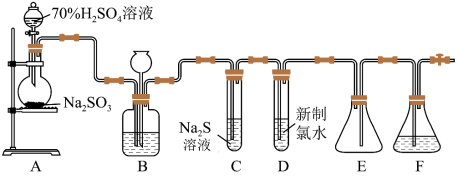

 溶液的仪器名称为
溶液的仪器名称为(2)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择___________(填字母)。
生成的快慢,其中的液体最好选择___________(填字母)。| A.蒸馏水 | B.饱和 溶液 溶液 | C.饱和 溶液 溶液 | D.饱和NaOH溶液 |
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验
方案Ⅰ 向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ 向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ 向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案合理的是方案
(5)装置E的作用是
更新时间:2024/05/01 20:26:42
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某学习小组设计制取SO2并验证其部分性质的实验装置如图(夹持装置省略):

请回答:
(1)简述检查装置A气密性的方法:__________________ 。
(2)写出C中发生的离子反应方程式:_________________ 。
(3)通氮气的作用是________________________ 。

请回答:
(1)简述检查装置A气密性的方法:
(2)写出C中发生的离子反应方程式:
(3)通氮气的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂。
Ⅰ.甲组同学拟利用 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与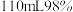 的浓硫酸(含
的浓硫酸(含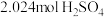 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。
(1)写出 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:__________________ 。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_________ (填化学式)。
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)
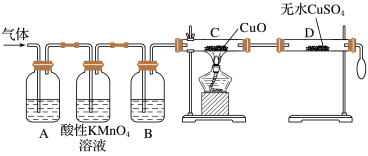
①A中试剂是品红溶液,作用是____________ 。
②B中所装试剂为____________ 。
③证明气体中混有杂质气体的实验现象是:________ 。
Ⅱ. 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。
(4)工业上有多种方法可以减少 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是___________ 。
(5)丙组同学认为 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
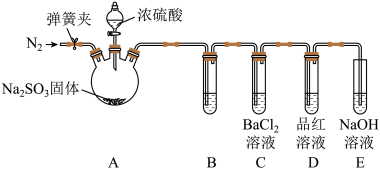
已知: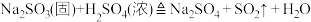
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是___________ 。
Ⅰ.甲组同学拟利用
 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与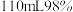 的浓硫酸(含
的浓硫酸(含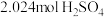 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。(1)写出
 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
Ⅱ.
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。(4)工业上有多种方法可以减少
 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是(5)丙组同学认为
 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知:
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】大气污染物 是一种无色刺激性气味气体。某学习小组利用如图所示装置探究
是一种无色刺激性气味气体。某学习小组利用如图所示装置探究 的相关性质(装置A加热装置略),回答下列问题:
的相关性质(装置A加热装置略),回答下列问题:

(1)实验开始前,先检查装置的___________ 。
(2)仪器a的名称___________ 。
(3)装置A用于制取 气体,其中发生反应的化学方程式为
气体,其中发生反应的化学方程式为___________ 。
(4)一段时间后,装置B中出现的现象是___________ ,可证明 具有
具有___________ (填“氧化性”或“还原性”)。
(5)充分反应后取装置C中溶液,加热出现的现象是___________ 。
(6)装置D中发生反应的化学方程式是___________ 。
 是一种无色刺激性气味气体。某学习小组利用如图所示装置探究
是一种无色刺激性气味气体。某学习小组利用如图所示装置探究 的相关性质(装置A加热装置略),回答下列问题:
的相关性质(装置A加热装置略),回答下列问题:
(1)实验开始前,先检查装置的
(2)仪器a的名称
(3)装置A用于制取
 气体,其中发生反应的化学方程式为
气体,其中发生反应的化学方程式为(4)一段时间后,装置B中出现的现象是
 具有
具有(5)充分反应后取装置C中溶液,加热出现的现象是
(6)装置D中发生反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。
(已知:C+2H2SO4(浓) CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_____ 。
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。_____ ;装置C中品红溶液的作用是_____ 。
(3)装置D中加入的试剂为_____
(4)装置H的作用为_____ 。
兴趣小组设计如图装置验证二氧化硫的化学性质。_____ ;
为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(6)上述方案中合理的是_____ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为_____ 。
(7)如果用硫酸溶液和 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是_____ 。
(已知:C+2H2SO4(浓)
 CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)(1)有同学认为制得的SO2中可能混有杂质,其化学式为
为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
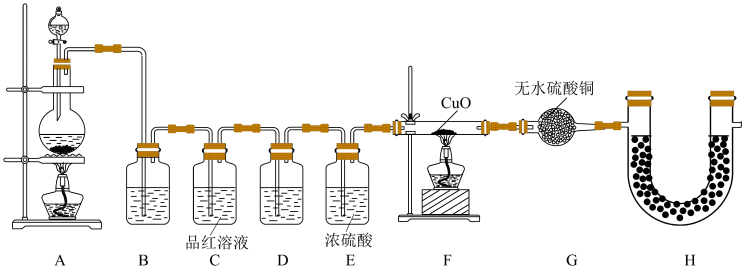
(3)装置D中加入的试剂为
(4)装置H的作用为
兴趣小组设计如图装置验证二氧化硫的化学性质。
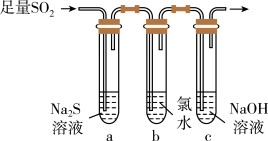
为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
(6)上述方案中合理的是
(7)如果用硫酸溶液和
 固体反应制取
固体反应制取 装置如图所示。其中
装置如图所示。其中 导管的作用是
导管的作用是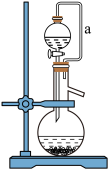
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室里研究不同价态硫元素之间的转化

(1)A中发生反应的化学方程式为___________ 。
(2)B中的现象是___________ 。
(3)C中出现淡黄色沉淀,反应中Na2S做___________ (填“氧化剂”或“还原剂”)。
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为___________ 价。
(5)E的作用是吸收多余的SO2,离子方程式为___________ 。
(6)上述实验D体现SO2的性质是___________ 。

(1)A中发生反应的化学方程式为
(2)B中的现象是
(3)C中出现淡黄色沉淀,反应中Na2S做
(4)D中溴水褪色,该反应S元素的价态变化是由+4价变为
(5)E的作用是吸收多余的SO2,离子方程式为
(6)上述实验D体现SO2的性质是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】化学课外活动小组利用以下装置完成系列实验。请回答以下问题:
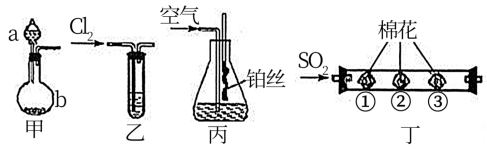
(1)装置甲中仪器a的名称为____________ ;用装置甲制取NH3,在b中加入CaO固体,a中加入浓氨水,写出反应的化学方程式:_________________ 。
(2)将C12持续通入装有淀粉一KI无色溶液的装置乙中,溶液变蓝而后逐渐褪色。查阅资料得知:溶液蓝色逐渐褪色,是因为有+5价的碘元素生成。请写出该反应的离子方程式:____________ 。
(3)用装置丙模拟“氨的催化氧化”实验。锥形瓶内装有浓氨水,通入空气,并将红热的铂丝插入锥形瓶内,铂丝保持红热。铂丝保持红热的原因是__________ ;锥形瓶内还可观察到现象是__________ 。
(4)活动小组从“绿色化学”角度出发。在装置丁中进行SO2的性质实验。其中棉花上蘸有不同试剂。请填写表中空白:

(1)装置甲中仪器a的名称为
(2)将C12持续通入装有淀粉一KI无色溶液的装置乙中,溶液变蓝而后逐渐褪色。查阅资料得知:溶液蓝色逐渐褪色,是因为有+5价的碘元素生成。请写出该反应的离子方程式:
(3)用装置丙模拟“氨的催化氧化”实验。锥形瓶内装有浓氨水,通入空气,并将红热的铂丝插入锥形瓶内,铂丝保持红热。铂丝保持红热的原因是
(4)活动小组从“绿色化学”角度出发。在装置丁中进行SO2的性质实验。其中棉花上蘸有不同试剂。请填写表中空白:
| 棉花位置 | ① | ② | ③ |
| 棉花上蘸有的试剂 | 品红溶液 | 酸性高锰酸钾溶液 | |
| 现象 | 溶液紫色退去 | 无 | |
| 结论 | SO2具有漂白性 | SO2具有 | SO2有毒,不能排空 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某校化学兴趣小组同学取锌粒与浓 充分反应制取
充分反应制取 气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。
气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。
(1)杂质气体可能是____ ,酸性 溶液的作用
溶液的作用____ ;B中添加的试剂是____ 。
(2)装置C中所装药品为____ ,D中所装药品为____ ,可证实气体X中混有较多量某杂质气体的实验现象是____ 。
 充分反应制取
充分反应制取 气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。
气体,待锌粒全部溶解后,同学们准备用收集到的气体(X)做有关实验,但是老师说收集到的气体(X)可能含有杂质。为证实相关分析,该小组的同学设计了如下图所示的实验装置,对此气体(X)取样进行认真研究。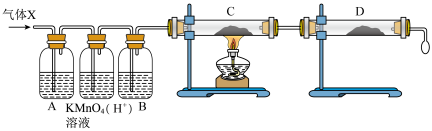
(1)杂质气体可能是
 溶液的作用
溶液的作用(2)装置C中所装药品为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】工业生产过程中产生的二氧化硫会造成环境问题,可用多种方法脱除。
Ⅰ.由次氯酸钠碱性废水(含有杂质Ca2+)处理硫酸工业尾气的流程如下:
①脱硫时需保持溶液呈碱性,此过程的主要反应之一为SO2+2OH-= +H2O;另一个为二氧化硫与次氯酸钠发生的氧化还原反应,请写出该反应的离子方程式:
+H2O;另一个为二氧化硫与次氯酸钠发生的氧化还原反应,请写出该反应的离子方程式:___________ 。
②提高脱硫率的可行措施有___________ (填序号)。
a.加快通入尾气的速率
b.吸收塔中喷淋的碱液与气体逆向接触
c.提高碱液pH
③温度控制在40~60 ℃之间,脱硫率较高,原因是___________ 。
(2)滤渣的主要成分为___________ (填化学式)。
Ⅱ.为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的MgSO4。
(3)写出该反应的化学方程式:___________ 。
Ⅲ. 双碱法脱除烟气中SO2的过程如图所示。___________ (填化学式)。
(5)过程Ⅱ中,1 mol O2可氧化___________ mol Na2SO3。
Ⅰ.由次氯酸钠碱性废水(含有杂质Ca2+)处理硫酸工业尾气的流程如下:
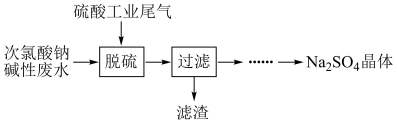
①脱硫时需保持溶液呈碱性,此过程的主要反应之一为SO2+2OH-=
 +H2O;另一个为二氧化硫与次氯酸钠发生的氧化还原反应,请写出该反应的离子方程式:
+H2O;另一个为二氧化硫与次氯酸钠发生的氧化还原反应,请写出该反应的离子方程式:②提高脱硫率的可行措施有
a.加快通入尾气的速率
b.吸收塔中喷淋的碱液与气体逆向接触
c.提高碱液pH
③温度控制在40~60 ℃之间,脱硫率较高,原因是
(2)滤渣的主要成分为
Ⅱ.为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的MgSO4。
(3)写出该反应的化学方程式:
Ⅲ. 双碱法脱除烟气中SO2的过程如图所示。
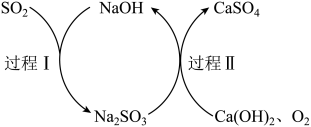
(5)过程Ⅱ中,1 mol O2可氧化
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】学习小组在实验室中利用下图装置制备SO2并进行相关性质的探究。
(1)仪器Q的名称为_________ 。
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
(3)装置C中出现的现象说明SO2具有_________ 性。
(4)装置E中__________________ (填现象)可说明SO2具有还原性,发生反应的离子方程式为__________________ 。
(5)装置F的作用是_________ 。
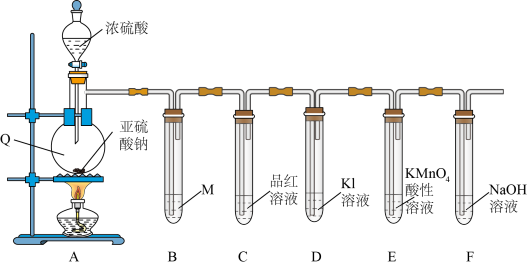
(1)仪器Q的名称为
(2)装置B是为了观察气体的流速,则试剂M为_________(填字母)。
| A.NaOH溶液 | B.饱和NaHSO3溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
(3)装置C中出现的现象说明SO2具有
(4)装置E中
(5)装置F的作用是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】为探究某绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案。
可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液,请参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)如何证明绿矾已经被氧化_______ 。
(2)如何证明绿矾已经被完全氧化_______ 。
(3)在使用硫酸亚铁时,如何防止 的干扰?写出相关离子方程式
的干扰?写出相关离子方程式_______ 。
可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液,请参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
(1)如何证明绿矾已经被氧化
(2)如何证明绿矾已经被完全氧化
(3)在使用硫酸亚铁时,如何防止
 的干扰?写出相关离子方程式
的干扰?写出相关离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某研究性学习小组设计了一组实验验证元素周期律
(1)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相同的锂、钠、钾块,观察现象。
甲同学设计该实验的目的是______ ,反应最剧烈的烧杯是_____ (填字母),结论是________ 。
(2)乙同学想验证同周期元素金属性强弱的规律,最好选用第____ 周期的________ 三种元素,最简单的实验是将大小相同的三小块金属分别投入相同浓度的稀盐酸中,观察现象。应该看到的现象是:①________ ,②________ ,③________ 。
(1)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相同的锂、钠、钾块,观察现象。
甲同学设计该实验的目的是
(2)乙同学想验证同周期元素金属性强弱的规律,最好选用第
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】已知铁氰化钾K3[Fe(CN)6]溶液呈黄色,可以与Fe2+反应生成带有特征蓝色的Fe3[Fe(CN)6]2(铁氰化亚铁)沉淀,因而在实验室中常用于鉴别溶液中是否存在Fe2+。
I.某化学兴趣小组查阅资料了解到[Fe(CN)6]3-具有氧化性,可被还原生成[Fe(CN)6]4-。设计了如下实验,探究[Fe(CN)6]3-的相关性质。
(1)实验一:向饱和Na2S溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,溶液出现黄色浑浊,发生反应的离子方程式为______ 。
(2)实验二:向滴有淀粉的饱和KI溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,可以观察到的现象为______ 。
II.小组同学提出问题:K3[Fe(CN)6]能否将Fe氧化成Fe2+?设计并实施实验:
(3)指导老师指出实验中需要用煮沸后再冷却至室温的蒸馏水配制的K3[Fe(CN)6]溶液,并且往试管中的溶液上加入少量煤油,其目的为___________ 。
(4)①根据实验现象得出结论:___________ 。
②反思现象:乙同学认为实验三和实验四现象不同的原因是铁屑表面有一层金属氧化膜,阻止了反应进行,加入NaCl的作用为______ 。
③深度探究:为证明不同现象是由Cl-而不是Na+造成的,可向实验三的试管中加入少量___________ (填化学式),观察是否出现蓝色沉淀。
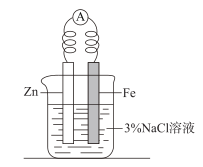
(5)拓展实验:按如图所示装置及试剂组装仪器,观察到电流表指针发生偏转,Fe电极表面的电极方程式为___________ 。请设计实验方案探究该装置是否能有效防止Fe发生腐蚀:___________ 。
I.某化学兴趣小组查阅资料了解到[Fe(CN)6]3-具有氧化性,可被还原生成[Fe(CN)6]4-。设计了如下实验,探究[Fe(CN)6]3-的相关性质。
(1)实验一:向饱和Na2S溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,溶液出现黄色浑浊,发生反应的离子方程式为
(2)实验二:向滴有淀粉的饱和KI溶液中滴加几滴0.1mol·L-1的K3[Fe(CN)6]溶液,可以观察到的现象为
II.小组同学提出问题:K3[Fe(CN)6]能否将Fe氧化成Fe2+?设计并实施实验:
| 序号 | 实验方案 | 实验现象 |
| 实验三 | 取少量0.1mol·L-1的K3[Fe(CN)6]溶液于试管中,加入适量铁屑 | 无明显现象 |
| 实验四 | 向实验三的试管中加入少量NaCl固体 | 溶液中出现蓝色浑浊 |
(4)①根据实验现象得出结论:
②反思现象:乙同学认为实验三和实验四现象不同的原因是铁屑表面有一层金属氧化膜,阻止了反应进行,加入NaCl的作用为
③深度探究:为证明不同现象是由Cl-而不是Na+造成的,可向实验三的试管中加入少量
(5)拓展实验:按如图所示装置及试剂组装仪器,观察到电流表指针发生偏转,Fe电极表面的电极方程式为

您最近一年使用:0次



