有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦NaOH溶液;⑧蔗糖晶体;⑨FeCl3固体;⑩CH3COOH。请用序号填空。
(1)上述状态下的物质可导电的是_______ (请用序号填空)。
(2)属于电解质的是_______ ,属于非电解质的是 _______ (请用序号填空)。
(3)写出⑦的溶液和⑩的溶液反应的离子方程式_______ 。
(4)将⑨的饱和溶液滴入沸水中,继续煮沸直至溶液呈_______ 色,即可制得Fe(OH)3胶体,反应方程式为_______ 。
(1)上述状态下的物质可导电的是
(2)属于电解质的是
(3)写出⑦的溶液和⑩的溶液反应的离子方程式
(4)将⑨的饱和溶液滴入沸水中,继续煮沸直至溶液呈
更新时间:2024/08/28 15:35:04
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水
请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。写出制备Fe(OH)3胶体的离子方程式为:_______ 。
(3)写出④在水溶液中的电离方程式_______ 。
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式_______ 。
请回答下列问题:
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。写出制备Fe(OH)3胶体的离子方程式为:
(3)写出④在水溶液中的电离方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】央视《每周质量报告》曝光了少数明胶企业将皮革废料熬制成工业明胶,出售给个别制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。2010版《中国药典》明确规定,药用胶囊使用的明胶原料,重金属铬的含量均不得超过2mg•kg-1。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为___ ;如果某明胶原料100kg中含有铁元素的质量为0.56g,则药用胶囊使用的这种明胶原料重金属铬的含量___ (填“超标”或“不超标”)。
(2)区别明胶溶于水的分散系和Na2SO4溶液的方法是___ 。
(3)将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是___ 。
A.冷水 B.沸水 C.NaCl溶液 D.NaOH溶液
(4)已知胶体的分散质不能透过半透膜,但小分子或离子能透过半透膜。现将10mL明胶溶于水的分散系与5mLNa2SO4溶液混合后装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中。写出证明Na+能透过半透膜的实验方法(具体操作):___ 。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为
(2)区别明胶溶于水的分散系和Na2SO4溶液的方法是
(3)将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是
A.冷水 B.沸水 C.NaCl溶液 D.NaOH溶液
(4)已知胶体的分散质不能透过半透膜,但小分子或离子能透过半透膜。现将10mL明胶溶于水的分散系与5mLNa2SO4溶液混合后装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中。写出证明Na+能透过半透膜的实验方法(具体操作):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热煮沸饱和FeCl3溶液;
丙同学向25mL沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是__ ;若丙同学实验中不停止加热,会看到__ 。
(2)证明有Fe(OH)3胶体生成的实验操作及现象是__ 。
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明__ 。
②向其中加入稀硫酸,产生的现象是___ 。
甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热煮沸饱和FeCl3溶液;
丙同学向25mL沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的实验操作及现象是
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明
②向其中加入稀硫酸,产生的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下列物质:①NaCl固体②盐酸③Ba(OH)2溶液④铜⑤二氧化碳气体⑥硫酸氢钾固体⑦乙醇(C2H5OH)⑧液态硫酸⑨熔融态BaSO4⑩液态SO3。请回答下列问题(用序号):
(1)属于电解质的是________ ;属于非电解质的是________ 。
(2)上述状态下可导电的物质是________ ;上述物质溶于水后形成的溶液能导电的是________ 。
(3)NaHSO4是一种酸式盐,可用作清洁剂、防腐剂等。
①NaHSO4溶于水时的电离方程式________ 。
②少量NaHSO4与Ba(OH)2溶液混合,该反应的离子方程式为________ 。
③写出盐酸与氢氧化钾溶液反应的离子方程式:________ 。
(1)属于电解质的是
(2)上述状态下可导电的物质是
(3)NaHSO4是一种酸式盐,可用作清洁剂、防腐剂等。
①NaHSO4溶于水时的电离方程式
②少量NaHSO4与Ba(OH)2溶液混合,该反应的离子方程式为
③写出盐酸与氢氧化钾溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】阅读下列短文并填空:
纯碱是基本化工原料。工业上获得纯碱的方法主要为:将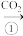 通入
通入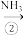 和
和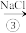 饱和溶液中,使溶解度小的
饱和溶液中,使溶解度小的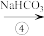 从溶液中析出,加热
从溶液中析出,加热 晶体即可获得
晶体即可获得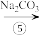 。我国化学家侯德榜于1943年提出了著名的侯氏制碱法,此法将
。我国化学家侯德榜于1943年提出了著名的侯氏制碱法,此法将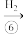 与
与 合成氨法、氨碱法工艺联合,同时得到了纯碱和
合成氨法、氨碱法工艺联合,同时得到了纯碱和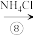 两种产品,大大缩短了生产流程,降低了成本,实现了中国人自己制碱的梦想。
两种产品,大大缩短了生产流程,降低了成本,实现了中国人自己制碱的梦想。
(1)在上述短文标有序号的物质中,属于盐的是___________ (选填序号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。
(2)上述物质中,能与NaOH溶液反应的是(选填序号):___________ ,书写它们在水溶液中的电离方程式(若为非电解质则不写):___________ 。
(3)根据材料二书写侯氏制碱法过程中得到 的化学方程式:
的化学方程式:___________ 。
纯碱是基本化工原料。工业上获得纯碱的方法主要为:将
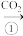 通入
通入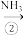 和
和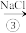 饱和溶液中,使溶解度小的
饱和溶液中,使溶解度小的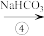 从溶液中析出,加热
从溶液中析出,加热 晶体即可获得
晶体即可获得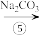 。我国化学家侯德榜于1943年提出了著名的侯氏制碱法,此法将
。我国化学家侯德榜于1943年提出了著名的侯氏制碱法,此法将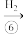 与
与 合成氨法、氨碱法工艺联合,同时得到了纯碱和
合成氨法、氨碱法工艺联合,同时得到了纯碱和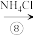 两种产品,大大缩短了生产流程,降低了成本,实现了中国人自己制碱的梦想。
两种产品,大大缩短了生产流程,降低了成本,实现了中国人自己制碱的梦想。(1)在上述短文标有序号的物质中,属于盐的是
(2)上述物质中,能与NaOH溶液反应的是(选填序号):
(3)根据材料二书写侯氏制碱法过程中得到
 的化学方程式:
的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质:①Ba(OH)2溶液 ②液氯 ③BaCO3固体 ④NaHSO4 ⑤Fe(OH)3胶体 ⑥铜 ⑦干冰(固态的二氧化碳) ⑧冰醋酸(纯净的醋酸) ⑨CuSO4·5H2O
(1)以上物质中属于电解质的是___________ (均填序号)
(2)写出①和⑧的水溶液反应的离子方程式___________
(3)向①中滴加④的水溶液之后,溶液导电能力随滴入NaHSO4溶液体积变化曲线如图所示。
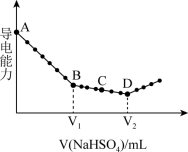
①AB段反应的离子方程式:___________
②C点溶液呈___________ 性(填“酸”、“碱”或“中”)。
③V1、V2的关系为V1:V2=___________
(4)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请结合化学方程式表述原因___________
(5)稀Na2S溶液有一种腐卵气味,加入AlCl3溶液后,腐卵气味加剧,用离子方程式表示气味加剧过程所发生的化学反应___________
(6)已知硼酸与足量氢氧化钠溶液反应的离子方程式为H3BO3+OH-= ,则硼酸的电离方程式为
,则硼酸的电离方程式为___________ 。
(1)以上物质中属于电解质的是
(2)写出①和⑧的水溶液反应的离子方程式
(3)向①中滴加④的水溶液之后,溶液导电能力随滴入NaHSO4溶液体积变化曲线如图所示。

①AB段反应的离子方程式:
②C点溶液呈
③V1、V2的关系为V1:V2=
(4)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请结合化学方程式表述原因
(5)稀Na2S溶液有一种腐卵气味,加入AlCl3溶液后,腐卵气味加剧,用离子方程式表示气味加剧过程所发生的化学反应
(6)已知硼酸与足量氢氧化钠溶液反应的离子方程式为H3BO3+OH-=
 ,则硼酸的电离方程式为
,则硼酸的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A 可以是_______ (填序号)。

①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥ 氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)写出一水合氨的电离方程式_______ 。
(3)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是_______ (填字母),并写出发生反应的离子方程式_______ 。
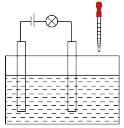
A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(4)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且 Ca(HCO3)2易溶于水。若在(3)题图中,电解质溶液为 Ca(OH)2溶液,向溶液中逐渐通入 CO2。则:下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2 气体量的关系(x 轴表示 CO2通入的量,y 轴表示导电能力)。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A 可以是

①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥ 氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)写出一水合氨的电离方程式
(3)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是

A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(4)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且 Ca(HCO3)2易溶于水。若在(3)题图中,电解质溶液为 Ca(OH)2溶液,向溶液中逐渐通入 CO2。则:下列四个图中,_______(填字母)能比较准确地反映出溶液的导电能力和通入CO2 气体量的关系(x 轴表示 CO2通入的量,y 轴表示导电能力)。
A. | B.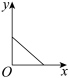 | C.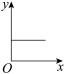 | D.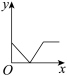 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)下列物质中: A.NaCl晶体;B.乙醇;C.稀 ;D.单质铜;E.蔗糖;F.
;D.单质铜;E.蔗糖;F. ;G.干冰;H.液态氯化氢;I.熔融硝酸钠;J.盐酸。
;G.干冰;H.液态氯化氢;I.熔融硝酸钠;J.盐酸。
①能够直接导电的是______ (填字母,下同);②属于非电解质的是______ ;
③能直接导电,且是电解质的是______ ;④虽不能直接导电,但是电解质的是______ 。
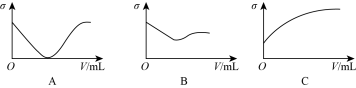
(2)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率(σ)随新物质加入量(V)的变化曲线如图所示。分别与A、B、C曲线变化趋势一致的是______ (填序号)。②中的离子反应方程式依次为______ 、______ 。
①向氨水中通入HC1气体直至过量
②向饱和石灰水中不断通入
③向硝酸中逐滴加入等浓度的氢氧化钾溶液至过量
(3)某无色透明溶液存在大量 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种(水电离的离子浓度忽略不计),请填写下列空白:
中的一种或几种(水电离的离子浓度忽略不计),请填写下列空白:
①取少量原溶液,加入过量稀盐酸有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。
②取①的滤液加过量的NaOH溶液,出现白色沉淀。
通过过以上叙述可知原溶液中肯定的离子有______ ;肯定不存在的离子是______ ,可能存在的离子是______ 。
(1)下列物质中: A.NaCl晶体;B.乙醇;C.稀
 ;D.单质铜;E.蔗糖;F.
;D.单质铜;E.蔗糖;F. ;G.干冰;H.液态氯化氢;I.熔融硝酸钠;J.盐酸。
;G.干冰;H.液态氯化氢;I.熔融硝酸钠;J.盐酸。①能够直接导电的是
③能直接导电,且是电解质的是
(2)在一定温度下,向不同电解质溶液中加入新物质时溶液电导率(σ)随新物质加入量(V)的变化曲线如图所示。分别与A、B、C曲线变化趋势一致的是

①向氨水中通入HC1气体直至过量
②向饱和石灰水中不断通入

③向硝酸中逐滴加入等浓度的氢氧化钾溶液至过量
(3)某无色透明溶液存在大量
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种(水电离的离子浓度忽略不计),请填写下列空白:
中的一种或几种(水电离的离子浓度忽略不计),请填写下列空白:①取少量原溶液,加入过量稀盐酸有白色沉淀生成,再加入过量稀硝酸,沉淀不消失。
②取①的滤液加过量的NaOH溶液,出现白色沉淀。
通过过以上叙述可知原溶液中肯定的离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列10种物质:①铝,②纯醋酸,③ ,④
,④ ,⑤NaOH,⑥硫酸铜溶液,⑦熔融的
,⑤NaOH,⑥硫酸铜溶液,⑦熔融的 ,⑧
,⑧ ,⑨硝酸钾晶体,⑩乙醇。
,⑨硝酸钾晶体,⑩乙醇。
(1)上述物质中属于非电解质的有___________ (填序号);①②⑥⑦⑨⑩这六种物质中能导电的有___________ (填序号)。
(2)向②的水溶液中加入⑤的离子方程式是___________ 。
(3)⑧在水中的电离方程式为___________ 。
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式___________ 。
(5)用双线桥分析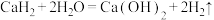 ,并在线桥上标明得失电子情况:
,并在线桥上标明得失电子情况: ___________ 。
 ,④
,④ ,⑤NaOH,⑥硫酸铜溶液,⑦熔融的
,⑤NaOH,⑥硫酸铜溶液,⑦熔融的 ,⑧
,⑧ ,⑨硝酸钾晶体,⑩乙醇。
,⑨硝酸钾晶体,⑩乙醇。(1)上述物质中属于非电解质的有
(2)向②的水溶液中加入⑤的离子方程式是
(3)⑧在水中的电离方程式为
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应
 表示,请写出该离子反应对应的其中一个化学方程式
表示,请写出该离子反应对应的其中一个化学方程式(5)用双线桥分析
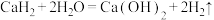 ,并在线桥上标明得失电子情况:
,并在线桥上标明得失电子情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某小组同学探究Na2CO3的性质,请你与他们一起完成,并回答下列问题。
(1)观察:描述Na2CO3的颜色、状态:____ 。
(2)预测:从物质的类别来看,Na2CO3属于____ 类,可以与____ 等类别的物质发生反应。
(3)设计实验并得出结论:
(4)问题和讨论:①对实验II的离子方程式原理,你能再找出一个与它解释相同的化学反应吗____ ?
②在实验室中,如何鉴别Na2CO3和NaHCO3____ ?
③该组同学在探究Na2CO3的性质时的思路是什么____ ?用了什么方法____ ?
(1)观察:描述Na2CO3的颜色、状态:
(2)预测:从物质的类别来看,Na2CO3属于
(3)设计实验并得出结论:
| 实验步骤 | 实验现象 | 结论或解释(用离子方程式) |
| I.向盛有Na2CO3溶液的试管中滴加澄清石灰水 | ||
| II.向盛有Na2CO3溶液的试管中滴加CaCl2溶液 | ||
| III.向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ①CO +H+=HCO +H+=HCO ② |
②在实验室中,如何鉴别Na2CO3和NaHCO3
③该组同学在探究Na2CO3的性质时的思路是什么
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.现有以下物质:① 溶液;②干冰;③熔融
溶液;②干冰;③熔融 ;④NaOH溶液;⑤
;④NaOH溶液;⑤ ;⑥
;⑥ 胶体;⑦氨水;⑧
胶体;⑦氨水;⑧ 固体;⑨
固体;⑨ 溶液
溶液
(1)其中在该状态下能导电且该物质为电解质的是___________ (填编号,下同),属于非电解质的是___________ 。
(2)请写出⑦和⑨反应的离子反应方程式___________ 。
(3)⑤为酸性氧化物,写出④与⑤反应的离子方程式___________ 。
Ⅱ.现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
①甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和 溶液;
溶液;
③丙同学向25 mL沸水中逐滴加入几滴 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(4)其中操作正确的同学是___________ (填甲、乙、丙)。写出此过程中的化学方程式:___________ 。
(5)证明有 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是___________ 。
(6)丁同学利用所制得的 胶体进行下列实验:
胶体进行下列实验:
① 胶粒因吸附离子而带正电荷。将其装入U形管内,用石墨作为电极,接透直流电,通电一段时间后发现
胶粒因吸附离子而带正电荷。将其装入U形管内,用石墨作为电极,接透直流电,通电一段时间后发现___________ (填阳极或阴极)附近的颜色逐渐变深。
②向所得 胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:
胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:___________ 。
③欲除去 胶体中混有的
胶体中混有的 ,所需要进行的操作名称是
,所需要进行的操作名称是___________ 。
 溶液;②干冰;③熔融
溶液;②干冰;③熔融 ;④NaOH溶液;⑤
;④NaOH溶液;⑤ ;⑥
;⑥ 胶体;⑦氨水;⑧
胶体;⑦氨水;⑧ 固体;⑨
固体;⑨ 溶液
溶液(1)其中在该状态下能导电且该物质为电解质的是
(2)请写出⑦和⑨反应的离子反应方程式
(3)⑤为酸性氧化物,写出④与⑤反应的离子方程式
Ⅱ.现有甲、乙、丙三名同学分别进行
 胶体的制备实验。
胶体的制备实验。①甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和
 溶液;
溶液;③丙同学向25 mL沸水中逐滴加入几滴
 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。试回答下列问题:
(4)其中操作正确的同学是
(5)证明有
 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是(6)丁同学利用所制得的
 胶体进行下列实验:
胶体进行下列实验:①
 胶粒因吸附离子而带正电荷。将其装入U形管内,用石墨作为电极,接透直流电,通电一段时间后发现
胶粒因吸附离子而带正电荷。将其装入U形管内,用石墨作为电极,接透直流电,通电一段时间后发现②向所得
 胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:
胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:③欲除去
 胶体中混有的
胶体中混有的 ,所需要进行的操作名称是
,所需要进行的操作名称是
您最近一年使用:0次



