下列关于电解质溶液中离子关系的说法中正确的是
A.0.1mol·L-1Na2CO3溶液中离子浓度关系:c(Na+)=2c( )+c( )+c( )+c(H2CO3) )+c(H2CO3) |
B.0.1mol·L-1NH4Cl和0.1mol·L-1NH3·H2O等体积混合后离子浓度关系c(Cl-)>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| C.常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合液溶中:c(Na+)=c(CH3COO-) |
D.常温下,在pH=1的溶液中,Fe2+、 、ClO-、Na+能大量共存 、ClO-、Na+能大量共存 |
2016高三上·北京东城·专题练习 查看更多[2]
更新时间:2016/12/09 09:54:09
|
相似题推荐
单选题-单题
|
较易
(0.85)
解题方法
【推荐1】某化学实验小组以草木灰为原料制取 晶体,制取流程如下图所示。
晶体,制取流程如下图所示。 、
、 、
、 和不溶于水的杂质。
和不溶于水的杂质。
② 的溶解度随温度的升高而增大,且增幅较大。
的溶解度随温度的升高而增大,且增幅较大。
下列说法错误的是
 晶体,制取流程如下图所示。
晶体,制取流程如下图所示。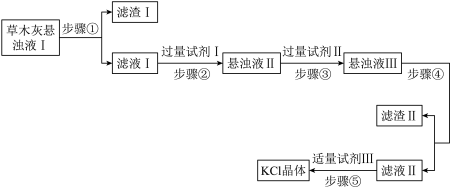
 、
、 、
、 和不溶于水的杂质。
和不溶于水的杂质。②
 的溶解度随温度的升高而增大,且增幅较大。
的溶解度随温度的升高而增大,且增幅较大。下列说法错误的是
| A.步骤①和步骤④的操作均为过滤 |
B.过量试剂I是 溶液,其作用是除去 溶液,其作用是除去 、 、 |
C.过量试剂Ⅱ是 溶液,其作用是除去过量 溶液,其作用是除去过量 |
| D.步骤⑤的操作是蒸发浓缩、冷却结晶 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】某溶液可能含有 Ca2+、Na+、Cu2+、K+、 、
、 、Cl-、
、Cl-、 中的一种或几种,现对其进行如下实验:
中的一种或几种,现对其进行如下实验:
①取少量溶液于试管中,观察为无色透明溶液;
②在①溶液中,滴加足量氯化钡溶液,产生白色沉淀。过滤后,在白色沉淀中加过量稀盐酸,沉淀部分溶解,且有气泡产生。
③在②的滤液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成。
④取原溶液进行焰色实验,火焰为黄色。
下列对原溶液中的所含离子的说法正确的是
 、
、 、Cl-、
、Cl-、 中的一种或几种,现对其进行如下实验:
中的一种或几种,现对其进行如下实验:①取少量溶液于试管中,观察为无色透明溶液;
②在①溶液中,滴加足量氯化钡溶液,产生白色沉淀。过滤后,在白色沉淀中加过量稀盐酸,沉淀部分溶解,且有气泡产生。
③在②的滤液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成。
④取原溶液进行焰色实验,火焰为黄色。
下列对原溶液中的所含离子的说法正确的是
A.一定有 Na+、 和 和  ,可能有 K+、Cl-、Ca2+ ,可能有 K+、Cl-、Ca2+ |
B.一定有 K+、 和 和  , , 、Cl-两种离子中至少有一种 、Cl-两种离子中至少有一种 |
C.一定有 K+、 和 和  ,不含 Cu2+和 Cl-,可能有 Na+和 Ca2+ ,不含 Cu2+和 Cl-,可能有 Na+和 Ca2+ |
D.一定有 Na+、 和 和  ,不含 Cu2+和 Ca2+,可能有 K+、Cl-和 ,不含 Cu2+和 Ca2+,可能有 K+、Cl-和  |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下, 溶液
溶液 。关于该溶液下列说法正确的是
。关于该溶液下列说法正确的是
 溶液
溶液 。关于该溶液下列说法正确的是
。关于该溶液下列说法正确的是A.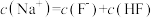 |
B.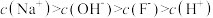 |
C.加水稀释,溶液 增大 增大 |
D. 溶液可用玻璃试剂瓶盛装 溶液可用玻璃试剂瓶盛装 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】常温下,用 的
的 溶液滴定
溶液滴定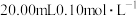 的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
的HX溶液,所得滴定曲线如图所示,下列说法不正确的是

 的
的 溶液滴定
溶液滴定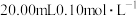 的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
| A.HX为强酸 |
B.对应溶液中水的电离程度: |
C.c点所示的溶液中: |
D.相同条件下, 的水解能力弱于 的水解能力弱于 的电离能力 的电离能力 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】已知下表为 时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是
时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是
 时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是
时某些弱酸的电离平衡常数。依据所给信息判断,下列说法正确的是 | HClO |  |
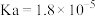 |  | 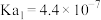 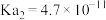 |
A.向NaClO溶液中通入少量二氧化碳的离子方程式为: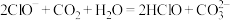 |
B.相同浓度的 和NaClO的混合溶液中, 和NaClO的混合溶液中,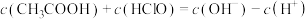 |
C.向 溶液中加入少量水,溶液中pH增大 溶液中加入少量水,溶液中pH增大 |
D.25℃时, 溶液通入 溶液通入 至溶液的 至溶液的 时,溶液中: 时,溶液中: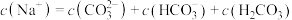 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】现有物质的量浓度均为0.1 mol/L的溶液①NH3·H2O ②CH3COOH ③KHSO4。下列有关离子浓度分析一定不正确的是
A.向①中逐滴加入少量②, 逐渐增大 逐渐增大 |
B.①、③等体积混合后溶液中存在:NH4+ +H2O NH3·H2O+H+ NH3·H2O+H+ |
| C.①、②任意比混合:c(CH3COO-)+c(OH-)=c(H+)+c(NH4+ ) |
| D.①、③按体积比2:1混合:c(NH4+)>c(NH3•H2O)>c(SO42-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】25 ℃时,向20mL 0.1mol/LNH4HSO4溶液中滴入0.1mol/L的NaOH溶液至恰好反应完全,下列说法正确的是( )
| A.整个反应过程中:c(H+) + c(NH4+)+ c(Na+) = c(SO42-) + c(OH-) |
| B.当溶液呈中性时:c(NH4+) > c(SO42-) > c(Na+) > c(H+) = c(OH-) |
| C.当滴入20mL NaOH溶液时:2c(SO42-) = c(NH3∙H2O) + c(NH4+) |
| D.当滴入30mL NaOH溶液时(pH>7):c(NH4+) > c(NH3∙H2O) > c(OH-) > c(H+) |
您最近一年使用:0次

 、
、 、
、 ,
, ,稀盐酸
,稀盐酸 ,
, ,稀盐酸
,稀盐酸

