某研究性学习小组利用如图所示装置完成有关实验。
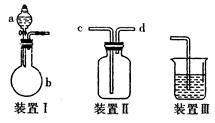
【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入 。装置Ⅱ从 管口进气可作为氨气的收集装置。
【实验二】收集NO
(2)利用装置Ⅱ可收集NO,试简述操作方法: 。
【实验三】比较硫、碳、硅三种元素的非金属性强弱
(3)设计实验,完成下列表格(可以不填满,也可以再加行)

【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入 。装置Ⅱ从 管口进气可作为氨气的收集装置。
【实验二】收集NO
(2)利用装置Ⅱ可收集NO,试简述操作方法: 。
【实验三】比较硫、碳、硅三种元素的非金属性强弱
(3)设计实验,完成下列表格(可以不填满,也可以再加行)
| 装置序号 | 仪器中所加物质名称 | 现象 |
10-11高三·湖北武汉·开学考试 查看更多[1]
(已下线)2012届武汉市部分学校高三新起点调研测试化学试卷
更新时间:2016/12/09 02:02:17
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】 .
. 四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体
四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体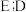 的L层电子数等于
的L层电子数等于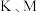 两个电子层上的电子数之和。
两个电子层上的电子数之和。
(1)B为___________ (填元素符号),简单离子半径大小B___________ (填“>”“<”或“=”)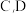 的最高价氧化物对应的水化物是
的最高价氧化物对应的水化物是___________ (填化学式)。
(2)写出 的化合物与E反应的化学方程式:
的化合物与E反应的化学方程式:___________ 。
(3) 两元素形成的化合物属于
两元素形成的化合物属于___________ (填“离子”或“共价”)化合物,D的氢化物的电子式为___________ 。
 .随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。
.随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。
(4)a为以上两种元素组成的分子,a分子中有四个原子和10个电子,则a的分子式为___________ ,结构式为___________ 。
(5)比较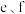 两种元素对应离子的半径大小
两种元素对应离子的半径大小___________ (用元素离子符号表示);非金属性g___________ (填“强于”或“弱于”)h,用一个化学方程式证明你的判断___________ 。
 .
. 四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体
四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体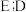 的L层电子数等于
的L层电子数等于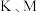 两个电子层上的电子数之和。
两个电子层上的电子数之和。(1)B为
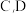 的最高价氧化物对应的水化物是
的最高价氧化物对应的水化物是(2)写出
 的化合物与E反应的化学方程式:
的化合物与E反应的化学方程式:(3)
 两元素形成的化合物属于
两元素形成的化合物属于 .随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。
.随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。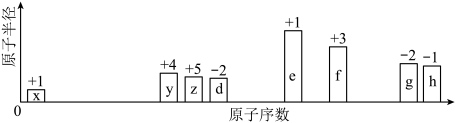
(4)a为以上两种元素组成的分子,a分子中有四个原子和10个电子,则a的分子式为
(5)比较
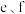 两种元素对应离子的半径大小
两种元素对应离子的半径大小
您最近一年使用:0次
【推荐2】元素周期表中前四周期几种主族元素的位置关系如图所示(过渡元素已忽略)。
请回答下列问题。
(1)①和②能形成简单化合物,该物质的化学式为_______ ,已知该物质为离子化合物,两种离子半径①_______ ②(填“>”“<”或“=”)。
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为_______ (用元素符号表示,下同),电负性由大到小的顺序为_______ 。
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为_______ (用化学式表示)。
(4)元素⑦的基态原子的电子排布式为_______ ,其电子占据的最高能级的轨道形状为_______ 。
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||
| ⑩ | ⑾ |
(1)①和②能形成简单化合物,该物质的化学式为
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为
(4)元素⑦的基态原子的电子排布式为
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下图为周期表的主族元素的一部分,L原子最外层电子数是次外层电子数的一半。
(1)写出M的元素符号:___________ 。
(2)写出R在元素周期表中的位置:___________ 。
(3)最高价氧化物对应水化物的碱性:R___________ (填“>”“<”或“=”,下同)W。
(4)气态氢化物的稳定性:Z___________ X。
(5)R、W、Z的简单离子的半径由大到小的排列顺序是___________ (用元素的离子符号表示)。
(6)下列说法不正确的是___________(填标号)。
| X | Z | ||||
| R | W | L | J | Q | |
| M |
(2)写出R在元素周期表中的位置:
(3)最高价氧化物对应水化物的碱性:R
(4)气态氢化物的稳定性:Z
(5)R、W、Z的简单离子的半径由大到小的排列顺序是
(6)下列说法不正确的是___________(填标号)。
| A.Q、M的最高价氧化物对应的水化物酸性:M<Q |
B.L元素的单质具有半导体的特性,与Z可形成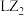 |
| C.W、Z形成的化合物既能与酸反应又能与碱反应 |
| D.M的单质的氧化性大于Q |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
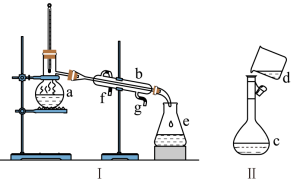
(1)写出下列仪器的名称:a、_____ b、 _____
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是____ ,将仪器补充完整后进行实验,温度计水银球的位置在____ 处。冷凝水由____ (填f或g)口通入,___ 口流出。

(1)写出下列仪器的名称:a、
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】(1)写出以下两种仪器的名称:
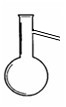 A:
A:____________________  B:
B:__________________
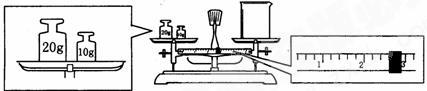
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为_________ g.
(3)指出下面实验中存在的错误:_________________________________________ 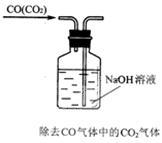
 A:
A: B:
B:(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧杯的实际质量为

(3)指出下面实验中存在的错误:

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
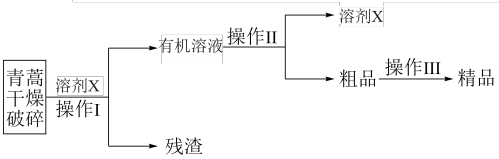
【推荐3】青蒿素是一种高效的抗疟药,常温下为无色针状晶体,难溶于水,易溶于有机溶剂,其提取的主要工艺如图:
已知:
①青蒿素熔点为156~157℃。提取过程中温度超过60℃时,所得青蒿素的药效明显降低。
②常见有机溶剂的沸点:
(1)青蒿破碎的目的是_______ 。
(2)溶剂X应选择表中的_______ (填名称)。
(3)“操作Ⅰ”需要用到的玻璃仪器有_______ 。
(4)“操作Ⅱ”的名称是_______ ,所需的玻璃仪器除酒精灯、冷凝管、牛角管、锥形瓶外,还有_______ 。
(5)“操作Ⅲ”主要过程是加95%乙醇溶解、蒸发浓缩、_______ 、过滤。
(6)某学生对青蒿素的性质进行探究。将青蒿素加入滴有酚酞的NaOH溶液中,搅拌,发现溶液红色变浅。可以得到的实验结论是_______ 。

已知:
①青蒿素熔点为156~157℃。提取过程中温度超过60℃时,所得青蒿素的药效明显降低。
②常见有机溶剂的沸点:
| 物质 | 丙醇 | 四氯化碳 | 乙醚 | 煤油 |
| 沸点/℃ | 97.4 | 76.8 | 34.5 | 180~310 |
(2)溶剂X应选择表中的
(3)“操作Ⅰ”需要用到的玻璃仪器有
(4)“操作Ⅱ”的名称是
(5)“操作Ⅲ”主要过程是加95%乙醇溶解、蒸发浓缩、
(6)某学生对青蒿素的性质进行探究。将青蒿素加入滴有酚酞的NaOH溶液中,搅拌,发现溶液红色变浅。可以得到的实验结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
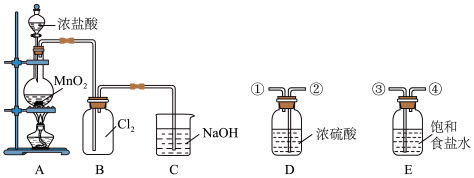
【推荐1】某化学兴趣小组在实验室用如下装置制备氯气:
(1)装置A中发生反应的化学方程式为_______ 。
(2)若要制备纯净、干燥的氯气,需在A、B之间添加净化装置D、E,其中导管连接的顺序是_______ (填写数字编号)。
(3)D装置的作用是_______ ;E装置的作用是_______ 。
(4)C装置中发生反应的离子方程式为_______ 。
(1)装置A中发生反应的化学方程式为
(2)若要制备纯净、干燥的氯气,需在A、B之间添加净化装置D、E,其中导管连接的顺序是
(3)D装置的作用是
(4)C装置中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】已知生石灰与水反应生成 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
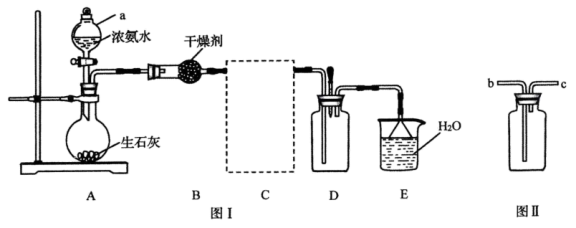
回答下列问题:
(1)仪器 的名称为
的名称为____________ ;装置 中的干燥剂为
中的干燥剂为___________ 。
(2)装置 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接__________ (填“ ”或“
”或“ ”)。
”)。
(3)装置 中倒置漏斗的作用为
中倒置漏斗的作用为___________ 。
(4)实验进行一段时间后,挤压装置 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为___________ ;向装置 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为____________ 。
 并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
并放出热量,实验室利用此原理向生石灰中滴加浓氨水制取氨气并探究其性质(部分夹持装置已略去)。
回答下列问题:
(1)仪器
 的名称为
的名称为 中的干燥剂为
中的干燥剂为(2)装置
 如图Ⅱ所示,用于收集氨气,装置
如图Ⅱ所示,用于收集氨气,装置 应连接
应连接 ”或“
”或“ ”)。
”)。(3)装置
 中倒置漏斗的作用为
中倒置漏斗的作用为(4)实验进行一段时间后,挤压装置
 中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为
中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象为 中滴入1~2滴酚酞溶液,装置
中滴入1~2滴酚酞溶液,装置 中溶液颜色为
中溶液颜色为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
实验步骤如下:
①连接好实验装置,检查装置的气密性;
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为16.0g;
③加热,开始反应,直到不再有气体产生为止;
④测量排入量筒中水的体积为284.3mL,换算成标准状况下氧气的体积为279.0mL;
⑤准确称量试管和残留物的质量为15.6g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?______ .
(2)以下是测量收集到气体体积必须包括的几个步骤: ①调整量筒的高度使广口瓶和量筒内的液面高度相同;②使试管和广口瓶内气体都冷却至室温;③读取量筒内液体的体积,这三步操作的正确顺序是___________________________ (请填写步骤代号),进行③的实验操作时,若仰视读数,则读取氧气的体积_______________ (填“偏大”、“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是___________________ mol;实验测得氧气的气体摩尔体积是____________ L/mol(列出算式即可)。

实验步骤如下:
①连接好实验装置,检查装置的气密性;
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为16.0g;
③加热,开始反应,直到不再有气体产生为止;
④测量排入量筒中水的体积为284.3mL,换算成标准状况下氧气的体积为279.0mL;
⑤准确称量试管和残留物的质量为15.6g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?
(2)以下是测量收集到气体体积必须包括的几个步骤: ①调整量筒的高度使广口瓶和量筒内的液面高度相同;②使试管和广口瓶内气体都冷却至室温;③读取量筒内液体的体积,这三步操作的正确顺序是
(3)实验过程中产生氧气的物质的量是
您最近一年使用:0次



