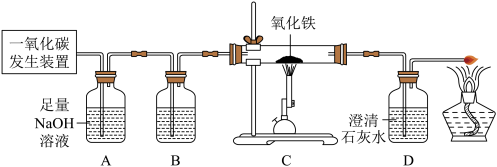
海水是一种丰富的资源,从海水中获得的粗盐中含有NaCl、MgCl2、CaCl2、Na2SO4、泥沙等物质,粗盐中的难溶性杂质去除之后可获得精盐,为了从中提取氯化镁和氯化钠,设计实验方案如下:
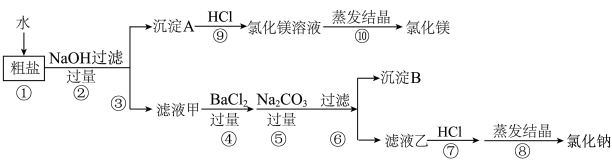
(1)写出步骤⑨中反应的化学方程式________________
(2)步骤⑤⑥的顺序颠倒会导致什么后果?____________
(3)在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?_______ 原因是什么?______________

(1)写出步骤⑨中反应的化学方程式
(2)步骤⑤⑥的顺序颠倒会导致什么后果?
(3)在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?
更新时间:2020/06/04 17:27:42
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】化学试剂常常要密封保存,但原因各不相同。
(1)浓盐酸密封保存的原因是什么_____ ?
(2)氢氧化钠溶液若敞口放置会发生变质,请用化学方程式表示其变质原因_____ 。
(3)如何检验NaOH溶液是否完全变质,请简述实验方法_____ 。
(1)浓盐酸密封保存的原因是什么
(2)氢氧化钠溶液若敞口放置会发生变质,请用化学方程式表示其变质原因
(3)如何检验NaOH溶液是否完全变质,请简述实验方法
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】盐酸是氯化氢气体(HCl)的水溶液,有挥发性,回答问题。
(1)打开盛浓盐酸的试剂瓶的瓶塞,闻到刺激性气味,体现分子具有的性质是___________ 。
(2)加热条件下,浓盐酸与二氧化锰发生反应: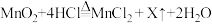 。X是一种气体单质,则X的化学式是
。X是一种气体单质,则X的化学式是___________ 。
(3)实验室制取H2的反应原理: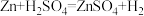 ↑,若用稀盐酸代替稀硫酸,制得的H2中会混入的气体杂质是
↑,若用稀盐酸代替稀硫酸,制得的H2中会混入的气体杂质是___________ 。
(1)打开盛浓盐酸的试剂瓶的瓶塞,闻到刺激性气味,体现分子具有的性质是
(2)加热条件下,浓盐酸与二氧化锰发生反应:
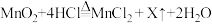 。X是一种气体单质,则X的化学式是
。X是一种气体单质,则X的化学式是(3)实验室制取H2的反应原理:
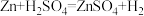 ↑,若用稀盐酸代替稀硫酸,制得的H2中会混入的气体杂质是
↑,若用稀盐酸代替稀硫酸,制得的H2中会混入的气体杂质是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】已知酸性物质可使紫色的石蕊试液变成红色,某同学为了探究微粒的一些性质,设计了如下的系列实验:

(1)向一小烧杯中加入蒸馏水,然后滴加紫色石蕊试液(如图Ⅰ),观察到的实验现象是烧杯里的水变成了________ 色,该实验说明水呈 ____________ 的性质(选填:酸性,中性,碱性)。
(2)向(Ⅰ)中的烧杯中再加入稀盐酸,观察到的实验是紫色石蕊试液变成________ 色。
(3)分别取A、B两个烧杯,A杯中加入蒸馏水,再向其中加入紫色石蕊,B杯中盛有浓盐酸,用一大烧杯把A、B两烧杯的溶液罩在一起(如图Ⅱ),过一段时间后观察到的现象是A烧杯中的紫色石蕊试液变________________ 色。该实验说明构成物质的微粒总是在 __________________ 。
(4)上述实验还说明浓盐酸的两个重要的性质分别是:
①物理性质:浓盐酸具有______________ 性
②化学性质:浓盐酸具有_____________ 性。(选填,酸性或碱性)

(1)向一小烧杯中加入蒸馏水,然后滴加紫色石蕊试液(如图Ⅰ),观察到的实验现象是烧杯里的水变成了
(2)向(Ⅰ)中的烧杯中再加入稀盐酸,观察到的实验是紫色石蕊试液变成
(3)分别取A、B两个烧杯,A杯中加入蒸馏水,再向其中加入紫色石蕊,B杯中盛有浓盐酸,用一大烧杯把A、B两烧杯的溶液罩在一起(如图Ⅱ),过一段时间后观察到的现象是A烧杯中的紫色石蕊试液变
(4)上述实验还说明浓盐酸的两个重要的性质分别是:
①物理性质:浓盐酸具有
②化学性质:浓盐酸具有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】如图中A、B、C、D、E、F六种物质及他们之间的关系均为初中化学常见的。其中A、B、C、D、E为不同类别的物质,A在工业上广泛用于制取肥皂,C是胃液的主要成分(图中用“—”表示两种物质间能发生反应, 用“→”或“ ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。______ ;E:______ 。
(2)写出C和F反应的化学方程式_____ 。
(3)D和足量的C反应的现象是:黑色固体逐渐________ 。
 ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。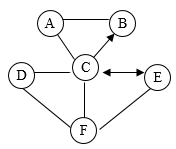
(2)写出C和F反应的化学方程式
(3)D和足量的C反应的现象是:黑色固体逐渐
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】小苏打和食盐是厨房中常见物质。现有一包白色固体,可能由碳酸氢钠、氯化钠中的一种或两种物质组成。某科学小组同学展开了系列研究。
【实验目的】确定白色固体的组成
【实验方案】如图所示:
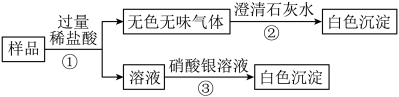
【实验结论】小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤①发生反应的化学方程式是_____________ 。步骤③发生反应的化学方程式是 _________
(2)步骤②中的澄清石灰水也可以用其他碱溶液代替,如_______________ 。
(3)科学小组认真研究讨论后认为,此方案不能得出小明同学的结论。理由是:______ ,一致认为将上述方案中使用的一种试剂进行调换,如仍出现上述现象,则小明同学的结论正确。调换措施是 ______________ 。
【实验目的】确定白色固体的组成
【实验方案】如图所示:

【实验结论】小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤①发生反应的化学方程式是
(2)步骤②中的澄清石灰水也可以用其他碱溶液代替,如
(3)科学小组认真研究讨论后认为,此方案不能得出小明同学的结论。理由是:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2 杂质。用该矿石制备 Mg(OH)2 的工艺流程简图如图:
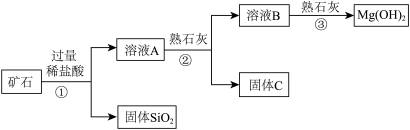
回答下列问题:
(1)步骤①和步骤②均用到的操作是_____________ ;
(2)步骤①中加过量稀盐酸的目的是______________ ;
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH见下表:
步骤②加入熟石灰,调节溶液的 pH 范围为________________ 。

回答下列问题:
(1)步骤①和步骤②均用到的操作是
(2)步骤①中加过量稀盐酸的目的是
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH见下表:
| 对应离子 | Fe3+ | Cu2+ | Mg2+ |
| 开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为
您最近一年使用:0次
【推荐1】海洋是巨大的资源宝库。“筑梦”学习小组模拟化工厂生产流程,利用海水制取纯碱和金属镁,设计方案如图所示。请回答下列问题。
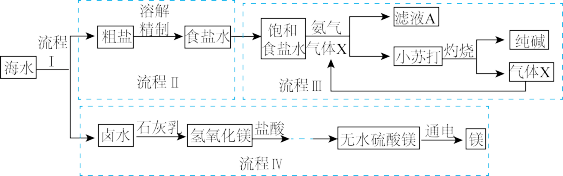
(1)流程I为海水晒盐的过程。结晶池中析出晶体后的母液是氯化钠的_______ (填“饱和”或“不饱和”)溶液。
(2)流程II为除去粗盐水中的CaC2、MgCl2和Na2SO4、和杂质。加入下列3种过量试剂的顺序依次可以是 (填字母序号);
(3)流程III为海水“制碱”。制取小苏打(碳酸氢钠)通入的气体X的化学式为__ ;在该流程中,是先向饱和食盐水中通入过量的氨气,然后再通入过量的二氧化碳,先通入过量氨气的目的是___ 。
(4)流程IV为海水提镁。氢氧化镁和盐酸反应的化学方程式为_______ 。海水中本来就有氯化镁,不直接将海水进行电解来制取金属镁,而是经过了加石灰乳、盐酸等过程,目的是_______ 。

(1)流程I为海水晒盐的过程。结晶池中析出晶体后的母液是氯化钠的
(2)流程II为除去粗盐水中的CaC2、MgCl2和Na2SO4、和杂质。加入下列3种过量试剂的顺序依次可以是 (填字母序号);
| A.Na2CO3、NaOH、BaCl2 | B.BaCl2、Na2CO3、NaOH | C.NaOH、BaCl2、Na2CO3 |
(3)流程III为海水“制碱”。制取小苏打(碳酸氢钠)通入的气体X的化学式为
(4)流程IV为海水提镁。氢氧化镁和盐酸反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】粗盐中常含有氯化钙,氯化镁,碳酸钠等杂质。得到氯化钠晶体的流程如下。
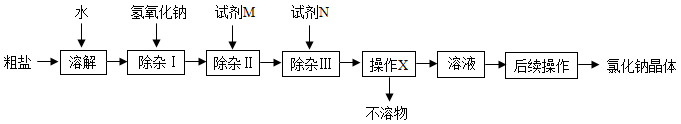
﹙1﹚为了使杂质能够完全被除去,对所加入试剂的量的要求是_________ ;
﹙2﹚操作X是___________ ;
﹙3﹚加入试剂N可以除去的杂质是____________ ;
﹙4﹚后续操作是______________________ 。

﹙1﹚为了使杂质能够完全被除去,对所加入试剂的量的要求是
﹙2﹚操作X是
﹙3﹚加入试剂N可以除去的杂质是
﹙4﹚后续操作是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】海洋资源丰富,应用前景广阔。
(1)海水淡化:将海水转化为淡水可以有效地解决淡水短缺的问题,工业上常采用的海水淡化方法有_______ (填一种方法即可)。
(2)海水晒盐:海水通过蒸发池、结晶池析出晶体后的“母液”是氯化钠的_______ 溶液(填“饱和”或“不饱和”)。
(3)海水制镁:先将海水中氯化镁转化为氢氧化镁沉淀,再加入稀盐酸将其转化为氯化镁溶液,目的是_______ 。
(4)粗盐精制:
①实验室里除去粗盐中难溶性杂质一般步骤为溶解、过滤、蒸发,这三种基本操作中都要使用的玻璃仪器是_______ 。
②粗盐水中主要含有Ca2+、Mg2+、 等杂质离子,工业上常用加入稍过量的A.NaOH溶液、B.Na2CO3溶液、C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证Na2CO3溶液在加入
等杂质离子,工业上常用加入稍过量的A.NaOH溶液、B.Na2CO3溶液、C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证Na2CO3溶液在加入_______ 之后再加入即可(填试剂序号)。
(5)海水“制碱”:我国化学家侯德榜创立的联合制碱法的优点有_______。
(6)海底矿物:“可燃冰”是一种新型和矿产资源,它是由天然气(主要成分为_______ )与水在低温、高压下形成的块状固体,被称为“未来能源”。
(7)除了海水化学资源和海底矿产资源外,海洋还蕴含着丰富的_______ 资源。(写一点即可)
(1)海水淡化:将海水转化为淡水可以有效地解决淡水短缺的问题,工业上常采用的海水淡化方法有
(2)海水晒盐:海水通过蒸发池、结晶池析出晶体后的“母液”是氯化钠的
(3)海水制镁:先将海水中氯化镁转化为氢氧化镁沉淀,再加入稀盐酸将其转化为氯化镁溶液,目的是
(4)粗盐精制:
①实验室里除去粗盐中难溶性杂质一般步骤为溶解、过滤、蒸发,这三种基本操作中都要使用的玻璃仪器是
②粗盐水中主要含有Ca2+、Mg2+、
 等杂质离子,工业上常用加入稍过量的A.NaOH溶液、B.Na2CO3溶液、C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证Na2CO3溶液在加入
等杂质离子,工业上常用加入稍过量的A.NaOH溶液、B.Na2CO3溶液、C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证Na2CO3溶液在加入(5)海水“制碱”:我国化学家侯德榜创立的联合制碱法的优点有_______。
| A.没有“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境 |
| B.大大提高了食盐的利用率,节约了成本 |
| C.将“制碱”与制氨生产联合起来,同时反应均不需要加热,可节约能源 |
(7)除了海水化学资源和海底矿产资源外,海洋还蕴含着丰富的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐1】从海水得到的粗盐,往往含有可溶性杂质(主要有)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活.粗盐提纯的部分流程如下:
其中,滤液一至滤液二之间需进行三步操作:
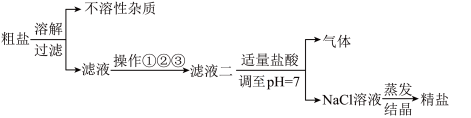
操作一: 加入过量的碳酸钠,除去滤液中的Ca2+
操作二: 加入过量的X,除去滤液中的Mg2+
操作三: 加入过量的氯化钡,除去滤液中的SO42-
请回答:
(1)操作中的物质X为___________ ,正确的操作顺序为_______________________ (填序号),为最终获得精盐,操作①、②和③后还需增加的操作是________________________ ;
(2)滤液二中加入适量稀盐酸的目的是____________________________ .
其中,滤液一至滤液二之间需进行三步操作:

操作一: 加入过量的碳酸钠,除去滤液中的Ca2+
操作二: 加入过量的X,除去滤液中的Mg2+
操作三: 加入过量的氯化钡,除去滤液中的SO42-
请回答:
(1)操作中的物质X为
(2)滤液二中加入适量稀盐酸的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国制碱工业先驱侯德榜发明了“侯氏制碱法”。在充分利用空气资源和海洋资源的基础上,结合“侯氏制碱法”的基本原理,模拟流程如图。
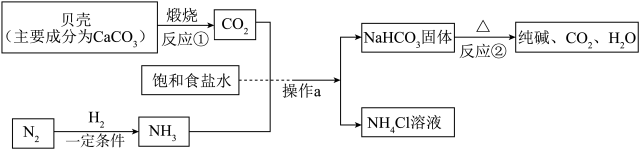
请回答下列问题:
(1)粉碎贝壳的目的是______________ 。
(2)分离液态空气法制得氮气属于_______ (填“物理变化”还是“化学变化”)。
(3)操作a的名称是_______ ,写出NH4Cl的一种用途______________ 。
(4)上述流程中除NH3外还可循环利用的物质有______________ 。
(5)在实际生产的产品碳酸钠中会混有少量的氯化钠,现有该样品混合物12.4 g,将其放入一洁净的烧杯中,向其中逐滴滴入7.3%的稀盐酸,放出气体质量与滴加稀盐酸质量的关系如图所示。
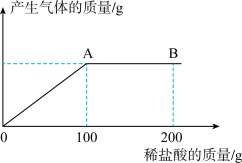
请回答下列问题。
①当滴加稀盐酸至图中B点时,烧杯中溶液的pH_______ (填“>”“<”或“=”)7。
②该样品混合物中碳酸钠的质量分数___________ 。

请回答下列问题:
(1)粉碎贝壳的目的是
(2)分离液态空气法制得氮气属于
(3)操作a的名称是
(4)上述流程中除NH3外还可循环利用的物质有
(5)在实际生产的产品碳酸钠中会混有少量的氯化钠,现有该样品混合物12.4 g,将其放入一洁净的烧杯中,向其中逐滴滴入7.3%的稀盐酸,放出气体质量与滴加稀盐酸质量的关系如图所示。

请回答下列问题。
①当滴加稀盐酸至图中B点时,烧杯中溶液的pH
②该样品混合物中碳酸钠的质量分数
您最近一年使用:0次