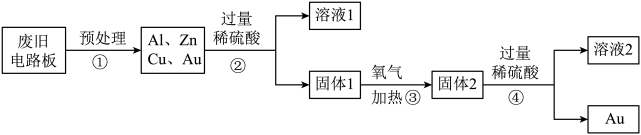
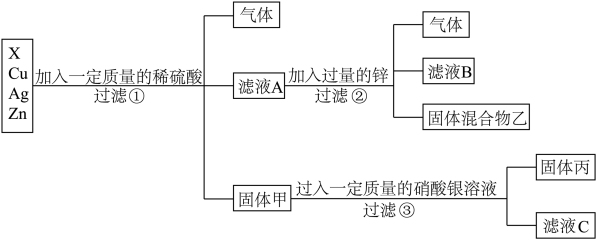
金属及金属材料具有广泛的应用。
Ⅰ纽扣电池是生活中常用的电源。
(1)纽扣电池的金属外壳可以加工得很薄,说明金属具有________________ 性。
(2)某纽扣电池中涉及到铜和银等金属,从所给试剂中选取合适药品设计实验方案比较铜和银的金属活动性强弱。试剂:铜丝、银丝、稀盐酸、硝酸银溶液、硫酸铝溶液。
Ⅱ运用手持技术探究金属与酸的反应。向 250mL 的烧瓶内注入 25mL 某浓度的稀盐酸(足量),分别剪取相同长度和宽度、质量的镁、铝、锌、铁、铜金属片,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图 1),点击采集,得到如图 2 所示的变化曲线。
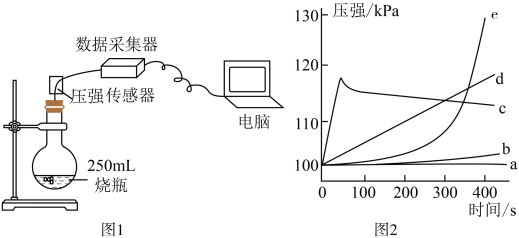
(1)曲线 b 对应的金属是铁,反应的化学方程式为___________________ 。
(2)曲线 c 在 18s 左右达到最高点后又略微下降的原因是____________________ 。
(3)下列说法不正确的是________________ (填字母)。
A曲线a 对应的金属是铜
B曲线d 对应的反应速率适中,适合实验室制取气体
C曲线e 在 0~100s 段几乎没有上升,可能是该金属打磨不彻底
D曲线e 在 300s 后迅速上升,是因为盐酸浓度变大
E如延长横坐标时间,曲线 c、d、e 最终将交于一点
Ⅲ氢气的储存是科学研究热点之一。某镁铜合金 X 是一种储存氢气的材料,高温时在氩气保护下,由一定质量比的 Mg、Cu 单质熔炼获得。
(1)制取X 时不能在空气中熔炼的原因是___________ (任写一个有关反应的化学方程式)。
(2)取 11.2gX 在 O2 中完全燃烧,生成 8.0g MgO 和 8.0g CuO。则X 中各元素的原子个数比为___________ 。
Ⅰ纽扣电池是生活中常用的电源。
(1)纽扣电池的金属外壳可以加工得很薄,说明金属具有
(2)某纽扣电池中涉及到铜和银等金属,从所给试剂中选取合适药品设计实验方案比较铜和银的金属活动性强弱。试剂:铜丝、银丝、稀盐酸、硝酸银溶液、硫酸铝溶液。
| 实验方案 | 实验现象 | 结论 |
| 铜的金属活动性比银强 | ||
| 有关反应的化学方程式为 |

(1)曲线 b 对应的金属是铁,反应的化学方程式为
(2)曲线 c 在 18s 左右达到最高点后又略微下降的原因是
(3)下列说法不正确的是
A曲线a 对应的金属是铜
B曲线d 对应的反应速率适中,适合实验室制取气体
C曲线e 在 0~100s 段几乎没有上升,可能是该金属打磨不彻底
D曲线e 在 300s 后迅速上升,是因为盐酸浓度变大
E如延长横坐标时间,曲线 c、d、e 最终将交于一点
Ⅲ氢气的储存是科学研究热点之一。某镁铜合金 X 是一种储存氢气的材料,高温时在氩气保护下,由一定质量比的 Mg、Cu 单质熔炼获得。
(1)制取X 时不能在空气中熔炼的原因是
(2)取 11.2gX 在 O2 中完全燃烧,生成 8.0g MgO 和 8.0g CuO。则X 中各元素的原子个数比为
更新时间:2021/01/25 12:08:40
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
名校
【推荐1】用赤铁矿冶炼生铁的化学原理是__ (用化学方程式表示),铁制品在潮湿的空气中生锈是由于铁与空气中的水蒸气和__ 反应生成铁锈,配制农药“波尔多液”时不用铁桶盛装硫酸铜溶液的原因是_____ (用化学方程式表示),常见金属铁、锌、铝的金属活动性顺序是_____ .
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】“实以立人廿载春风播雨露,验以求真满园桃李竞芳菲”,我校迎来建校20周年。已知A~F为初中化学常见的六种物质,图中数字“2”中相连物质可以发生反应,数字“0”中相连物质按“逆时针”方向可以转化,符号“ ”指向生成物。其中B是地壳中含量最高的金属;D能使带火星的木条复燃,B和D相连能反应;A与C中有相同原子团,且C的浓溶液溶于水放热;E、F为元素种类相同的氧化物。
”指向生成物。其中B是地壳中含量最高的金属;D能使带火星的木条复燃,B和D相连能反应;A与C中有相同原子团,且C的浓溶液溶于水放热;E、F为元素种类相同的氧化物。

(1)若E中含碳元素的质量分数高于F。
①在自然界中通过______ 实现“F→D”的转化。
②物质D由______ 构成(填“分子”、“原子”、“离子”)。
(2)若转化“E→F”发生的反应是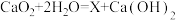 ,X为物质F,F的名称为
,X为物质F,F的名称为_____ 。
(3)日常生活中物质B耐腐蚀的原因_______ 。
(4)A和B反应的化学方程式可能为______ ,该反应的基本反应类型是____ 反应。
 ”指向生成物。其中B是地壳中含量最高的金属;D能使带火星的木条复燃,B和D相连能反应;A与C中有相同原子团,且C的浓溶液溶于水放热;E、F为元素种类相同的氧化物。
”指向生成物。其中B是地壳中含量最高的金属;D能使带火星的木条复燃,B和D相连能反应;A与C中有相同原子团,且C的浓溶液溶于水放热;E、F为元素种类相同的氧化物。
(1)若E中含碳元素的质量分数高于F。
①在自然界中通过
②物质D由
(2)若转化“E→F”发生的反应是
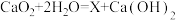 ,X为物质F,F的名称为
,X为物质F,F的名称为(3)日常生活中物质B耐腐蚀的原因
(4)A和B反应的化学方程式可能为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】某兴趣小组同学从实验室中收集到一桶废液,他们想从中回收金属铜和硫酸亚铁,于是设计了以下流程图

(1)固体A的成分为______ ;操作a和操作b都要用到一种玻璃仪器,该仪器在操作a中的作用是_______ 。
(2)加入Y时发生反应的化学方程式为________ 。
(3)理论上所得硫酸亚铁晶体的质量_________ (填“>”“<”或“=”)原废液中硫酸亚铁的质量。

(1)固体A的成分为
(2)加入Y时发生反应的化学方程式为
(3)理论上所得硫酸亚铁晶体的质量
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐2】某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,其稀溶液X具有如下转化关系。A、B、C、D、E、F、G、M、N都是初中常见的化学物质。已知:B、C、F都是氧化物,通常状况下它们分别是无色无味液体、无色无味气体和黑色粉末状固体;G是通常状况下密度最小的气体。(图中部分反应物、生成物已略去)。请回答下列问题:
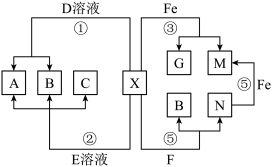
(1)写出化学式:G____________ ,X______________ ;
(2)写出化学反应的类型:反应⑤_________________ ;
(3)写出符合题意的化学方程式:
反应②________________________________________________ ;
反应③_________________________________________________ ;
反应④_________________________________________________ 。

(1)写出化学式:G
(2)写出化学反应的类型:反应⑤
(3)写出符合题意的化学方程式:
反应②
反应③
反应④
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】图中 A~I 为初中化学常见物质,且分别由 H、O、Cl、S、Fe、Cu、Al 中的一种或几种元素组成。F 在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能; 只有 G 由三种元素组成:A、B、C、F、I均为单质;H、G 类别相同;图中“→”表示转化关系,“—”表示相互之间能发生反应(部分反应物、生成物及反应条件省略)。
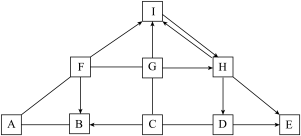
(1)写出 F 的化学式:______ 。
(2)写出 I→H 反应的化学方程式______ 。
(3)G 和 C 反应的基本反应类型为______ 。
(4)如 E 和F 含有同一种金属元素,写出 D→E 反应的化学方程式______ 。

(1)写出 F 的化学式:
(2)写出 I→H 反应的化学方程式
(3)G 和 C 反应的基本反应类型为
(4)如 E 和F 含有同一种金属元素,写出 D→E 反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】已知某工业废水中含有大量FeSO4较多的CuSO4少量的Na2SO4以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
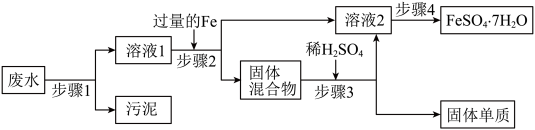
(1)步骤1、步骤2、步骤3的主要操作是相同的,需用到的玻璃仪器除烧杯和玻璃棒外还有_____ 。
(2)步骤2中发生反应的化学方程式为_____ 。
(3)步骤3中发生反应的化学方程式为_____ 。
(4)步骤4中涉及的操作是:蒸发浓缩、降温结晶、过滤、洗涤、烘干,过滤后滤液中还存在的金属阳离子有_____ 。
(5)最后的固体单质是_____ (填名称)
(6)若测得某溶液中仅有钠离子、镁离子、硫酸根离子、氯离子这四种离子,已知钠离子、镁离子、氯离子个数之比为4:5:8,若钠离子为4n个,则硫酸根离子的个数是_____ 。

(1)步骤1、步骤2、步骤3的主要操作是相同的,需用到的玻璃仪器除烧杯和玻璃棒外还有
(2)步骤2中发生反应的化学方程式为
(3)步骤3中发生反应的化学方程式为
(4)步骤4中涉及的操作是:蒸发浓缩、降温结晶、过滤、洗涤、烘干,过滤后滤液中还存在的金属阳离子有
(5)最后的固体单质是
(6)若测得某溶液中仅有钠离子、镁离子、硫酸根离子、氯离子这四种离子,已知钠离子、镁离子、氯离子个数之比为4:5:8,若钠离子为4n个,则硫酸根离子的个数是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】为测定某工厂废铁屑(杂质不溶于水不与酸反应且不含铁元素)中铁的含量,某化学兴趣小组,进行如下实验:

(1)上述实验过程中发生反应的化学方程式为___________ 。
(2)根据已知条件列出求解参加反应铁质量(x)的比例式___________ 。
(3)用36.5%的浓盐酸配制上述实验稀盐酸,需要浓盐酸的质量为___________ 。
(4)废铁屑中铁的含量为___________ 。
(5)若要使滤液质量分数变为12.7%,需蒸发水的质量___________ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解参加反应铁质量(x)的比例式
(3)用36.5%的浓盐酸配制上述实验稀盐酸,需要浓盐酸的质量为
(4)废铁屑中铁的含量为
(5)若要使滤液质量分数变为12.7%,需蒸发水的质量
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】金属材料在历史发展中有着重要的作用,请用金属的相关知识解释下列问题。

(1)在四川三星堆遗址出土大量重要文物,其中有巨青铜面具如图甲,其制作材料属于______ (填“金属”或“合成”)材料,其中出土的“黄金面具”为一整块金箔制作,最薄处仅0.2毫米,说明金具有良好的______ 性。
(2)对钢铁制品进行“发蓝”处理,使表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程发生了______ (填“物理变化”或“化学变化”)。
②致密氧化膜能防止钢铁锈蚀的原因是______ 。
(3)某同学用图乙所示实验来验证铜与银的金属活动性强弱,则X、Y分别是______ ,其反应的化学方程式是______ 。
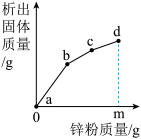
(4)往含有AgNO3、Cu(NO3)2、Fe(NO3)2的废水中缓慢连续加入质量为m的锌粉,溶液中析出固体质量与参加反应的锌质量关系如图所示,下列说法中正确的是______。(填字母序号)

(1)在四川三星堆遗址出土大量重要文物,其中有巨青铜面具如图甲,其制作材料属于
(2)对钢铁制品进行“发蓝”处理,使表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程发生了
②致密氧化膜能防止钢铁锈蚀的原因是
(3)某同学用图乙所示实验来验证铜与银的金属活动性强弱,则X、Y分别是
(4)往含有AgNO3、Cu(NO3)2、Fe(NO3)2的废水中缓慢连续加入质量为m的锌粉,溶液中析出固体质量与参加反应的锌质量关系如图所示,下列说法中正确的是______。(填字母序号)

| A.c点对应溶液中含有的金属离子为Zn2+和Cu2+ |
| B.bc段(不含两端点)析出的金属是Fe |
| C.ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+ |
| D.若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1,和m2,则m1>m2 |
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐2】某同学进行了如图所示的实验,探究Ag、Zn、Cu三种金属的活动性强弱,请分析回答:
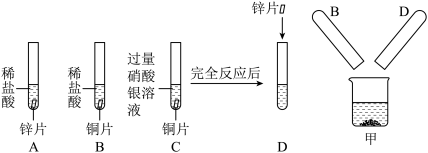
(1)试管A中反应的化学方程式是__________________________________ ,C中实验现象是 ___________________________________ ,由实验A、B、C可推断出Ag、Zn、Cu三种 金属的活动性由强到弱的顺序为 _________________ 。
(2)向C完全反应后的试管里加入一定质量的锌片,D试管中一定会发生的反应是_____________________________________ (用化学方程式表示)。
(3)完全反应后,将B、D试管反应后的物质全部倒入烧杯甲中,无明显现象产生,则烧杯甲中的固体物质是___________ ,溶液中一定含有的溶质是 ______________ 。

(1)试管A中反应的化学方程式是
(2)向C完全反应后的试管里加入一定质量的锌片,D试管中一定会发生的反应是
(3)完全反应后,将B、D试管反应后的物质全部倒入烧杯甲中,无明显现象产生,则烧杯甲中的固体物质是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】金属的冶炼为国民经济的发展奠定了坚实的基础,金属活动性顺序在生产和生活中有重要的应用。
(1)铁制品与_____ 接触易生锈。
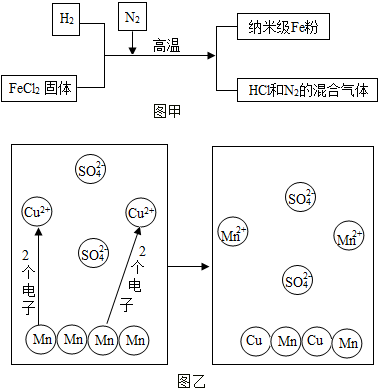
(2)新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图甲所示:请回答下列问题:
请上述制备工艺的化学方程式_____ ; 在制备纳米级 Fe 粉的工艺流程中,N2的作用是_____ 。
(3)图乙为Mn和 CuSO4溶液反应的示意图,实际与Mn反应的微粒是_____ 。
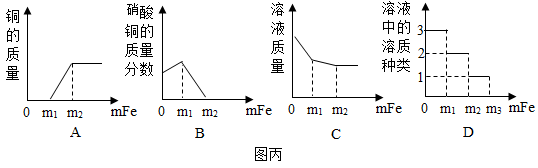
(4)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,铁粉先与_____ 反应,充分反应后,他对反应过程进行了分析,得到了图丙的几个图象(横坐标表示加入铁的质量),其中错误的是_____ (填字母序号)。


(1)铁制品与
(2)新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图甲所示:请回答下列问题:
请上述制备工艺的化学方程式
(3)图乙为Mn和 CuSO4溶液反应的示意图,实际与Mn反应的微粒是
(4)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,铁粉先与
您最近一年使用:0次