垃圾合理化回收利用可以减少污染,节约资源。黄铁矿制硫酸会产生大量废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)可制备黄钠铁矾净水剂和高档颜料铁红(Fe2O3),其流程如图:
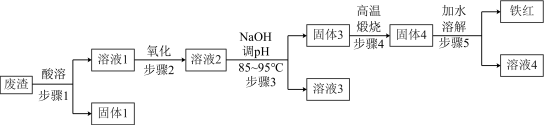
已知:①“固体3”为黄钠铁矾,化学式为:NaFe3(SO4)2(OH)6。
②“溶液4”是含有Na+的可溶盐。
③通过调节pH范围可使某种金属沉淀。下表是物质开始沉淀与沉淀完全的pH。
(1)NaFe3(SO4)2(OH)6中铁元素的化合价为______ ,为使铁元素以黄钠铁矾形式沉淀完全,步骤3调节pH的数值范围为______ ,溶液3中溶质的成分是______ (任写一种)。
(2)“氧化”过程中,需要加入一种将Fe2+氧化为Fe3+的物质,工业上最好选用______ 。
A 空气 B H2O2 C MnO2 D O2
(3)“酸溶”时MgO参加反应的化学方程式为______ 。
(4)步骤5中检验铁红是否洗涤干净的操作是:取最后一次洗涤液少量于试管中,______ ,证明已洗涤干净。

已知:①“固体3”为黄钠铁矾,化学式为:NaFe3(SO4)2(OH)6。
②“溶液4”是含有Na+的可溶盐。
③通过调节pH范围可使某种金属沉淀。下表是物质开始沉淀与沉淀完全的pH。
| NaFe3(SO4)2(OH)6 | Fe(OH)3 | Mg(OH)2 | |
| 开始沉淀的pH | 1.6 | 2.0 | 8.1 |
| 沉淀完全的pH | 1.8 | 3.2 | 9.4 |
(2)“氧化”过程中,需要加入一种将Fe2+氧化为Fe3+的物质,工业上最好选用
A 空气 B H2O2 C MnO2 D O2
(3)“酸溶”时MgO参加反应的化学方程式为
(4)步骤5中检验铁红是否洗涤干净的操作是:取最后一次洗涤液少量于试管中,
2020·甘肃兰州·中考真题 查看更多[1]
更新时间:2021/04/03 21:33:43
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
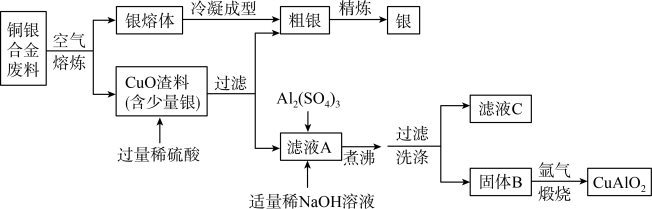
【推荐1】p型透明导电化合物CuAlO2具有良好的热电性能,在热电转换领域具有广阔的应用前景。银铜合金广泛用于航空工业,以下为从航空切割废料中回收银并制备CuAlO2的工艺流程。
Ⅱ.CuAlO2受热易氧化、高温易分解,银在空气中不易被氧化。
(1)CuAlO2中铜元素的化合价为___________ ,过滤后所得滤液A中的阳离子有___________ (填离子符号);
(2)滤液A充分反应后,煮沸过程中发生反应的化学方程式为___________ ;
(3)固体B在煅烧时发生的一个反应的化学方程式为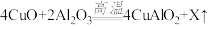 ,气体X的化学式为
,气体X的化学式为___________ ;
(4)“煅烧”时温度须控制在1042℃~1085℃范围内且在氩气中进行,其原因是___________ 。
Ⅱ.CuAlO2受热易氧化、高温易分解,银在空气中不易被氧化。
(1)CuAlO2中铜元素的化合价为
(2)滤液A充分反应后,煮沸过程中发生反应的化学方程式为
(3)固体B在煅烧时发生的一个反应的化学方程式为
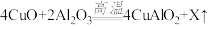 ,气体X的化学式为
,气体X的化学式为(4)“煅烧”时温度须控制在1042℃~1085℃范围内且在氩气中进行,其原因是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸铁铵NH4Fe(SO4)2·xH2O是一种重要的化合物,常用于物质检测的指示剂。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:回答下列问题: ____________ (填“酸”、“碱”、“盐”),其中铁元素的化合价是____________ 。
(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有 。
(3)步骤②中发生的反应化学方程式为____________ 。该反应加热的目的是____________ 。温度欲保持在80~90℃,采用的合适加热方式是____________ 。
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为____________ 。反应过程中要分批加入H2O2溶液,原因是____________ 。
(5)步骤⑤的具体实验操作有:________ 、降温结晶、过滤、洗涤、干燥得到硫酸铁铵晶体样品。
(6)为测定硫酸铁铵所带结晶水个数,实验小组进行了如下实验:称取4.82g硫酸铁铵晶体溶于水,加入足量BaCl2溶液,将生成的沉淀经过滤、洗涤、干燥,测得质量为4.66g。请通过计算确定x的值(要有计算过程)____________ 。实验过程中,若沉淀未洗涤干净,则测得的x的值会_______ (“偏大”、“偏小”、“无影响”)。

(2)步骤①的目的是除去废铁屑表面的油污,可选择的试剂有 。
| A.稀盐酸 | B.纯碱溶液 | C.氢氧化钠溶液 |
(4)步骤③中的反应为2FeSO4+X+H2O2=Fe2(SO4)3+2H2O(放热),X的化学式为
(5)步骤⑤的具体实验操作有:
(6)为测定硫酸铁铵所带结晶水个数,实验小组进行了如下实验:称取4.82g硫酸铁铵晶体溶于水,加入足量BaCl2溶液,将生成的沉淀经过滤、洗涤、干燥,测得质量为4.66g。请通过计算确定x的值(要有计算过程)
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】铁红(Fe2O3)常用于油漆、油墨、橡胶等工业中,现以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:
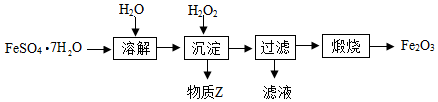
已知沉淀时的主要反应为: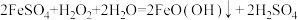
(1)FeO(OH)中铁元素的化合价为______ 。
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是______ (填字母)。
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,______ (写出操作和现象),则沉淀已洗涤干净。
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于______ 反应(选填“放热”或“吸热”)。为了加快煅烧的反应速率,可以将固体______ (填操作名称)。
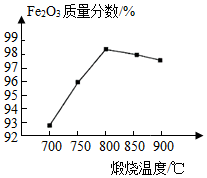
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达______ ℃时,Fe2O3的质量分数最高。若继续升高温度,所得产品发黑且铁元素质量分数升高,同时有无色气体产生,其可能原因是______ (用化学反应方程式表示)。

已知沉淀时的主要反应为:
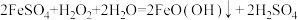
(1)FeO(OH)中铁元素的化合价为
(2)沉淀时需调节溶液的初始pH约为4,过程中需不断加入物质Z调节溶液的pH,保持溶液的pH为3.0-4.5,Z应该具备的性质是
A.不与FeO(OH)反应 B.能与酸反应 C.能与碱反应
(3)为保证产品纯度,需对沉淀进行洗涤。检验沉淀是否洗涤干净的方法:用适量蒸馏水淋洗过滤器中的沉淀2-3次,取少量最后一次淋洗下来的液体,
(4)在煅烧过程中需要不断加热,以达到高温条件,说明该反应可能属于
(5)如图为其他条件相同时,不同煅烧温度对产品中Fe2O3质量分数的影响。当煅烧温度达

您最近一年使用:0次
【推荐1】近年来新冠病毒疫情已成为国际关注的突发公共卫生事件。
(1)“新冠肺炎”危重症患者主要表现为肺部纤维化,呼吸功能受阻,此时可用于医疗急救的气体是______ (填化学式)。
(2)KN95活性炭口罩可以有效过滤病毒还能除去异味,利用的是活性炭的______ 作用。
(3)适当补充蛋白质可以提高自身免疫性,因此我们日常可以食用______ (填一种食物)。
(4)用酒精消毒时,能闻到酒精散发出的特殊气味,主要是因为______ 。
(5)为配制质量分数为0.04%的消毒液用于餐具消毒,可将质量分数为6.0%的84消毒液与水按质量比为1:______ 进行稀释。
(1)“新冠肺炎”危重症患者主要表现为肺部纤维化,呼吸功能受阻,此时可用于医疗急救的气体是
(2)KN95活性炭口罩可以有效过滤病毒还能除去异味,利用的是活性炭的
(3)适当补充蛋白质可以提高自身免疫性,因此我们日常可以食用
(4)用酒精消毒时,能闻到酒精散发出的特殊气味,主要是因为
(5)为配制质量分数为0.04%的消毒液用于餐具消毒,可将质量分数为6.0%的84消毒液与水按质量比为1:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
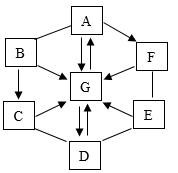
【推荐2】A、B、C、D、E、F是初中化学常见的物质,A、C、D、F均为气体,且A为生命必需的气体,C为光合作用必需的气体,D为最轻的气体,F为沼气的主要成分。它们之间的转化关系如下图所示,根据信息和图示回答问题(反应条件和部分生成物已略去)。
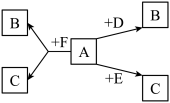
(1)B的化学式________ ;E的化学式_________ 。
(2)写出A+F→B+C反应的化学方程式:__________ 。

(1)B的化学式
(2)写出A+F→B+C反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】金属在生产生活中应用广泛。
(1)新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如图甲所示,请写出上述制备工艺的化学方程式_____ 。氮气的作用是_____ 。
(2)图乙为Mn和CuSO4溶液反应的示意图,实际与Mn反应的微粒是_____ ,由反应可知金属的活泼性:Cu_____ Mn(填“>”或“<”)
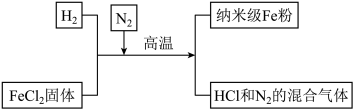
图甲
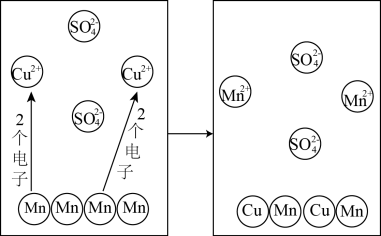
图乙
(3)工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中反应的化学方程式为_____ 。
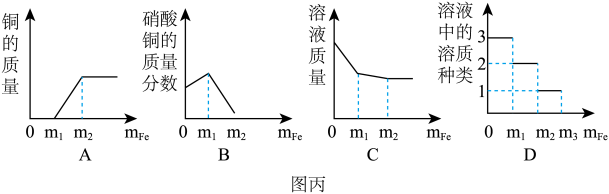
(4)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了图丙的几个图象(横坐标表示加入铁的质量),其中错误的是_____ (填字母序号)。
(1)新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如图甲所示,请写出上述制备工艺的化学方程式
(2)图乙为Mn和CuSO4溶液反应的示意图,实际与Mn反应的微粒是

图甲

图乙
(3)工人师傅切割铁板时,常用硫酸铜溶液在铁板上画线即可留下红色的印迹,此过程中反应的化学方程式为
(4)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了图丙的几个图象(横坐标表示加入铁的质量),其中错误的是

您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】某金属冶炼厂的管道烟泥中含有Cu、Zn及S等,现欲回收铜和锌,主要流程如图所示:
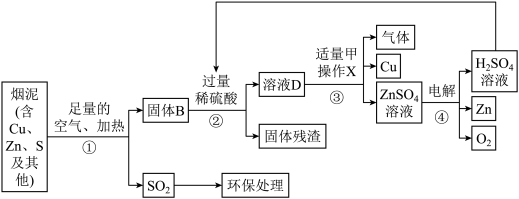
(1)步骤②中生成蓝色溶液的化学方程式为:____________ ;加入过量稀硫酸的作用是_____________ 。
(2)步骤③中甲的化学式为__________ 。步骤③中操作X的名称是___________ 。
(3)步骤④中反应的化学方程式为_____________ 。
(4)该工业流程中,可以循环利用的一种物质是______________ (填化学式)。

(1)步骤②中生成蓝色溶液的化学方程式为:
(2)步骤③中甲的化学式为
(3)步骤④中反应的化学方程式为
(4)该工业流程中,可以循环利用的一种物质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】现有编号为①②③④的四瓶无色液体,仅知道是稀盐酸、食盐水、Ca(OH)2溶液和酚酞试液。现要求甲、乙、丙、丁四位学生进行鉴别,且每人只鉴别两瓶溶液。实验成绩评定标准为:鉴别两瓶溶液都正确得满分,只有一瓶正确可以及格。四位学生的鉴别结果与老师的评价如下:
请你根据上面四位同学的鉴别结果和老师的评价,回答以下问题:
(1)请根据上述现象确定四种溶液的组成。
答:①____________ 、②____________ 、③____________ 、④____________ 。
(2)若仅用一种试剂并将该试剂依次滴入四种未知就可以一次性加以鉴别,你将选用__________ 。若将该试剂加入①—④四种溶液,请根据(1)的推断结果填写下表:
请写出上述实验中涉及到的反应的化学方程式_________ 、__________ 。
| 学生 | 学生鉴别结果 | 教师评价 |
| 甲 | ③号为食盐水 ④号为稀盐酸 | 四位同学都及格,但是没有一位同学得满分。 |
| 乙 | ①号为稀盐酸 ④号为Ca(OH)2溶液 | |
| 丙 | ②号为稀盐酸 ④号为酚酞试液 | |
| 丁 | ②号为Ca(OH)2溶液 ③号为稀盐酸 |
(1)请根据上述现象确定四种溶液的组成。
答:①
(2)若仅用一种试剂并将该试剂依次滴入四种未知就可以一次性加以鉴别,你将选用
| 液体代号 | ① | ② | ③ | ④ |
| 观察到的现象 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】某固体混合物 A 中可能含硫酸钠、碳酸钠、硝酸钡、氯化铵等物质中的若干种.按 如图所示进行实验,出现的现象如图所述(实验过程中所有发生的反应都恰好完全反应). 根据实验过程和发生的现象做出判断,填写以下空白:
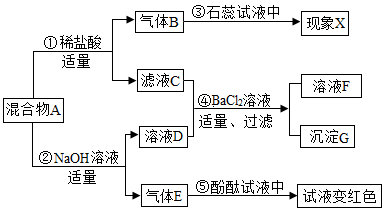
(1)现象 X 是_______ ,气体 E 的化学式为 _______ .
(2)固体混合物 A 中,肯定存在的物质是_______ (写化学式).
(3)写出步骤①中发生反应的化学方程式______ .
(4)仅根据上述实验现象,还不能确定混合物 A 的组成.为确定混合物 A 的成分,可用沉淀 G 再进行实验.方法是取沉淀 G 少许,向其中加入足量稀硝酸,若沉淀全部溶解, 则固体混合物 A 中不含______ (化学式).

(1)现象 X 是
(2)固体混合物 A 中,肯定存在的物质是
(3)写出步骤①中发生反应的化学方程式
(4)仅根据上述实验现象,还不能确定混合物 A 的组成.为确定混合物 A 的成分,可用沉淀 G 再进行实验.方法是取沉淀 G 少许,向其中加入足量稀硝酸,若沉淀全部溶解, 则固体混合物 A 中不含
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】实验室有一包不纯的氯化钾样品,含有的杂质可能是氯化铜、氢氧化钾、氯化钙、氯化钠,碳酸钠中的一种或几种,为了确定其成分,进行如下实验。
步骤I:取少许该粉末,加入足量的蒸馏水,使其完全溶解,只得到无色澄清溶液。
步骤Ⅱ:取步骤I中无色溶液加入BaCl2溶液,产生白色沉淀A。
步骤Ⅲ:另称取少许粉末于烧杯中,加入蒸馏水使其完全溶解,然后加入过量的稀硝酸,再加入足量的硝酸银溶液,充分反应后得到白色沉淀B和无色溶液A。
根据上述实验,回答下列问题:
(1)根据步骤I的现象,可以推测原样品中一定不存在的物质是______ 。
(2)步骤Ⅱ中产生白色沉淀A的化学方程式是______ 。
(3)取少量步骤Ⅱ中的白色沉淀于试管中,加入过量的稀硝酸,观察到的现象是______ 。
(4)通过以上实验,可以推测原样品中一定存在的杂质有______ 。
(5)无色溶液A中一定存在的离子有______ 。
步骤I:取少许该粉末,加入足量的蒸馏水,使其完全溶解,只得到无色澄清溶液。
步骤Ⅱ:取步骤I中无色溶液加入BaCl2溶液,产生白色沉淀A。
步骤Ⅲ:另称取少许粉末于烧杯中,加入蒸馏水使其完全溶解,然后加入过量的稀硝酸,再加入足量的硝酸银溶液,充分反应后得到白色沉淀B和无色溶液A。
根据上述实验,回答下列问题:
(1)根据步骤I的现象,可以推测原样品中一定不存在的物质是
(2)步骤Ⅱ中产生白色沉淀A的化学方程式是
(3)取少量步骤Ⅱ中的白色沉淀于试管中,加入过量的稀硝酸,观察到的现象是
(4)通过以上实验,可以推测原样品中一定存在的杂质有
(5)无色溶液A中一定存在的离子有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】垃圾合理化回收利用可以减少污染,节约资源。黄铁矿制硫酸会产生大量废渣(含FeSO4(质量分数为a%)、Fe2(SO4)3(质量分数为b%)及少量CaO和MgO)可制备黄钠铁矾净水剂和高档颜料铁红(Fe2O3),其流程如图:
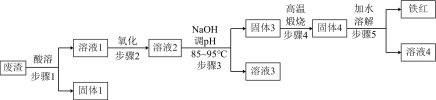
已知:①“固体3”为黄钠铁矾,化学式为:NaFe3(SO4)2(OH)6。
②“溶液4”是含有Na+的可溶盐。
③通过调节pH范围可使某种金属沉淀。如表是物质开始沉淀与沉淀完全的pH。
(1)NaFe3(SO4)2(OH)6中铁元素的化合价为______ ,为使铁元素以黄钠铁矾形式沉淀完全,步骤3调节pH的数值范围为________ ,溶液3中溶质的成分是______ (任写一种)。
(2)“氧化”过程中,需要加入一种将Fe2+氧化为Fe3+的物质,工业上最好选用______ 。
A.空气 B.H2O2 C.MnO2 D.O2
其理由是________ 。
(3)“酸溶”时MgO参加反应的化学方程式为________ 。
(4)步骤5中检验铁红是否洗涤干净的操作是:取最后一次洗涤液少量于试管中,_______ ,证明已洗涤干净。
(5)已知固体废渣质量为m,理论上可产生铁红的质量为_________ (列式即可)。

已知:①“固体3”为黄钠铁矾,化学式为:NaFe3(SO4)2(OH)6。
②“溶液4”是含有Na+的可溶盐。
③通过调节pH范围可使某种金属沉淀。如表是物质开始沉淀与沉淀完全的pH。
| NaFe3(SO4)2(OH)6 | Fe(OH)3 | Mg(OH)2 | |
| 开始沉淀的pH | 1.6 | 2.0 | 8.1 |
| 沉淀完全的pH | 1.8 | 3.2 | 9.4 |
(1)NaFe3(SO4)2(OH)6中铁元素的化合价为
(2)“氧化”过程中,需要加入一种将Fe2+氧化为Fe3+的物质,工业上最好选用
A.空气 B.H2O2 C.MnO2 D.O2
其理由是
(3)“酸溶”时MgO参加反应的化学方程式为
(4)步骤5中检验铁红是否洗涤干净的操作是:取最后一次洗涤液少量于试管中,
(5)已知固体废渣质量为m,理论上可产生铁红的质量为
您最近一年使用:0次