某校实验兴趣小组的同学利用如图所示的装置,对质量守恒定律进行了探究。
设计实验:小云同学将一定质量的白磷放入A装置内,称得A装置的总质量为203.1 g,然后将烧红的玻璃管伸人锥形瓶内,并立即塞紧橡胶塞。
(1)观察现象:此时观察到锥形瓶内的现象是_________________________ ,装置冷却后,再次称得A装置总质量为203.1 g。
(2)总结:①该反应符合质量守恒定律。
②锥形瓶中细沙的作用是________________________________________________ 。
小兵同学认为碳酸钠与稀盐酸反应也符合质量守恒定律。于是他设计了B装置,实验前药品及装置的总质量为300.4 g,反应结束后,他与小云的实验进行了以下对比:
(3)①冷却至室温,气球胀大的是___________________ (填“A”“B"或"A和B”)。
②称量反应后药品及装置的总质量为300.0 g,你认为数据减小的原因可能是________________ (填字母)。
A.稀盐酸不足
B.碳酸钠中含有不与稀盐酸反应的杂质
C.装置气密性不好
D.气球受到浮力的影响
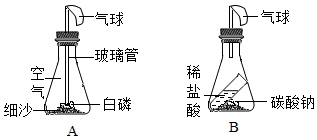
设计实验:小云同学将一定质量的白磷放入A装置内,称得A装置的总质量为203.1 g,然后将烧红的玻璃管伸人锥形瓶内,并立即塞紧橡胶塞。
(1)观察现象:此时观察到锥形瓶内的现象是
(2)总结:①该反应符合质量守恒定律。
②锥形瓶中细沙的作用是
小兵同学认为碳酸钠与稀盐酸反应也符合质量守恒定律。于是他设计了B装置,实验前药品及装置的总质量为300.4 g,反应结束后,他与小云的实验进行了以下对比:
(3)①冷却至室温,气球胀大的是
②称量反应后药品及装置的总质量为300.0 g,你认为数据减小的原因可能是
A.稀盐酸不足
B.碳酸钠中含有不与稀盐酸反应的杂质
C.装置气密性不好
D.气球受到浮力的影响
22-23九年级上·全国·课后作业 查看更多[1]
(已下线)第五单元课题1 质量守恒定律(第02课时)-2022-2023学年九年级化学上册课后分层作业(人教版)
更新时间:2022/11/24 09:15:40
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
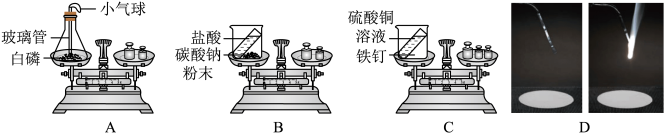
【推荐1】某化学课外小组同学用如图所示实验探究质量守恒定律:______ 。
(2)乙同学用B装置研究质量守恒定律时,一段时间后发现天平的指针偏右,造成天平的指针向右偏转的原因是______ 。
(3)丙同学用C实验说明了质量守恒定律,C实验能在敞口容器中进行实验的原因______ 。
(4)丁同学用图D中的镁带在空气中燃烧的实验来探究质量守恒定律时,发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是______ 。
(5)综上所述,A、B、C、D所示四个实验中能用质量守恒定律解释的是实验______ (选填字母序号)。
(2)乙同学用B装置研究质量守恒定律时,一段时间后发现天平的指针偏右,造成天平的指针向右偏转的原因是
(3)丙同学用C实验说明了质量守恒定律,C实验能在敞口容器中进行实验的原因
(4)丁同学用图D中的镁带在空气中燃烧的实验来探究质量守恒定律时,发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是
(5)综上所述,A、B、C、D所示四个实验中能用质量守恒定律解释的是实验
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】化学小组利用图1所示密闭装置,分别探究红磷和蜡烛(含C、H元素)在其中燃烧时氧气含量的变化情况,测得图2所示的数据。
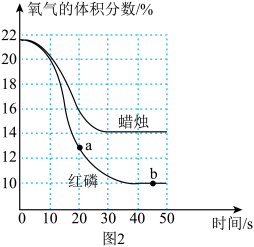
(1)红磷燃烧过程中,a点和b点对应的容器内物质总质量_________ (填“变大”“变小”或“不变”)。从0到20s,红磷燃烧消耗氧气的速率由慢变快的原因是_________ 。
(2)若将足量的、燃着的红磷和蜡烛,同时放入同一密闭装置(保持两者火焰高度一致)。推测两者熄灭的顺序为_________ ,理由是_________ 。
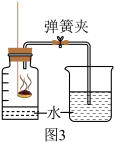
(3)图3是教材中测定空气中氧气含量的实验装置,说明该实验用红磷比蜡烛更适合的原因_____ (写出两点)。


(1)红磷燃烧过程中,a点和b点对应的容器内物质总质量
(2)若将足量的、燃着的红磷和蜡烛,同时放入同一密闭装置(保持两者火焰高度一致)。推测两者熄灭的顺序为
(3)图3是教材中测定空气中氧气含量的实验装置,说明该实验用红磷比蜡烛更适合的原因

您最近一年使用:0次
实验题
|
适中
(0.65)
真题
解题方法
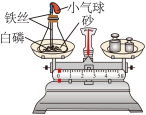
【推荐3】定律是对自然现象或关系的描述,通常可用数学方式加以表达。在学习“质量守恒定律”时,小丽查阅到以下材料:______ ;
(2)质量守恒定律的发现过程,带给我们的启示有______(填字母);
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在白磷燃烧前后质量测定实验中(如图),气球的作用有______ ;______ 。

(2)质量守恒定律的发现过程,带给我们的启示有______(填字母);
| A.要善于总结前人的成果和经验 |
| B.实验的成功与否,取决于药品的选择 |
| C.定量方法是科学研究的重要方法 |
受上述研究启发,小丽对相关实验进行了深入探究。
(3)在白磷燃烧前后质量测定实验中(如图),气球的作用有
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净后在天平上称得质量为56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉一起放在天平上称量,记录所称得质量m1。将上述铁钉浸到硫酸铜溶液中,待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和铁钉的锥形瓶放在天平上称量,记录所称的质量为m2。
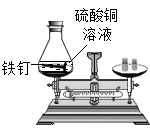
(1)m1______ m2(填“>”或“=”或“<”)
(2)锥形瓶的质量为______ (用含m1或m2的代数式表示)。
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。
(4)小明同学在做该实验时,忘记了将表面有少许铁锈的铁钉打磨,就直接称量后再完全反应,则m1______ m2(填“>”或“=”或“<”)。
(5)反应前,经测量某硫酸铜的浓溶液的pH=2.6,该硫酸铜溶液与铁的反应中发现铁钉表面有少量气泡,除水蒸气外,应当是______ (写一种)。

(1)m1
(2)锥形瓶的质量为
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。
(4)小明同学在做该实验时,忘记了将表面有少许铁锈的铁钉打磨,就直接称量后再完全反应,则m1
(5)反应前,经测量某硫酸铜的浓溶液的pH=2.6,该硫酸铜溶液与铁的反应中发现铁钉表面有少量气泡,除水蒸气外,应当是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】根据下图所示的实验回答问题:___________ (填“能”或“不能”)用来测定空气中氧气的含量;
(2)实验二用来验证质量守恒定律,其中气球的作用是___________ ;
(3)实验三可以说明物质的溶解性与___________ 有关。

(2)实验二用来验证质量守恒定律,其中气球的作用是
(3)实验三可以说明物质的溶解性与
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】a.质量守恒定律是物质科学中的一条重要规律。
(1)某科学兴趣小组的同学设计了A、B、C三个实验装置(天平略)来验证质量守恒律,其中,只有A装置能用来验证质量守恒定律,写出A中反应的化学方程式___________ 。B、C装置则不能,否定B、C装置的理由分别是:B___________ ;C___________ 。
(2)小明将C装置进行改进,如图D所示。
①此实验的现象是___________ 。
②待完全反应后,将装置D置于天平上称量,所得数据较反应前的小。若整个操作过程无差错,则造成上述实验误差的原因是___________ 。
b.实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:___________ ,检验二氯化碳是否集满的方法是___________ ,收集二氧化碳的装置可选择___________ 。
(4)若用高锰酸钾制取氧气,反应的化学方程式是___________ 。
(5)若用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是___________(填字母)。
(6)浓硫酸具有吸水性,若要除去氧气中混有的水蒸气,气体应从F装置的___________ 端进入。
(1)某科学兴趣小组的同学设计了A、B、C三个实验装置(天平略)来验证质量守恒律,其中,只有A装置能用来验证质量守恒定律,写出A中反应的化学方程式
|
|
|
| A.白磷燃烧 | B.酒精与水混合 | C.石灰石与稀盐酸反应 |
(2)小明将C装置进行改进,如图D所示。
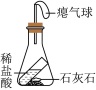
①此实验的现象是
②待完全反应后,将装置D置于天平上称量,所得数据较反应前的小。若整个操作过程无差错,则造成上述实验误差的原因是
b.实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
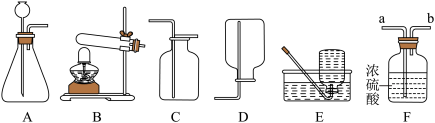
(4)若用高锰酸钾制取氧气,反应的化学方程式是
(5)若用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是___________(填字母)。
| A.③④①②⑤ | B.④③①②⑤ | C.④③①⑤② | D.①②③④⑤ |
(6)浓硫酸具有吸水性,若要除去氧气中混有的水蒸气,气体应从F装置的
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】为测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究(假设实验步骤与操作正确)。

(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开止水夹,观察到烧杯内有水倒流入集气瓶内,发生的反应方程式为_______ 。
(2)乙同学:用碳替代红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是_______ 。
(3)丙同学:向集气瓶中加入少量的氢氧化钠溶液,然后完成了乙同学的实验,得到了与甲同学相同的实验结果,则氢氧化钠溶液起到的作用是_______ 。

(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开止水夹,观察到烧杯内有水倒流入集气瓶内,发生的反应方程式为
(2)乙同学:用碳替代红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是
(3)丙同学:向集气瓶中加入少量的氢氧化钠溶液,然后完成了乙同学的实验,得到了与甲同学相同的实验结果,则氢氧化钠溶液起到的作用是
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组用如图所示实验装置测定空气中氧气含量。_______ ,发生反应的文字表达式是_______ 。
(2)图Ⅰ中,BC段压强增大的原因是_______ ,DE段压强增大的操作是_______ 。
(3)实验前广口瓶内空气体积为V,烧杯中水的体积是V1,实验后烧杯中剩余水的体积为V2,则空气中氧气的体积分数的表达式为_______ (用V、V1、V2表示)。
(4)若实验测得的氧气体积分数小于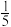 ,则可能的原因是
,则可能的原因是_______ (写一个)。
(5)小明同学取足量的红磷、镁条、木炭分别在等体积的A、B、C三瓶空气中同时燃烧;充分燃烧后恢复到常温再松开止水夹,发现集气瓶B中进水最多,C中几乎没有水进入。
查阅资料:镁是一种化学性质比较活泼的金属,把镁条在空气中点燃,不仅能与氧气反应,而且还能与化学性质不活泼的氮气反应生成淡黄色固体氮化镁;木炭在空气中燃烧生成二氧化碳气体。_______ ,写出镁与氧气反应的文字表达式_______ 。
②C的集气瓶中没有水进入的原因是_______ 。
③以上实验说明,在“测定空气中氧气体积含量”实验中,药品的选择要考虑的因素有:_______ (写1点)。

(2)图Ⅰ中,BC段压强增大的原因是
(3)实验前广口瓶内空气体积为V,烧杯中水的体积是V1,实验后烧杯中剩余水的体积为V2,则空气中氧气的体积分数的表达式为
(4)若实验测得的氧气体积分数小于
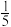 ,则可能的原因是
,则可能的原因是(5)小明同学取足量的红磷、镁条、木炭分别在等体积的A、B、C三瓶空气中同时燃烧;充分燃烧后恢复到常温再松开止水夹,发现集气瓶B中进水最多,C中几乎没有水进入。
查阅资料:镁是一种化学性质比较活泼的金属,把镁条在空气中点燃,不仅能与氧气反应,而且还能与化学性质不活泼的氮气反应生成淡黄色固体氮化镁;木炭在空气中燃烧生成二氧化碳气体。
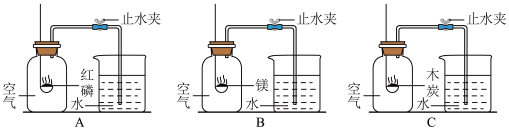
②C的集气瓶中没有水进入的原因是
③以上实验说明,在“测定空气中氧气体积含量”实验中,药品的选择要考虑的因素有:
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】建构合理的思维模型,既能促进深度学习,又能提高思维品质,小科建构了“两组分混合物含量测定”的思维模型;
【探究一】根据沸点低的组分先汽化的性质,测定混合物中某组分的含量。
(1)将空气转变为液态空气,液氮先汽化。从建模角度分析,该操作属于上述思维模型中的______ ;
【探究二】根据混合物中某组分发生化学反应,测定混合物中某组分的含量。
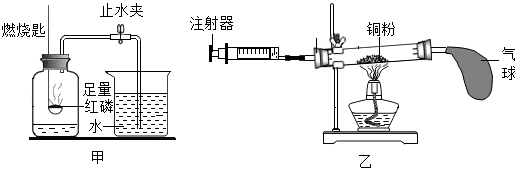
(2)按图甲装置测定空气中氧气含量时,止水夹最合理的打开时间是_______ (填“反应刚结束时”或“冷却到室温时”)。
(3)已知:在氧气不充足时,碳与氧气反应生成一氧化碳,一氧化碳不溶于水且不与水反应,小科用足量木炭替换红磷,规范操作后,测得的氧气含量将________ (填“偏大”“偏小”或“不变”);
【继续探究】
(4)运用上述思维模型,小科又设计了图乙的实验装置,其“测定空气中氧气含量”的原理是:铜和装置中的氧气反应,生成氧化铜固体,_______ 为装置内氧气的体积。
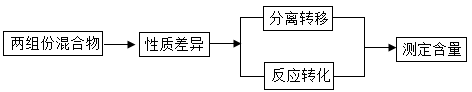
【探究一】根据沸点低的组分先汽化的性质,测定混合物中某组分的含量。
(1)将空气转变为液态空气,液氮先汽化。从建模角度分析,该操作属于上述思维模型中的
【探究二】根据混合物中某组分发生化学反应,测定混合物中某组分的含量。
(2)按图甲装置测定空气中氧气含量时,止水夹最合理的打开时间是
(3)已知:在氧气不充足时,碳与氧气反应生成一氧化碳,一氧化碳不溶于水且不与水反应,小科用足量木炭替换红磷,规范操作后,测得的氧气含量将
【继续探究】
(4)运用上述思维模型,小科又设计了图乙的实验装置,其“测定空气中氧气含量”的原理是:铜和装置中的氧气反应,生成氧化铜固体,
您最近一年使用:0次