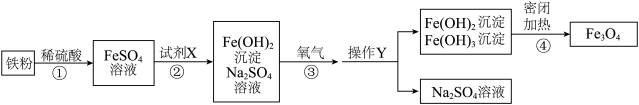
某化工厂用石灰乳对工业烟气进行脱硫,同时生产化工产品石膏(CaSO4)的工艺流程如图:______ 。
(2)步骤①中发生反应的化学方程式为______ 。
(3)步骤②的操作名称为______ ,该操作后液体仍然浑浊的原因可能是______ (写一点)。
(4)该工艺流程的价值是______ 。
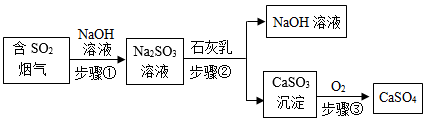
(2)步骤①中发生反应的化学方程式为
(3)步骤②的操作名称为
(4)该工艺流程的价值是
2023·安徽合肥·一模 查看更多[2]
更新时间:2023/04/07 17:16:54
|
相似题推荐
【推荐1】“碳中和”,我们一直在行动。我国宣布在2060年前实现碳中和,“碳封存”与“碳转化”是实现碳中和目标不可或缺的重要技术选择。
(1)“碳封存”。2023年6月1日,我国首个海上二氧化碳封存示范工程项目成功投入使用,填补了我国海上二氧化碳封存技术的空白。该技术是将油井开采产生的油气混合物注入高碳分离器,再将分离出的二氧化碳通入压缩机加压和干燥,使其变成介于气态和液态之间的超临界状态。超临界状态二氧化碳密度高,接近液态二氧化碳;黏度小,流动快,接近气态二氧化碳。
①从微观角度分析二氧化碳易被压缩的原因:___________ 。
②为了防止对输送管道内部造成腐蚀,输送超临界CO2的管道材料采用不锈钢等,同时对CO2进行干燥处理。请解释CO2需干燥的原因:___________ (用化学方程式表示)。
③下列对超临界二氧化碳的理解正确的是___________ (填字母序号)。
A.超临界二氧化碳与二氧化碳的组成不同
B.超临界二氧化碳容易燃烧
C.同等条件下,超临界二氧化碳的输送量比二氧化碳更大
D.超临界二氧化碳存在于特定的条件下,条件改变,状态改变
(2)“碳转化”。利用二氧化碳资源开发化工原料,合成化工产品,有着广阔的前景。
①二氧化碳与氨气在一定条件下可以合成尿素 ,同时生成水,该反应的化学方程式为
,同时生成水,该反应的化学方程式为___________ 。
②在一定条件下,利用新型电解装置将二氧化碳转化为甲酸(HCOOH),化学方程式为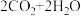

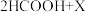 ,X的化学式为
,X的化学式为___________ 。
③从物质类别角度分析,①和②两个反应实现了___________ 的转化。
(3)碳中和,人人参与,低碳生活从我做起,你的低碳行动是___________ (写一条即可)。
(1)“碳封存”。2023年6月1日,我国首个海上二氧化碳封存示范工程项目成功投入使用,填补了我国海上二氧化碳封存技术的空白。该技术是将油井开采产生的油气混合物注入高碳分离器,再将分离出的二氧化碳通入压缩机加压和干燥,使其变成介于气态和液态之间的超临界状态。超临界状态二氧化碳密度高,接近液态二氧化碳;黏度小,流动快,接近气态二氧化碳。
①从微观角度分析二氧化碳易被压缩的原因:
②为了防止对输送管道内部造成腐蚀,输送超临界CO2的管道材料采用不锈钢等,同时对CO2进行干燥处理。请解释CO2需干燥的原因:
③下列对超临界二氧化碳的理解正确的是
A.超临界二氧化碳与二氧化碳的组成不同
B.超临界二氧化碳容易燃烧
C.同等条件下,超临界二氧化碳的输送量比二氧化碳更大
D.超临界二氧化碳存在于特定的条件下,条件改变,状态改变
(2)“碳转化”。利用二氧化碳资源开发化工原料,合成化工产品,有着广阔的前景。
①二氧化碳与氨气在一定条件下可以合成尿素
 ,同时生成水,该反应的化学方程式为
,同时生成水,该反应的化学方程式为②在一定条件下,利用新型电解装置将二氧化碳转化为甲酸(HCOOH),化学方程式为
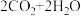

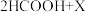 ,X的化学式为
,X的化学式为③从物质类别角度分析,①和②两个反应实现了
(3)碳中和,人人参与,低碳生活从我做起,你的低碳行动是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】已如A~F六种物质均为初中化学常见物,其中B为年产量最高的金属。如图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“—”表示相互反应)。请回答:
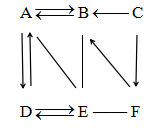
(1)B的化学式:______ ;
(2)E和F反应的化学方程式:______ 。
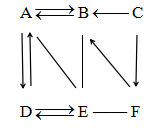
(1)B的化学式:
(2)E和F反应的化学方程式:
您最近一年使用:0次
【推荐1】小荀同学用如图所示装置,分别进行“燃烧条件”和“氧气性质”的探究实验(已知:白磷的着火点为40℃),请回答下列问题。
(1)H2O2与MnO2接触时,发生反应的化学方程式为___________ 。
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,燃烧匙中的白磷不燃烧的原因是___________ ;
步骤3:打开止水夹,继续推入H2O2溶液,烧杯中观察到的现象是___________ 。
(3)实验2中,步骤3:打开止水夹,快速推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是___________ ,木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶中,集气瓶中观察到的现象是___________ 。
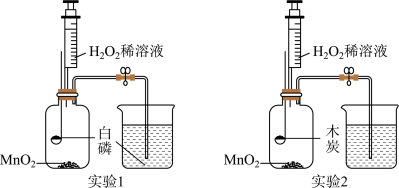
| 内容步骤 | (实验1)燃烧条件 | (实验2)氧气性质 |
| 步骤1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷、塞紧瓶塞 | 烧杯中盛有Ca(OH)2溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| 步骤2 | 推入适量H2O2溶液 | 慢慢推入少量H2O2溶液 |
(1)H2O2与MnO2接触时,发生反应的化学方程式为
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,燃烧匙中的白磷不燃烧的原因是
步骤3:打开止水夹,继续推入H2O2溶液,烧杯中观察到的现象是
(3)实验2中,步骤3:打开止水夹,快速推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】随着对“火”的认识和使用,人类能够更好地改造自然、改善生活。
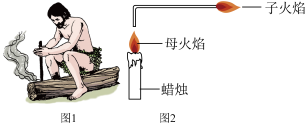
(1)如图1所示,古人“钻木取火”过程中,快速搓动木棍使底部的干草着火,从“燃烧条件”分析:“钻木”为干草燃烧提供的条件是_______________ ;
(2)形状大小相同的木炭在下列气体中燃烧的现象如表所示,回答问题:
①木炭在空气中和氧气中燃烧现象不同的原因是(答一点)________________ ;
②生成的气体使澄清石灰水变浑浊的化学方程式_______________________ ;
③根据表中信息,写一条对“燃烧条件”的新认识________________________ ;
④木炭在臭氧(O3)中燃烧的化学方程式为____________________________ ;
(3)如图2所示,1860年英国化学家法拉第做了一个有趣的“母子火焰”实验。经研究:子火焰中燃烧物为石蜡蒸汽,子火焰为石蜡蒸汽燃烧产生的。
①蜡烛能产生子火焰这一现象,证明石蜡具有的物理性质是_____________ (写一点,下同),化学性质是___________ ;
②该实验成功的关键因素之一是导气管不宜太长,其原因是_____________ 。

(1)如图1所示,古人“钻木取火”过程中,快速搓动木棍使底部的干草着火,从“燃烧条件”分析:“钻木”为干草燃烧提供的条件是
(2)形状大小相同的木炭在下列气体中燃烧的现象如表所示,回答问题:
| 不同气体中 | 在空气中 | 在氧气中 | 在臭氧中 |
| 实验现象 | 红热 | 剧烈燃烧 | 非常剧烈地燃烧 |
| 生成的气体能使澄清石灰水变浑浊 | |||
②生成的气体使澄清石灰水变浑浊的化学方程式
③根据表中信息,写一条对“燃烧条件”的新认识
④木炭在臭氧(O3)中燃烧的化学方程式为
(3)如图2所示,1860年英国化学家法拉第做了一个有趣的“母子火焰”实验。经研究:子火焰中燃烧物为石蜡蒸汽,子火焰为石蜡蒸汽燃烧产生的。
①蜡烛能产生子火焰这一现象,证明石蜡具有的物理性质是
②该实验成功的关键因素之一是导气管不宜太长,其原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】为应对全球气候问题,中国力争2060年前实现“碳中和”。“碳中和”涉及“碳排放”和“碳捕集”两个主要方面。结合下图关系回答有关问题:
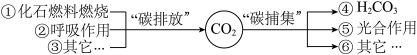
(1)①是产生“碳排放”的重要来源,人类燃烧化石燃料的主要目的是______________ 。
(2)②、⑤是实现“碳中和”的自然生态途径,参与该途径另一种常见气体是____________ 。
(3)利用海水通过④进行“碳捕集”,海水的pH将____________ (填“增大”或“减小”)。
(4)利用NaOH实现“碳捕集”是目前的重要研究方向。该方案NaOH参与的反应方程式为___ 。
(5)燃烧等质量的甲烷和乙醇,产生“碳排放”更多的是____________ 。

(1)①是产生“碳排放”的重要来源,人类燃烧化石燃料的主要目的是
(2)②、⑤是实现“碳中和”的自然生态途径,参与该途径另一种常见气体是
(3)利用海水通过④进行“碳捕集”,海水的pH将
(4)利用NaOH实现“碳捕集”是目前的重要研究方向。该方案NaOH参与的反应方程式为
(5)燃烧等质量的甲烷和乙醇,产生“碳排放”更多的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】某工厂生产的铜屑中含有少量铁屑,现要回收利用其中的铜,需除去其中铁屑,张山同学设计了如下图所示的甲、乙两个实验方案:
甲: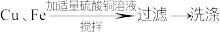
乙: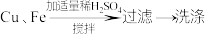
(1)以上两个实验方案中,从回收利用率角度考虑,你愿意选择______ 。
(2)两个方案中都有过滤操作,该操作中必须用到的玻璃仪器有______ 。
(3)写出两个实验方案中有关反应方程式:
方案甲______ ;
方案乙______ 。
(4)你能否再设计一个不同原理的方案?写出你的方案______ 。
甲:
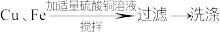
乙:
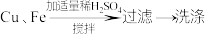
(1)以上两个实验方案中,从回收利用率角度考虑,你愿意选择
(2)两个方案中都有过滤操作,该操作中必须用到的玻璃仪器有
(3)写出两个实验方案中有关反应方程式:
方案甲
方案乙
(4)你能否再设计一个不同原理的方案?写出你的方案
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】实验室从含有 CuSO4、ZnSO4、FeSO4 的废液中回收工业原料硫酸锌和有关金属的流程如下:
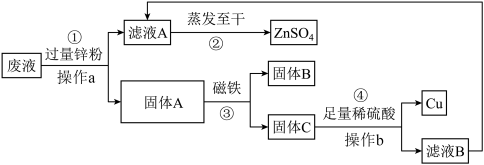
请回答:
(1)操作a、操作b均为__________ ,该操作用到的玻璃仪器为 _____ 、玻璃棒、烧杯。
(2)滤液 A 和滤液 B 含有相同的溶质,其名称是_____ ;固体 B 的化学式为 _____ 。
(3)步骤①中加入过量锌粉的目的让废液中的_______ 完全反应;步骤④加入足量稀硫酸有气泡产生,反应的化学方程式为 __________ 。
(4)该流程中发生的置换反应共有__________ 个。

请回答:
(1)操作a、操作b均为
(2)滤液 A 和滤液 B 含有相同的溶质,其名称是
(3)步骤①中加入过量锌粉的目的让废液中的
(4)该流程中发生的置换反应共有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
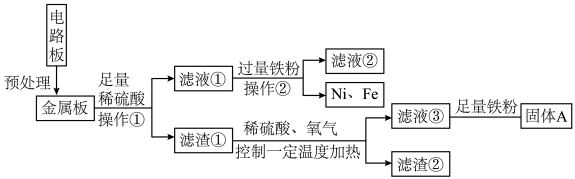
【推荐3】我国每年对金属的需求巨大,金属资源的回收再利用一直是我国实现可持续发展的重要项目。某电器的废旧电路板中还有 Fe、Cu、Ag、Ni(镍,银白色金属) 等金属,下图是某车间回收部分金属的工艺流程。已知: 。
。__________ ,金属板在与稀硫酸反应之前一般要进行粉碎处理,粉碎的目的是 ____________ 。
(2)根据以上工艺流程图,可以得出 Ni、Fe 的金属活动性强弱顺序是 Ni__________ Fe(填“>”或“<”)。
(3)固体 A 除主要含有铜外,还含有一定量的铁。为了进一步提纯铜,可以向固体 A 中加入稀硫酸后过滤,其反应方程式为__________ 。
(4)金属板中的铜在浓硫酸中加热可以直接溶解,生成蓝色的硫酸铜溶液,同时放出刺激性气味的气体。请写出铜与浓硫酸反应的化学方程式_________ 。处理铜时选用稀硫酸并通入氧气优于选用浓硫酸的原因是_______ 。
 。
。
(2)根据以上工艺流程图,可以得出 Ni、Fe 的金属活动性强弱顺序是 Ni
(3)固体 A 除主要含有铜外,还含有一定量的铁。为了进一步提纯铜,可以向固体 A 中加入稀硫酸后过滤,其反应方程式为
(4)金属板中的铜在浓硫酸中加热可以直接溶解,生成蓝色的硫酸铜溶液,同时放出刺激性气味的气体。请写出铜与浓硫酸反应的化学方程式
您最近一年使用:0次